Clear Sky Science · pt
Síntese da 3-desoxicollinocetona B e sua capacidade de reduzir proteínas mal dobradas associadas ao Alzheimer
Um Novo Ângulo sobre o Alzheimer
A doença de Alzheimer é impulsionada em parte por aglomerados de proteínas mal dobradas que danificam o cérebro gradualmente, mas os tratamentos atuais fazem pouco para remover esses depósitos nocivos. Este estudo apresenta um análogo sintético de um composto natural raro que alcança o cérebro de forma mais eficaz e ataca diretamente duas proteínas problemáticas ao mesmo tempo. Ao combinar química avançada, inteligência artificial e estudos em animais, os pesquisadores mostram como essa pequena molécula desagrega agregados proteicos tóxicos e melhora a memória em modelos de camundongo de Alzheimer.
Uma Molécula Natural com Limitações
Pesquisadores descobriram anteriormente um produto natural bacteriano chamado collinolactona que pode desmontar aglomerados de proteínas formados por amiloide-beta e tau — duas proteínas emblemáticas da doença de Alzheimer. Entretanto, a collinolactona é difícil de extrair em quantidades úteis de sua fonte microbiana e tem acesso limitado a certas regiões do cérebro, especialmente o córtex, onde grande parte do dano do Alzheimer ocorre. Essas limitações dificultam seu desenvolvimento como fármaco prático. A equipe propôs projetar e sintetizar uma molécula relacionada que preservasse a atividade benéfica da collinolactona, ao mesmo tempo em que melhorasse sua estabilidade e sua capacidade de penetrar no cérebro.
Construindo uma Molécula Mais Inteligente
Usando síntese orgânica moderna, os pesquisadores construíram um novo composto chamado 3-desoxicollinocetona B. Eles montaram três blocos químicos mais simples e então desencadearam uma rara reação de fechamento de anel que imita uma etapa acreditada ocorrer na natureza. Cálculos computacionais detalhados explicaram por que essa reação favorece uma conformação específica de três anéis, mais estável que estruturas alternativas. A molécula resultante é ligeiramente mais lipofílica que o produto natural original, uma propriedade que se espera ajudar sua passagem pela barreira hematoencefálica. Importante, a rota sintética é escalável, o que significa que quantidades em escala de gramas podem ser produzidas de forma confiável no laboratório para testes biológicos extensivos e otimização futura. 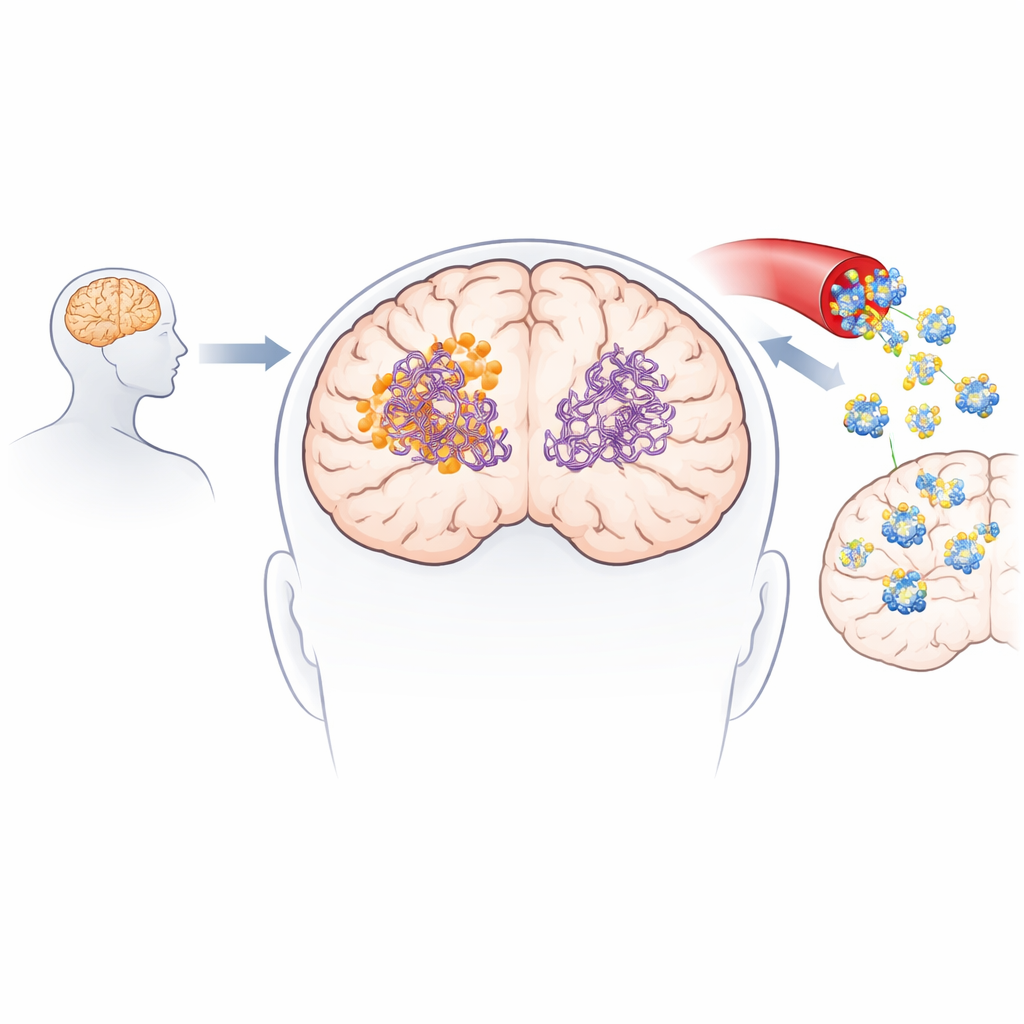
Simulações Revelam Como Ela Se Encaixa em Fibras Tóxicas
Para entender como a nova molécula pode interagir com proteínas causadoras de doença, a equipe recorreu à inteligência artificial e a simulações moleculares. Eles utilizaram modelos de acoplamento (docking) de última geração para explorar milhares de formas pelas quais o composto poderia se ligar a fibras pré-formadas de amiloide-beta e tau. Os cálculos mostraram de modo consistente que a 3-desoxicollinocetona B se liga mais fortemente a ambos os tipos de fibras do que a collinolactona, aninhando-se em bolsões hidrofóbicos (repelentes à água) e formando contatos estabilizadores como ligações de hidrogênio e pontes salinas. Simulações de dinâmica molecular acompanharam então as fibras ao longo do tempo e revelaram que, uma vez ligada, a molécula aumenta a flexibilidade local e enfraquece contatos críticos entre as fitas proteicas, encaminhando as fibras para a quebra estrutural.
Do Tubo de Ensaio ao Cérebro de Camundongos
Experimentos de laboratório confirmaram que a 3-desoxicollinocetona B não apenas desacelera a formação de novas fibras de amiloide-beta e tau, mas também desfaz ativamente fibras já existentes e oligômeros menores e altamente tóxicos. Em ensaios sem células, ela reduziu fibras e oligômeros de amiloide-beta em proporções significativas e mostrou efeitos ainda mais fortes sobre fragmentos de tau centrais para a formação de emaranhados. A molécula atravessou modelos artificiais e biológicos da barreira hematoencefálica e foi detectável nos cérebros de camundongos após administração intravenosa e oral. Em dois modelos murinos diferentes semelhantes ao Alzheimer, tratamentos de curto e mais longo prazo reduziram níveis de placas amiloides e espécies amiloides solúveis, diminuíram marcadores de inflamação cerebral, restauraram parcialmente proteínas sinápticas e melhoraram o desempenho em tarefas de memória e aprendizagem, como o labirinto em Y e o reconhecimento de novo objeto. 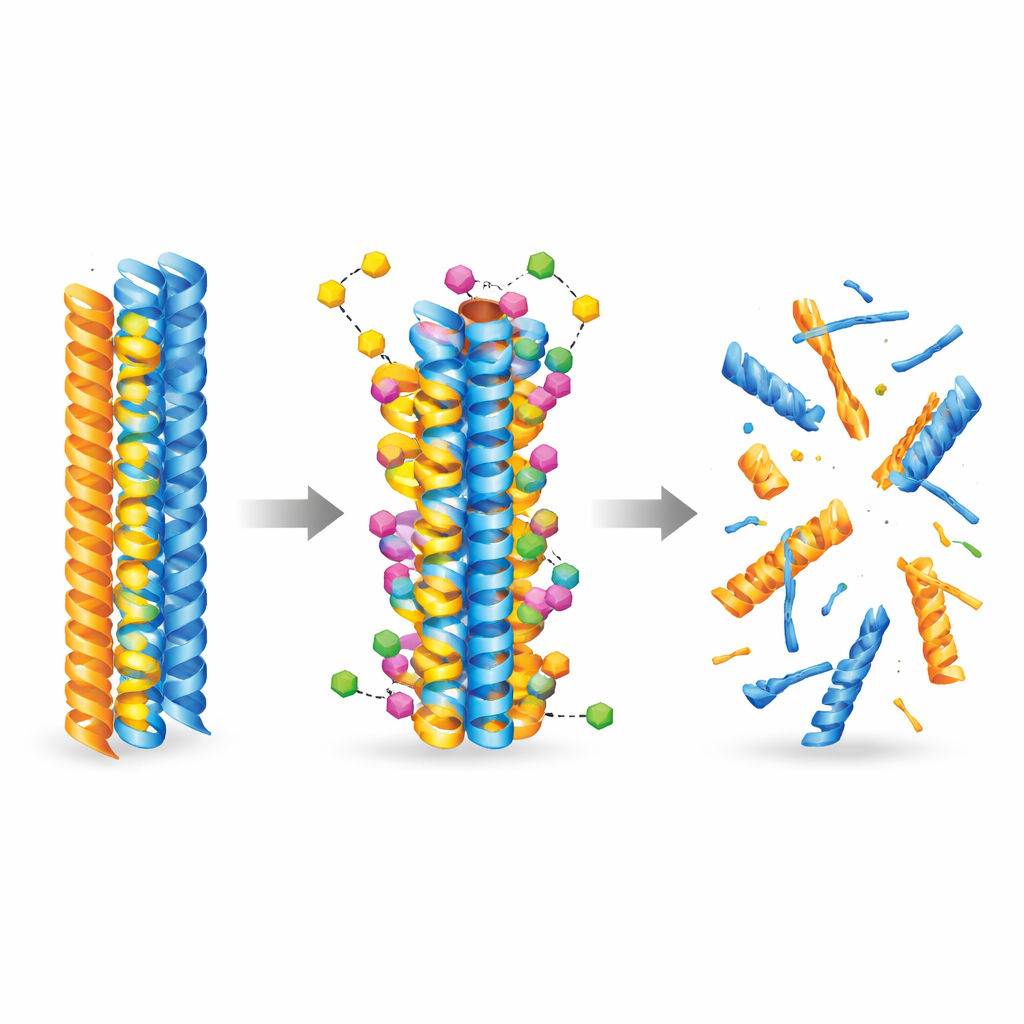
Promessa e Próximos Passos
No geral, o estudo demonstra que a 3-desoxicollinocetona B é uma pequena molécula de ação dupla que pode entrar no cérebro, ligar-se fortemente tanto a agregados de amiloide-beta quanto de tau e promover sua desagregação, levando a benefícios cognitivos mensuráveis em camundongos. Para um leigo, isso significa que o composto age um pouco como um solvente molecular para dois tipos-chave de aglomerados proteicos relacionados ao Alzheimer, em vez de apenas mascarar sintomas. Embora a molécula seja eliminada relativamente rápido do organismo e precise de ajustes adicionais para persistir mais tempo na corrente sanguínea, sua síntese escalável, penetração cerebral e ampla atividade contra proteínas mal dobradas a tornam um ponto de partida promissor para desenvolver tratamentos mais acessíveis e econômicos que ataquem a doença de Alzheimer em sua raiz.
Citação: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Palavras-chave: Doença de Alzheimer, amiloide-beta, proteína tau, terapia com pequenas moléculas, agregados proteicos