Clear Sky Science · sv
Syntes av 3-desoxycollinoketone B och dess förmåga att minska Alzheimersassocierade felveckade proteiner
En ny vinkel på Alzheimer
Alzheimers sjukdom drivs delvis av klumpar av felveckade proteiner som långsamt skadar hjärnan, men dagens behandlingar gör föga för att avlägsna dessa skadliga avlagringar. I denna studie presenteras en laboratorieframställd släkting till en sällsynt naturförening som når hjärnan mer effektivt och angriper två stora problemproteiner samtidigt. Genom att kombinera avancerad kemi, artificiell intelligens och djurstudier visar forskarna hur denna småmolekyl bryter ned giftiga proteinaggregat och förbättrar minnet i musmodeller för Alzheimer.
En naturlig molekyl med begränsningar
Forskare upptäckte tidigare en bakteriell naturprodukt kallad collinolacton som kan demontera proteinklumpar bildade av amyloid-beta och tau—två kännetecknande proteiner för Alzheimers sjukdom. Collinolacton är dock svår att utvinna i användbara mängder från sin mikrobiella källa och har dålig tillgång till vissa hjärnområden, särskilt cortex, där en stor del av skadan vid Alzheimer uppstår. Dessa nackdelar försvårar utvecklingen till ett praktiskt läkemedel. Teamet gav sig därför i kast med att utforma och syntetisera en närbesläktad molekyl som bibehåller collinolactons fördelaktiga aktivitet samtidigt som den får bättre stabilitet och förmåga att ta sig in i hjärnan.
Bygga en smartare molekyl
Med modern organisk syntes konstruerade forskarna en ny förening kallad 3-desoxycollinoketone B. De satte ihop tre enklare kemiska byggstenar och utlöste därefter en sällsynt ringbildande reaktion som efterliknar ett steg man tror sker i naturen. Utförliga datorberäkningar förklarade varför denna reaktion gynnar en specifik trefaldig ringskonstruktion som är mer stabil än alternativa strukturer. Den framställda molekylen är något mer fettlöslig än den ursprungliga naturprodukten, en egenskap som förväntas hjälpa den att passera blod-hjärnbarriären. Viktigt är att den syntetiska vägen är skalbar, vilket innebär att gramnivåer kan produceras pålitligt i laboratoriet för omfattande biologisk testning och framtida optimering. 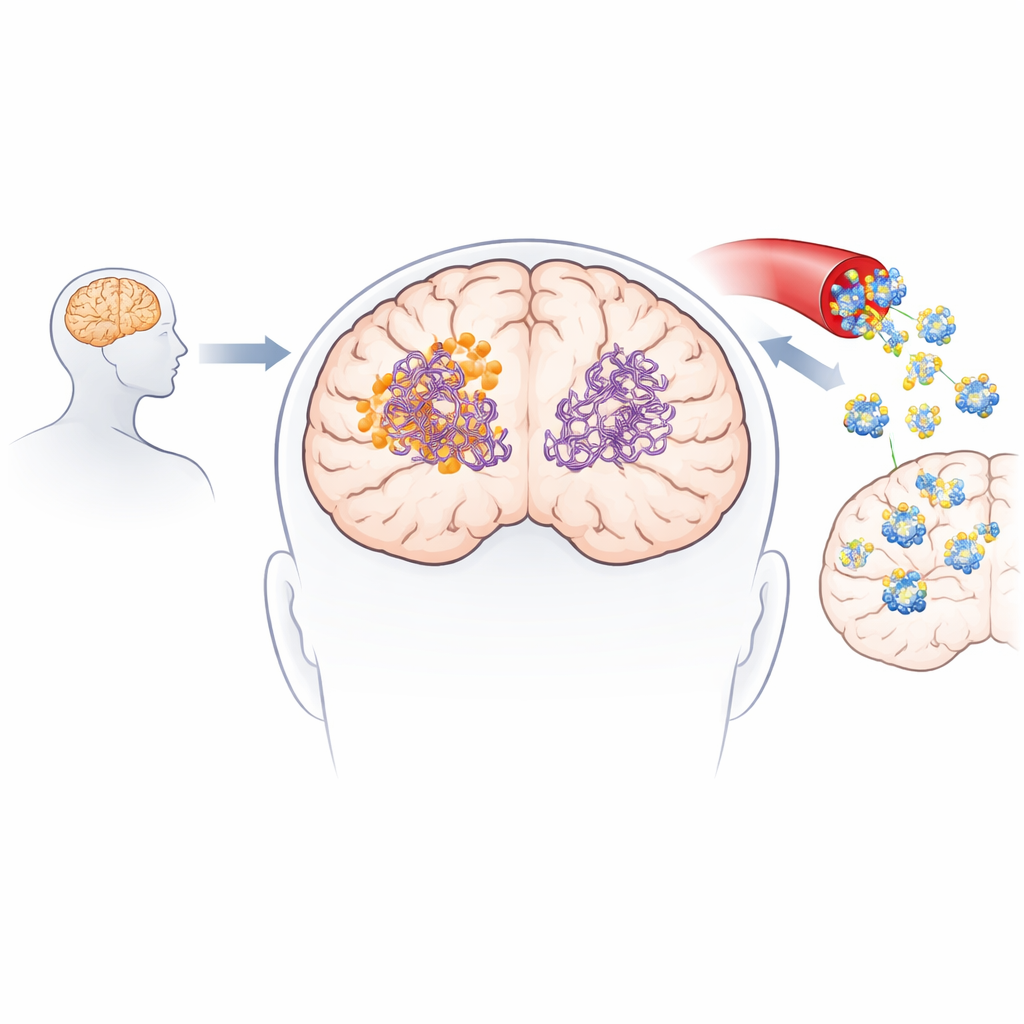
Simuleringar visar hur den greppar giftiga fibrer
För att förstå hur den nya molekylen kan interagera med sjukdomsorsakande proteiner vände sig teamet till artificiell intelligens och molekylära simuleringar. De använde toppmoderna dockingmodeller för att utforska tusentals sätt som föreningen kunde fästa vid redan bildade amyloid-beta- och taufibrer. Beräkningarna visade konsekvent att 3-desoxycollinoketone B binder starkare till båda typerna av fibrer än collinolacton, genom att lägga sig i hydrofoba (vattenavstötande) fickor och bilda stabiliserande kontakter som vätebindningar och saltbryggor. Molekylära dynamiksimuleringar följde sedan fibrerna över tid och avslöjade att när föreningen väl är bundet ökar den lokal flexibilitet och försvagar kritiska kontakter mellan proteinsträngar, vilket knuffar fibrerna mot strukturellt sönderfall.
Från provrör till mushjärnor
Laboratorieexperiment bekräftade att 3-desoxycollinoketone B inte bara bromsar bildningen av nya amyloid-beta- och taufibrer, utan även aktivt bryter sönder existerande fibrer och mindre, mycket toxiska oligomerer. I cellfria tester reducerade den amyloid-beta-fibrer och oligomerer avsevärt, och visade ännu starkare effekter på taufragment som är centrala för tanglebildning. Molekylen passerade artificiella och biologiska modeller av blod-hjärnbarriären och kunde detekteras i mössens hjärnor efter både intravenös och oral administrering. I två olika Alzheimer-liknande musmodeller ledde kort- och längre behandling till lägre nivåer av amyloidplack och lösliga amyloidformer, minskade markörer för hjärninflammation, delvis återställning av synaptiska proteiner och förbättrad prestation i minne- och inlärningsuppgifter såsom Y-labyrint och igenkänning av nytt föremål. 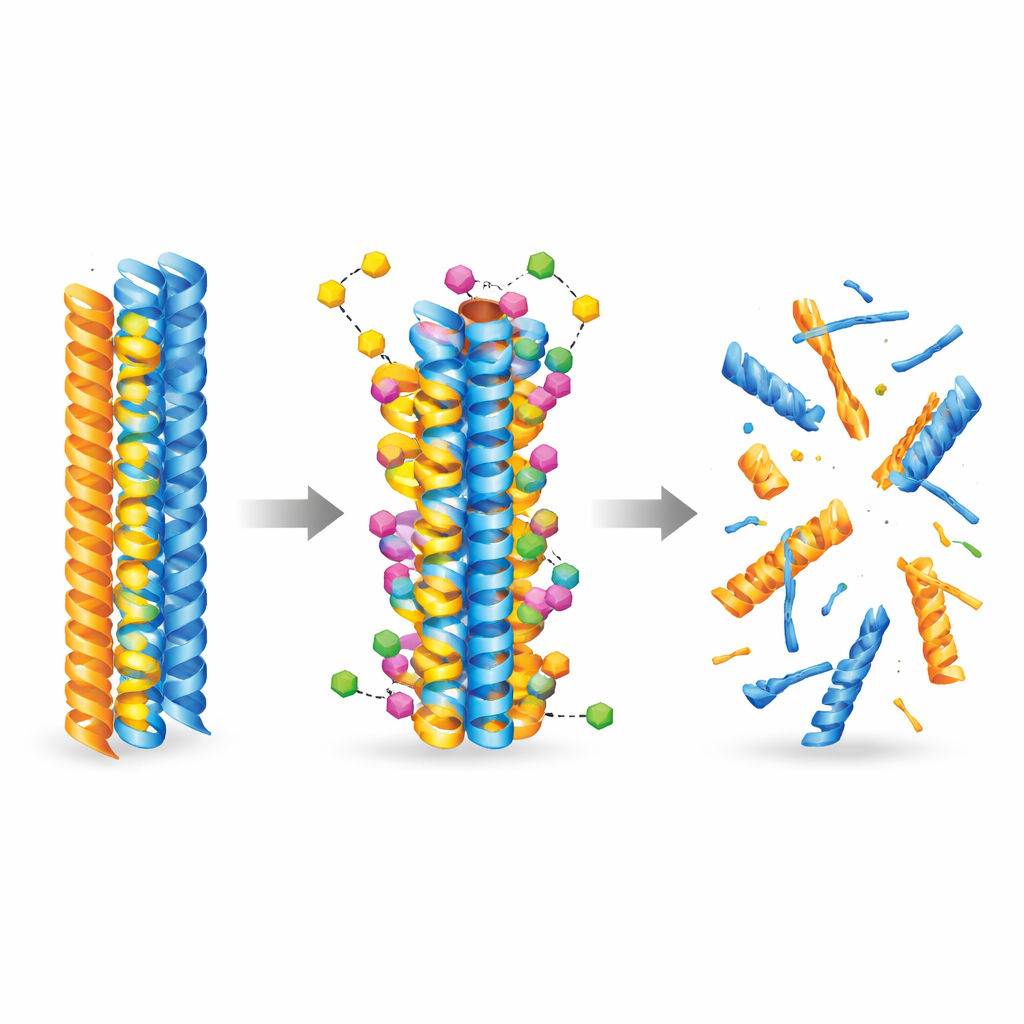
Löfte och nästa steg
Sammanfattningsvis visar studien att 3-desoxycollinoketone B är en dubbelverkande småmolekyl som kan ta sig in i hjärnan, binda starkt till både amyloid-beta- och tau-aggregat och främja deras uppbrytning, vilket leder till mätbara kognitiva fördelar hos möss. För en lekman innebär det att föreningen fungerar lite som ett molekylärt lösningsmedel för två nyckeltyper av Alzheimer-relaterade proteinklumpar, snarare än att bara maskera symtomen. Även om molekylen rensas relativt snabbt från kroppen och behöver ytterligare modifieringar för att stanna kvar längre i blodomloppet, gör dess skalbara syntes, hjärnpenetration och breda aktivitet mot felveckade proteiner den till en lovande utgångspunkt för att utveckla mer tillgängliga och kostnadseffektiva behandlingar som angriper Alzheimers sjukdom vid dess rot.
Citering: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Nyckelord: Alzheimers sjukdom, amyloid-beta, tau-protein, liten-molekylterapi, proteinaggregat