Clear Sky Science · zh
共转录折叠协调甘氨酸串联核糖开关的顺序多效应器感知
RNA 开关如何帮助细菌做出明智选择
细菌生活在不断变化的环境中,但必须实时决定开启或关闭哪些基因以节省能量并生存下去。本研究揭示了细菌 Bacillus subtilis 内一个微小 RNA “开关”如何同时监听多种分子信号——一种氨基酸、金属离子和一种蛋白辅因子——并快速决定是继续转录该基因还是将其关闭。理解这一内置决策电路不仅揭示了基因控制的基本规则,还有望为合成生物学工具和抗生素设计提供新思路。
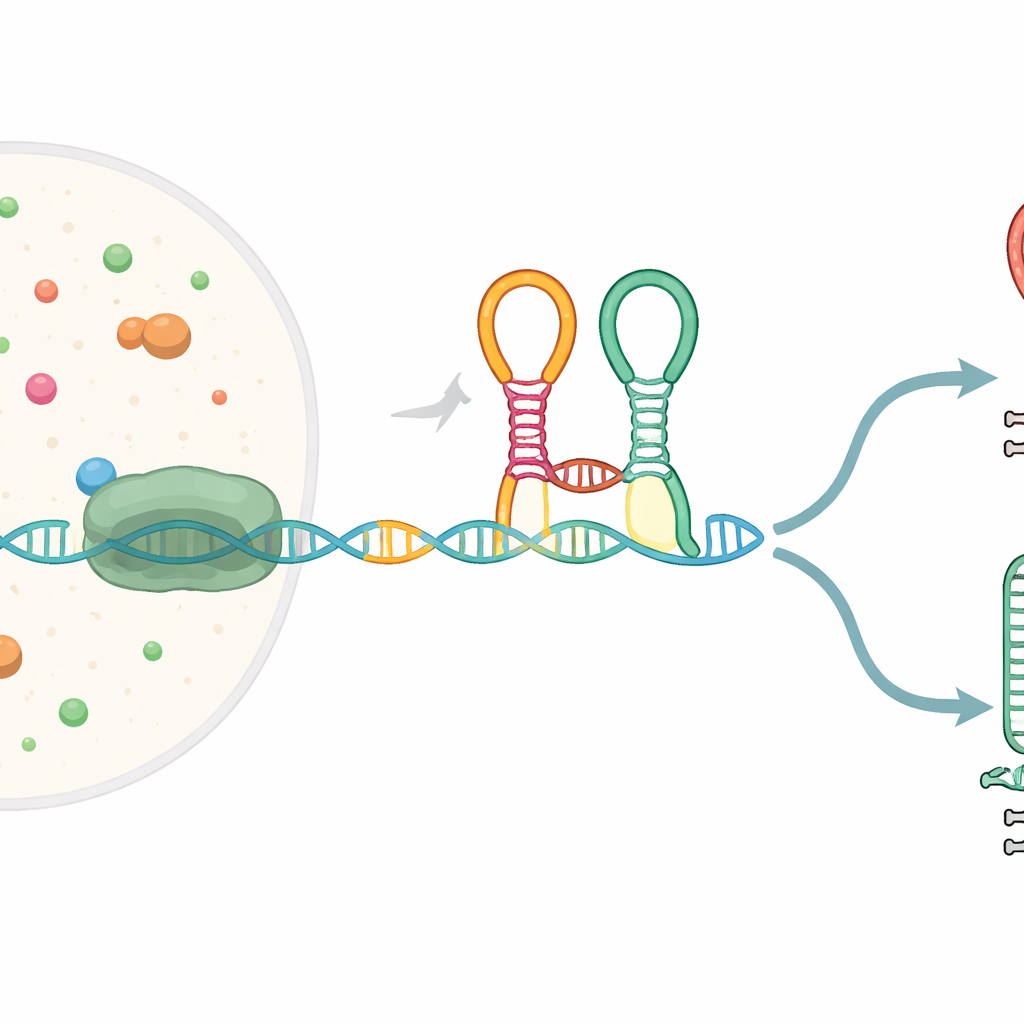
嵌入在基因信息中的微小传感器
许多细菌基因以称为核糖开关的特殊 RNA 片段开始,这些片段折叠成能感知小分子的构象,并据此改变基因表达。本研究中的核糖开关称为甘氨酸串联核糖开关,位于帮助分解氨基酸甘氨酸的基因上游。它包含两个相邻的感应模块(“适配体”),两者都能识别甘氨酸,并由一个称为折弯转角(kink-turn)的急弯相连。在 RNA 聚合酶将 DNA 复制为 RNA 的过程中,该核糖开关在合成时折叠,并能引导转录过程走向生成完整转录本或在内置终止信号处提前终止。
创建决策检查点的停顿
作者发现,复制 RNA 的酶并不会在该区域平滑移动;相反,它在核糖开关内的三个特定位点发生停顿。这些停顿像交通信号灯一样,为新生 RNA 提供折叠并与周围分子相互作用的时间。在第一个停顿处,上游的适配体形成并准备结合甘氨酸。在随后的停顿处,第二个适配体的部分结构和最终决定用的螺旋段逐步出现。一种名为 NusA 的辅助蛋白延长了其中两个停顿,尤其是在甘氨酸存在时,从而有效地扩大了核糖开关感知环境并决定继续转录或终止转录的时间窗口。
离子、甘氨酸与蛋白伙伴的逐步感知
通过单分子荧光显微镜和高通量化学探针实验,研究团队表明核糖开关并非一次性动作。首先,钾离子稳定了 RNA 底部的折弯转角,使第一个适配体朝向延伸的转录链方向定位。随后,甘氨酸结合到第一个适配体,收紧其局部结构。这些事件促进了两个适配体之间的远程接触,在第二个甘氨酸到来之前就预先排列好了两个甘氨酸结合位点。在靠近内置终止发夹的最后一个停顿处,第二个甘氨酸可以在这个预组织的环境中结合到下游适配体,且 NusA 增强的停顿进一步有利于形成这一紧凑且具活性的构象。
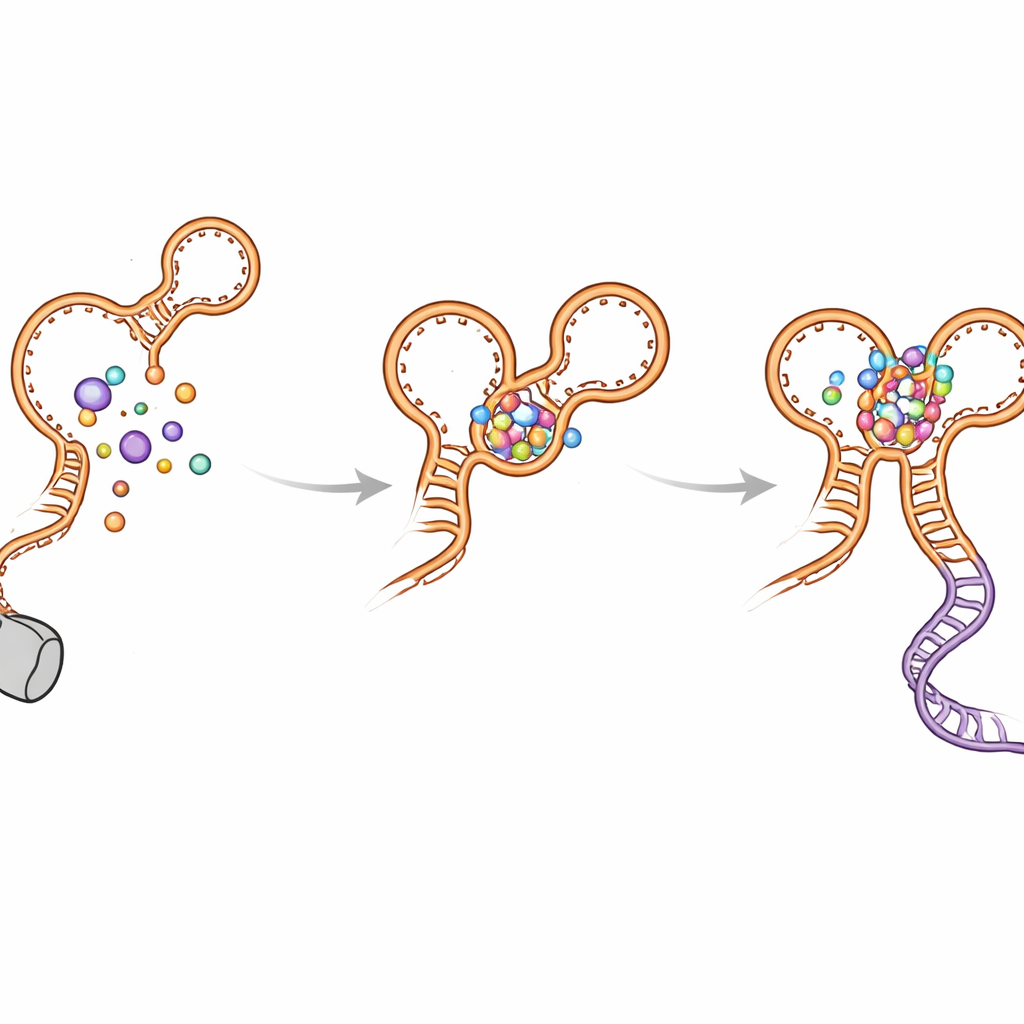
折叠的岔路与开关如何避免被卡住
作者还发现了若干在 RNA 延伸过程中暂时形成的“误入歧途”发夹。这些非本征结构出现在两个适配体中,可能延迟最终活性构象的形成。折弯转角螺旋(称为 P0)和适配体间接触有助于化解这些中间体并引导折叠走向功能性布局。当 P0 或关键接触点被突变破坏时,核糖开关的灵敏度和效率严重下降:甘氨酸仍能结合,但远程对接减弱、决定用的螺旋不够稳定,转录读通率下降。计算机模拟支持这些观察,显示当 P0 和两个甘氨酸位点完整时,核糖开关更加紧凑且稳定。
活细胞中的非平衡逻辑门
综述来看,这些结果支持这样一种图景:甘氨酸串联核糖开关表现为一种动力学逻辑门,而非简单的平衡传感器。与其让两个甘氨酸同时结合到预先形成的结构,不如说结合与折叠以精确的 5′→3′ 顺序发生,由转录停顿门控,并受钾离子与 NusA 蛋白塑形。这种逐步、远离平衡的过程让细菌在决定是否完全表达下游甘氨酸分解基因之前,整合多种信号——细胞内离子平衡、甘氨酸水平和转录速率。这项工作提示,类似的动力学驱动协同作用可能是一类通用策略,RNA 开关通过它们协调多种细胞因子以精细调控基因表达。
引用: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
关键词: 核糖开关, 甘氨酸感应, RNA 折叠, 转录停顿, 细菌基因调控