Clear Sky Science · de
Ko-transkriptionelles Falten steuert sequenzielles Multi-Effektor-Erkennen durch einen Glycin-Tandem-Riboschalter
Wie RNA-Schalter Bakterien bei klugen Entscheidungen helfen
Bakterien leben in ständig wechselnden Umgebungen und müssen dennoch in Echtzeit entscheiden, welche Gene sie ein- oder ausschalten, um Energie zu sparen und zu überleben. Diese Studie zeigt, wie ein winziger RNA‑„Schalter“ in Bacillus subtilis gleichzeitig mehrere molekulare Signale abhört — eine Aminosäure, Metallionen und einen Protein‑Cofaktor — und dann schnell entscheidet, ob das Ablesen eines Gens fortgesetzt oder abgebrochen wird. Das Verständnis dieses eingebauten Entscheidungsmechanismus offenbart nicht nur grundlegende Regeln der Genkontrolle, sondern könnte auch neue Werkzeuge für die synthetische Biologie und die Entwicklung von Antibiotika inspirieren.
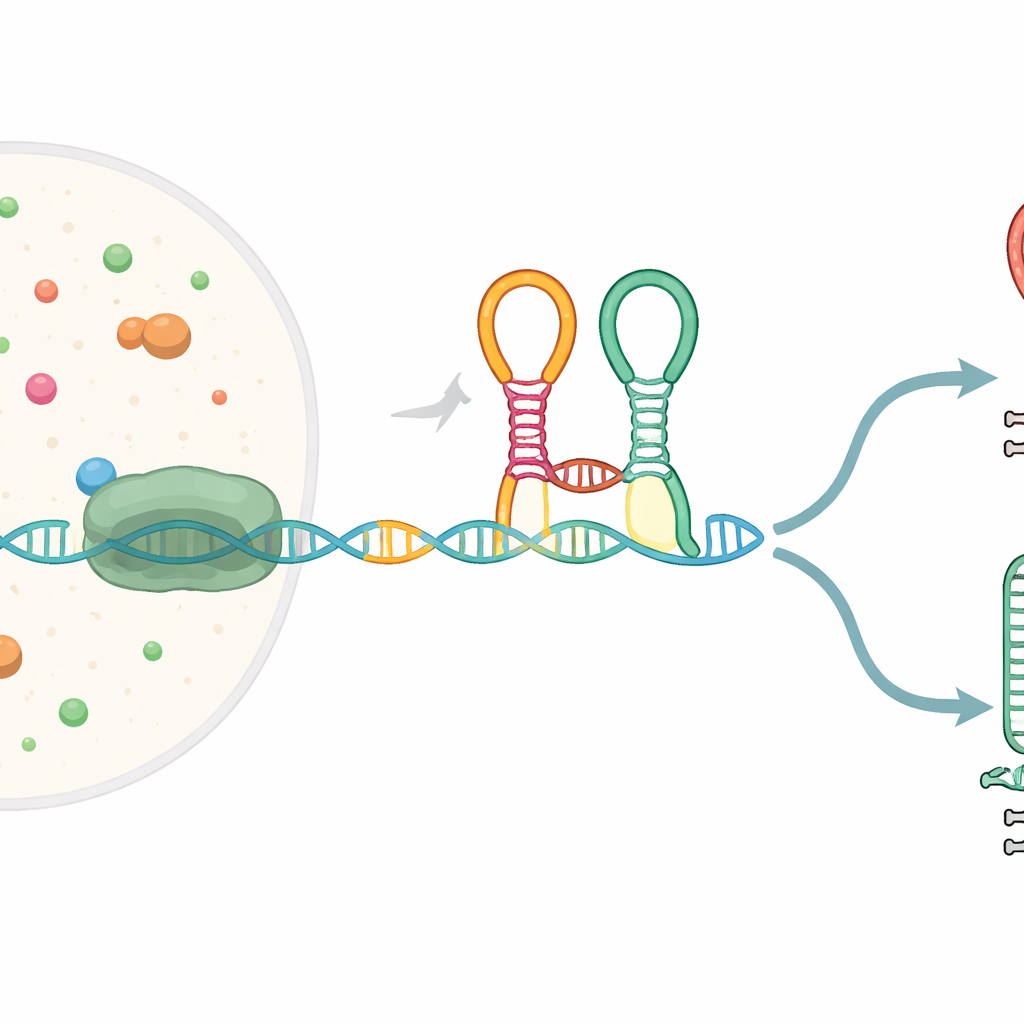
Ein winziger Sensor im Genmessage
Viele bakterielle Gene beginnen mit speziellen RNA‑Abschnitten, den sogenannten Riboschaltern, die in Formen falten, welche kleine Moleküle erkennen und daraufhin die Genexpression ändern. Der hier untersuchte Riboschalter, bekannt als Glycin‑Tandem‑Riboschalter, sitzt vor Genen, die am Abbau der Aminosäure Glycin beteiligt sind. Er enthält zwei nebeneinanderliegende Sensor‑Module („Aptamere“), die beide Glycin erkennen und durch eine scharfe Biegung, einen sogenannten Kink‑Turn, verbunden sind. Während die RNA‑Nachricht von der DNA durch die RNA‑Polymerase kopiert wird, faltet sich dieser Riboschalter „on the fly“ und kann den Prozess entweder zum vollständigen Transkriptieren oder zum vorzeitigen Abbruch an einem eingebauten Stoppsignal lenken.
Pausen, die Entscheidungs‑Checkpoint schaffen
Die Autoren fanden heraus, dass das RNA‑kopierende Enzym diese Region nicht gleichmäßig durchläuft; stattdessen pausiert es an drei spezifischen Stellen innerhalb des Riboschalters. Diese Pausen wirken wie Ampeln, die der entstehenden RNA Zeit geben, sich zu falten und mit umliegenden Molekülen zu interagieren. Bei der ersten Pause bildet sich das upstream Aptamer und wird bereit, Glycin zu binden. Bei späteren Pausen treten Teile des zweiten Aptamers und die finale Entscheidungshelix zutage. Ein Hilfsprotein namens NusA verlängert zwei dieser Pausen, besonders wenn Glycin vorhanden ist, und erweitert damit effektiv das Zeitfenster, in dem der Riboschalter seine Umgebung abtasten und sich für Fortsetzung oder Abbruch der Transkription entscheiden kann.
Schrittweises Erkennen von Ionen, Glycin und einem Proteinpartner
Mithilfe von Einzelmolekül‑Fluoreszenzmikroskopie und hochdurchsatzfähiger chemischer Prägung zeigte das Team, dass der Riboschalter nicht in einem einzigen Schnappvorgang arbeitet. Zuerst stabilisieren Kaliumionen den Kink‑Turn an der Basis der RNA und richten das erste Aptamer in Richtung des wachsenden Transkripts aus. Anschließend bindet Glycin an dieses erste Aptamer und verfestigt dessen lokale Struktur. Diese Ereignisse fördern langreichweitige Kontakte zwischen den beiden Aptameren, die beide Glycin‑Bindetaschen bereits vor der Ankunft des zweiten Glycins vorarrangieren. An der letzten Pause nahe der eingebauten Terminator‑Haarnadel kann in dieser vororganisierten Umgebung ein zweites Glycin an das downstream Aptamer binden, und die durch NusA verstärkte Pause begünstigt zusätzlich die Vollendung dieser kompakten, aktiven Konfiguration.
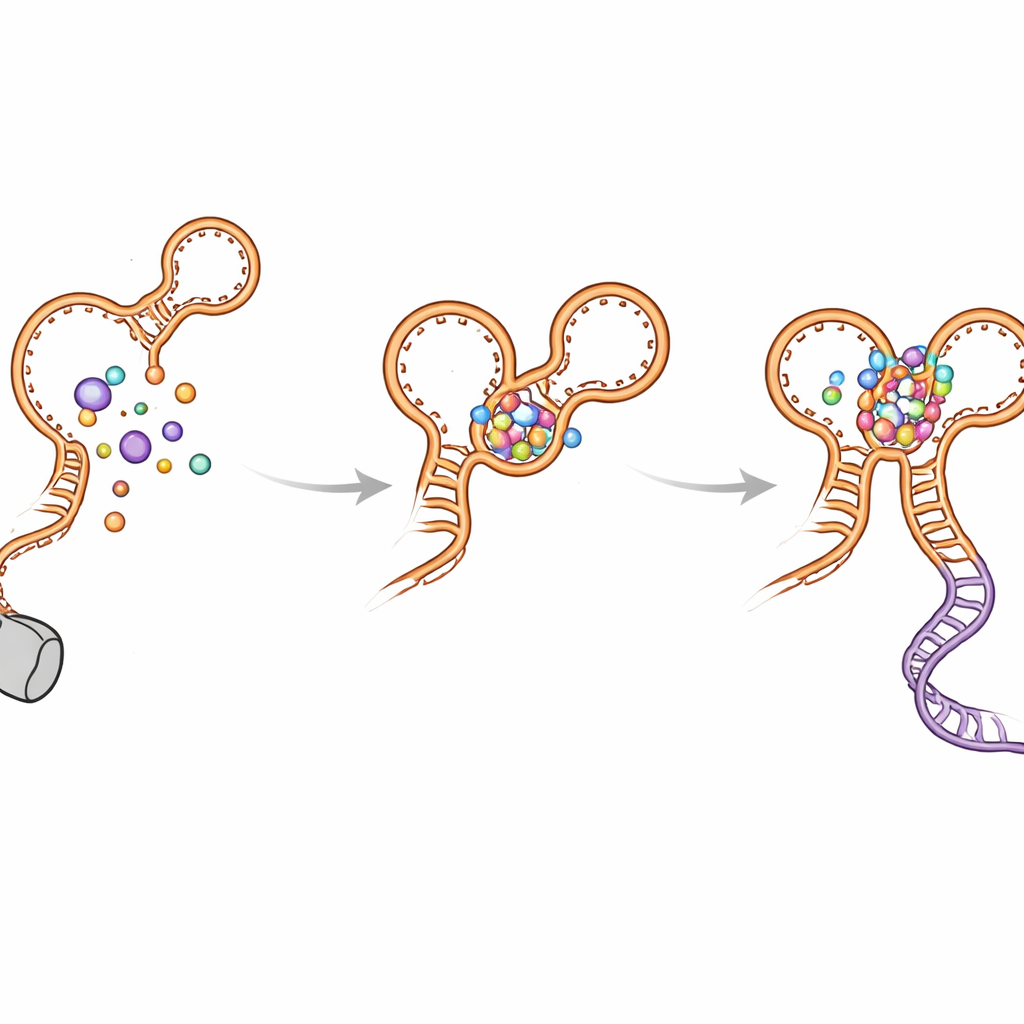
Falt‑Umwege und wie der Schalter verhindert, stecken zu bleiben
Die Autoren entdeckten außerdem mehrere vorübergehend gebildete „falsche Abzweigungen“ in Form von Haarnadeln, die beim Wachsen der RNA auftreten. Diese nicht‑nativen Strukturen erscheinen in beiden Aptameren und können die Ausbildung der finalen, aktiven Gestalt verzögern. Die Kink‑Turn‑Helix (genannt P0) und die inter‑Aptamer‑Kontakte helfen, diese Zwischenzustände aufzulösen und das Falten in Richtung der funktionalen Anordnung zu lenken. Werden P0 oder wichtige Kontaktstellen durch Mutationen gestört, verliert der Riboschalter einen großen Teil seiner Empfindlichkeit und Effizienz: Glycin bindet zwar noch, aber das langreichweitige Andocken wird geschwächt, die Entscheidungshelix ist weniger stabil und die Transkriptionsdurchlese nimmt ab. Computersimulationen stützten diese Beobachtungen und zeigten, dass der Riboschalter deutlich kompakter und stabiler ist, wenn P0 und beide Glycin‑Stellen intakt sind.
Ein Nicht‑Gleichgewichts‑Logikgatter in lebenden Zellen
In der Summe unterstützen die Ergebnisse das Bild, dass der Glycin‑Tandem‑Riboschalter eher als kinetisches Logikgatter denn als einfacher Gleichgewichtssensor fungiert. Anstatt dass beide Glycinmoleküle gleichzeitig an eine vorgeformte Struktur binden, verlaufen Bindung und Faltung in einer präzisen 5′‑zu‑3′‑Abfolge, gesteuert durch Transkriptionspausen und geformt von Kaliumionen sowie dem NusA‑Protein. Dieser schrittweise, aus dem Gleichgewicht arbeitende Prozess erlaubt es dem Bakterium, mehrere Signale — das zelluläre Ionengleichgewicht, Glycinspiegel und Transkriptionsgeschwindigkeit — zu integrieren, bevor es entscheidet, ob die downstream liegenden Glycin‑abbauenden Gene vollständig exprimiert werden. Die Arbeit legt nahe, dass eine derartig kinetisch getriebene Kooperation eine allgemeine Strategie sein könnte, mit der RNA‑Schalter mehrere zelluläre Faktoren koordinieren, um die Genexpression fein abzustimmen.
Zitation: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Schlüsselwörter: Riboschalter, Glycin-Erkennung, RNA-Faltung, Transkriptionspausen, bakterielle Genregulation