Clear Sky Science · es
El plegamiento cotranscripcional orquesta la detección secuencial por múltiples efectores en un riboswitch tándem de glicina
Cómo los interruptores de ARN ayudan a las bacterias a tomar decisiones inteligentes
Las bacterias viven en entornos en constante cambio y, sin embargo, deben decidir en tiempo real qué genes activar o silenciar para ahorrar energía y sobrevivir. Este estudio revela cómo un pequeño “interruptor” de ARN dentro de la bacteria Bacillus subtilis escucha varias señales moleculares a la vez—un aminoácido, iones metálicos y un cofactor proteico—y luego elige rápidamente si continuar la lectura de un gen o detenerla. Entender este circuito de decisión incorporado no solo desvela reglas fundamentales del control génico, sino que también podría inspirar nuevas herramientas para la biología sintética y el diseño de antibióticos.
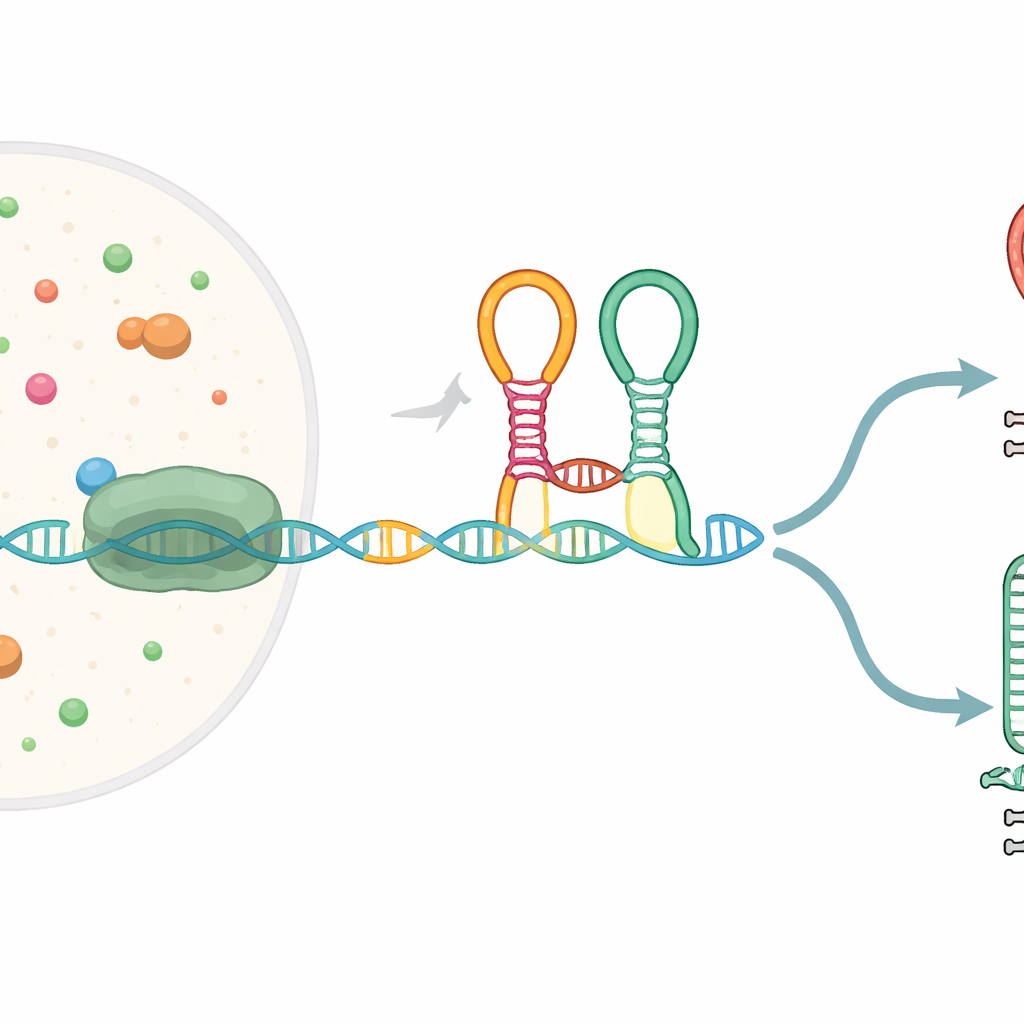
Un sensor diminuto integrado en el mensaje génico
Muchos genes bacterianos comienzan con segmentos especiales de ARN llamados riboswitches, que se pliegan en conformaciones capaces de detectar pequeñas moléculas y, en respuesta, modificar la expresión génica. El riboswitch estudiado aquí, conocido como riboswitch tándem de glicina, se sitúa delante de genes implicados en la degradación del aminoácido glicina. Contiene dos módulos sensores adyacentes (“aptámeros”) que reconocen glicina y están unidos por una quiebra pronunciada llamada kink-turn. A medida que el mensaje de ARN se copia desde el ADN por la ARN polimerasa, este riboswitch se pliega sobre la marcha y puede dirigir el proceso hacia completar la transcripción de longitud completa o acortarla en una señal de paro incorporada.
Pausas que crean puntos de control para la decisión
Los autores observaron que la enzima que copia el ARN no avanza de forma continua por esta región; en su lugar, se detiene en tres puntos específicos dentro del riboswitch. Estas pausas actúan como semáforos, dando tiempo al ARN emergente para plegarse e interactuar con las moléculas circundantes. En la primera pausa, el aptámero upstream se forma y queda listo para unir glicina. En pausas posteriores, emergen partes del segundo aptámero y la hélice de decisión final. Una proteína auxiliar llamada NusA alarga dos de estas pausas, especialmente cuando hay glicina presente, ampliando efectivamente la ventana temporal durante la cual el riboswitch puede sondear su entorno y decidir entre continuar la transcripción o terminarla.
Detección escalonada de iones, glicina y una proteína compañera
Usando microscopía de fluorescencia de molécula única y sondeo químico de alto rendimiento, el equipo mostró que el riboswitch no actúa en un solo instante. Primero, los iones potasio estabilizan el kink-turn en la base del ARN, orientando el primer aptámero hacia la ruta del transcript growing (creciente). Luego la glicina se une a este primer aptámero, apretando su estructura local. Estos eventos fomentan contactos de largo alcance entre los dos aptámeros, que preorganizan ambos sitios de unión a glicina incluso antes de que llegue la segunda glicina. En la pausa final cerca del horquillado terminador incorporado, una segunda glicina puede unirse al aptámero aguas abajo en este entorno preorganizado, y la prolongación de la pausa mediada por NusA favorece aún más la finalización de esta configuración compacta y activa.
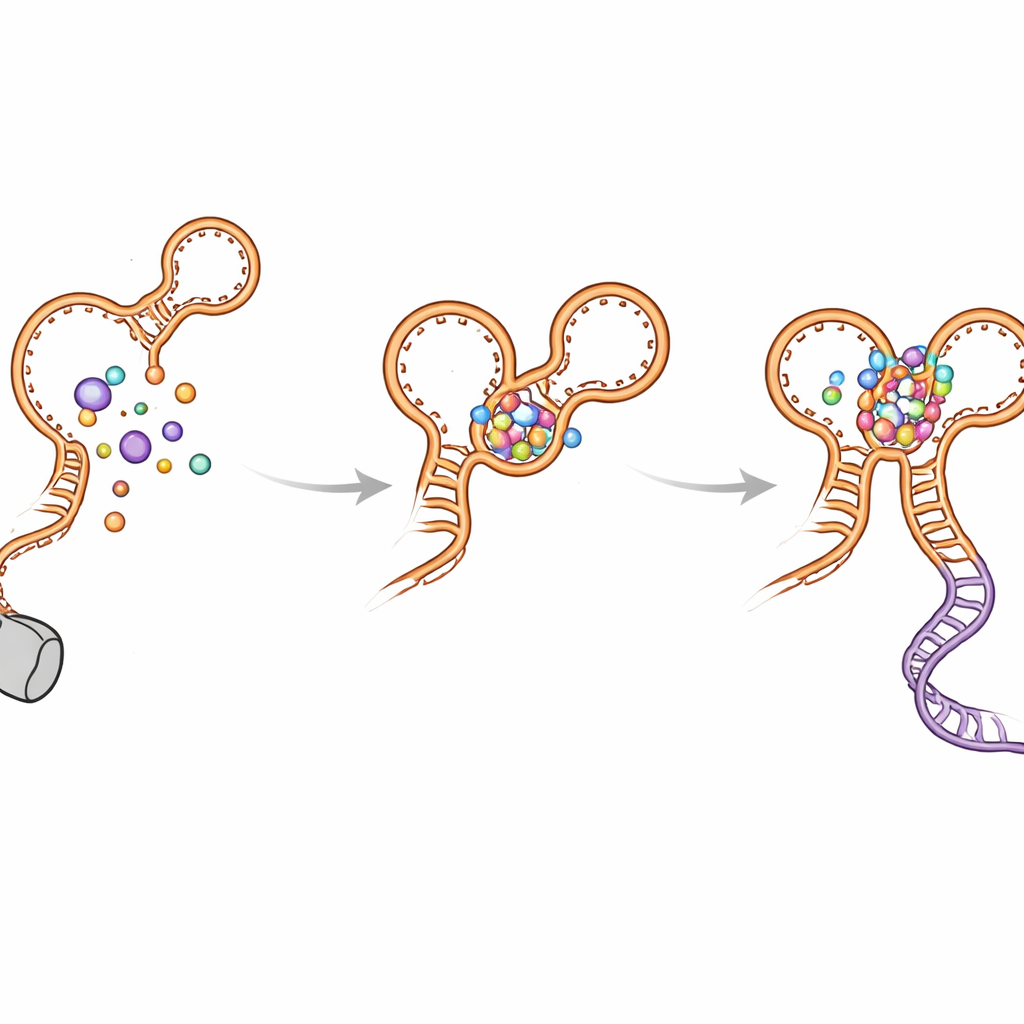
Desvíos de plegamiento y cómo el interruptor evita atascarse
Los autores también descubrieron varios horquillas de “giro equivocado” que se forman temporalmente a medida que el ARN crece. Estas estructuras no nativas aparecen en ambos aptámeros y pueden retrasar la formación de la conformación final y activa. La hélice kink-turn (denominada P0) y los contactos entre aptámeros ayudan a resolver estos intermedios y dirigir el plegamiento hacia la disposición funcional. Cuando P0 o puntos de contacto clave se alteran por mutaciones, el riboswitch pierde gran parte de su sensibilidad y eficiencia: la glicina aún se une, pero el acoplamiento de largo alcance se debilita, la hélice de decisión es menos estable y la lectura por transcripción disminuye. Las simulaciones por ordenador respaldaron estas observaciones, mostrando que el riboswitch es mucho más compacto y estable cuando P0 y ambos sitios de glicina están intactos.
Una compuerta lógica fuera de equilibrio en células vivas
En conjunto, los resultados apoyan la imagen de que el riboswitch tándem de glicina se comporta como una compuerta lógica cinética más que como un simple sensor en equilibrio. En lugar de que ambas moléculas de glicina se unan simultáneamente a una estructura preformada, la unión y el plegamiento ocurren en una secuencia precisa 5′ a 3′, regulada por pausas en la transcripción y moldeada por iones potasio y la proteína NusA. Este proceso escalonado y fuera del equilibrio permite a la bacteria integrar diversas señales—el balance iónico celular, los niveles de glicina y la velocidad de transcripción—antes de decidir si expresa por completo los genes dedicados a la degradación de glicina. El trabajo sugiere que tal cooperatividad impulsada cinéticamente puede ser una estrategia general mediante la cual los interruptores de ARN coordinan múltiples factores celulares para ajustar finamente la expresión génica.
Cita: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Palabras clave: riboswitch, detección de glicina, plegamiento de ARN, pausas en la transcripción, regulación génica bacteriana