Clear Sky Science · it
Il ripiegamento co-trascrizionale orchestra il rilevamento sequenziale multi-effettore da parte di un riboswitch tandem per la glicina
Come gli interruttori di RNA aiutano i batteri a fare scelte intelligenti
I batteri vivono in ambienti in continuo mutamento e devono decidere in tempo reale quali geni attivare o disattivare per risparmiare energia e sopravvivere. Questo studio svela come un piccolo “interruttore” di RNA all’interno di Bacillus subtilis ascolti contemporaneamente più segnali molecolari — un amminoacido, ioni metallici e un cofattore proteico — e poi scelga rapidamente se proseguire la lettura di un gene oppure interromperla. Comprendere questo circuito decisionale incorporato non solo rivela regole fondamentali del controllo genico, ma potrebbe anche ispirare nuovi strumenti per la biologia sintetica e la progettazione di antibiotici.
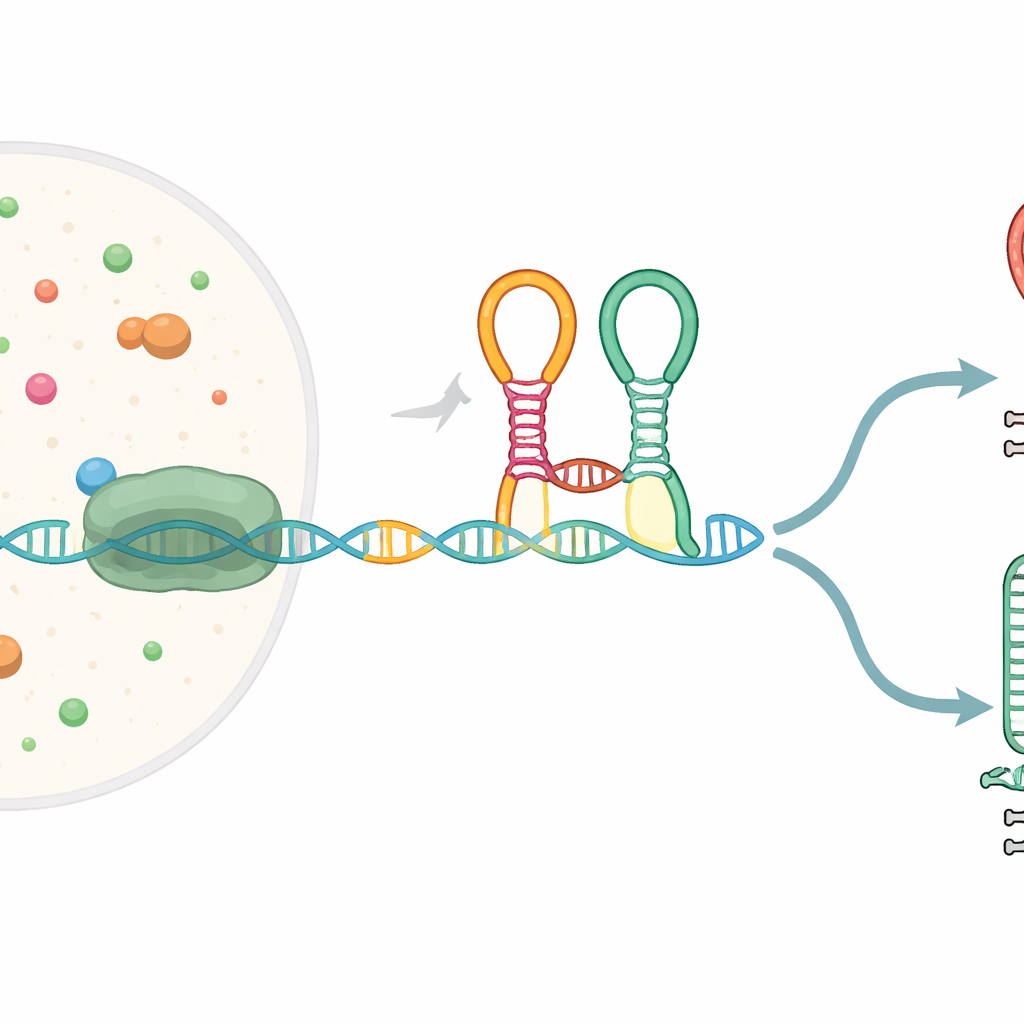
Un sensore minuscolo incorporato nel messaggio genico
Molti geni batterici iniziano con segmenti speciali di RNA detti riboswitch, che si ripiegano in conformazioni capaci di riconoscere piccole molecole e, in risposta, modificare l’espressione genica. Il riboswitch studiato qui, noto come riboswitch tandem per la glicina, si trova davanti a geni che aiutano a degradare l’amminoacido glicina. Contiene due moduli di riconoscimento adiacenti (“aptamer”) che riconoscono entrambi la glicina e sono collegati da una curva netta chiamata kink-turn. Mentre il messaggio di RNA viene copiato dal DNA dall’RNA polimerasi, questo riboswitch si ripiega al volo e può indirizzare il processo o verso il completamento della trascrizione a lunghezza intera o verso l’interruzione prematura in corrispondenza di un segnale di terminazione incorporato.
Pause che creano punti di controllo per la decisione
Gli autori hanno osservato che l’enzima che copia l’RNA non scorre in modo uniforme attraverso questa regione; invece, si ferma in tre punti specifici all’interno del riboswitch. Queste pause funzionano come semafori, dando all’RNA nascente il tempo di ripiegarsi e interagire con le molecole circostanti. Alla prima pausa si forma l’aptamer anteriore e diventa pronto a legare la glicina. Alle pause successive emergono parti del secondo aptamer e l’elica finale che determina la decisione. Una proteina ausiliaria chiamata NusA prolunga due di queste pause, soprattutto quando la glicina è presente, ampliando di fatto la finestra temporale durante la quale il riboswitch può sondare l’ambiente e impegnarsi a proseguire la trascrizione o a terminarla.
Rilevamento graduale di ioni, glicina e di un partner proteico
Usando microscopia a singola molecola con fluorescenza e mappature chimiche ad alta produttività, il gruppo ha mostrato che il riboswitch non agisce in un unico istante. Innanzitutto, gli ioni potassio stabilizzano il kink-turn alla base dell’RNA, orientando il primo aptamer lungo il percorso del trascritto in crescita. La glicina si lega quindi a questo primo aptamer, consolidandone la struttura locale. Questi eventi favoriscono contatti a lunga distanza tra i due aptamer, che predispongono entrambe le tasche di legame per la glicina prima ancora che arrivi la seconda molecola. Alla pausa finale, vicino all’hairpin terminatore incorporato, una seconda glicina può legarsi all’aptamer a valle in questo contesto pre-organizzato, e la pausa prolungata da NusA favorisce ulteriormente il completamento di questa configurazione compatta e attiva.
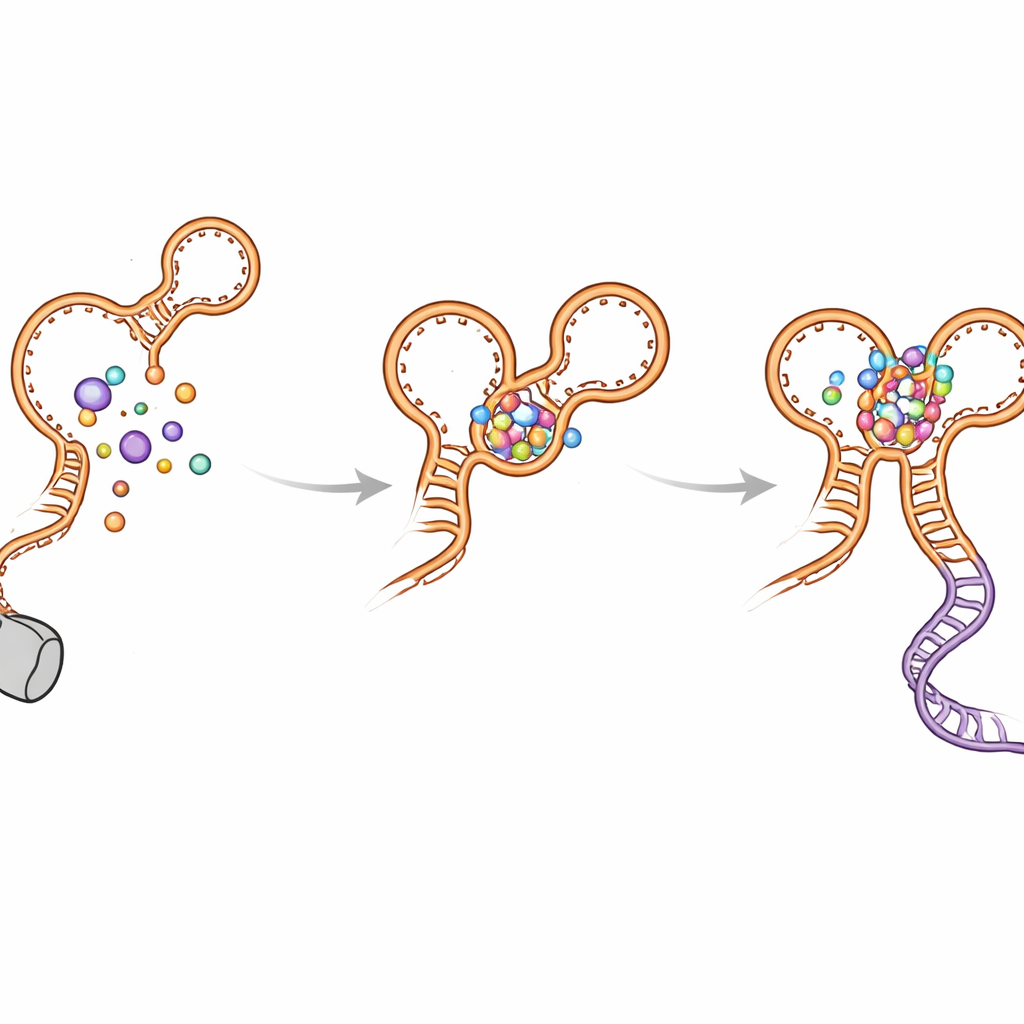
Deviazioni nel ripiegamento e come lo switch evita di bloccarsi
Gli autori hanno anche scoperto diversi hairpin «a svolta sbagliata» che si formano temporaneamente mentre l’RNA cresce. Queste strutture non native compaiono in entrambi gli aptamer e possono ritardare la formazione della forma finale e attiva. L’elica kink-turn (chiamata P0) e i contatti inter-aptamer aiutano a risolvere questi intermedi e indirizzare il ripiegamento verso la disposizione funzionale. Quando P0 o punti di contatto chiave vengono perturbati da mutazioni, il riboswitch perde gran parte della sua sensibilità ed efficienza: la glicina continua a legarsi, ma l’assemblaggio a lunga distanza si indebolisce, l’elica decisionale è meno stabile e la lettura in lettura (readthrough) della trascrizione diminuisce. Simulazioni al computer hanno supportato queste osservazioni, mostrando che il riboswitch è molto più compatto e stabile quando P0 e entrambi i siti per la glicina sono intatti.
Una porta logica fuori equilibrio nelle cellule viventi
Nel loro insieme, i risultati sostengono il quadro in cui il riboswitch tandem per la glicina si comporta come una porta logica cinetica piuttosto che come un semplice sensore all’equilibrio. Invece di entrambi i residui di glicina che si legano simultaneamente a una struttura preformata, legame e ripiegamento avvengono in una sequenza precisa 5′-3′, regolata dalle pause di trascrizione e plasmata dagli ioni potassio e dalla proteina NusA. Questo processo graduale e fuori equilibrio consente al batterio di integrare diversi segnali — bilancio ionico cellulare, livelli di glicina e velocità di trascrizione — prima di decidere se esprimere completamente i geni a valle responsabili della degradazione della glicina. Il lavoro suggerisce che tale cooperatività guidata cineticamente potrebbe essere una strategia generale con cui gli switch di RNA coordinano più fattori cellulari per calibrare finemente l’espressione genica.
Citazione: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Parole chiave: riboswitch, rilevamento della glicina, ripiegamento dell'RNA, pausa nella trascrizione, regolazione genica batterica