Clear Sky Science · sv
Ko-transkriptionell vikning orkestrerar sekventiell multi-effektoravkänning av en glycin-tandem-riboswitch
Hur RNA-växlar hjälper bakterier att fatta smarta val
Bakterier lever i ständigt föränderliga miljöer, men måste ändå i realtid avgöra vilka gener som ska slås på eller av för att spara energi och överleva. Denna studie avslöjar hur en liten RNA-”brytare” inne i bakterien Bacillus subtilis lyssnar på flera molekylära signaler samtidigt — en aminosyra, joner och en protein kofaktor — och sedan snabbt väljer om transkriptionen ska fortsätta eller avbrytas. Att förstå denna inbyggda beslutscircuit blottlägger inte bara grundläggande principer för genreglering, utan kan också inspirera nya verktyg för syntetisk biologi och antibiotikadesign.
En liten sensor inbyggd i genmeddelandet
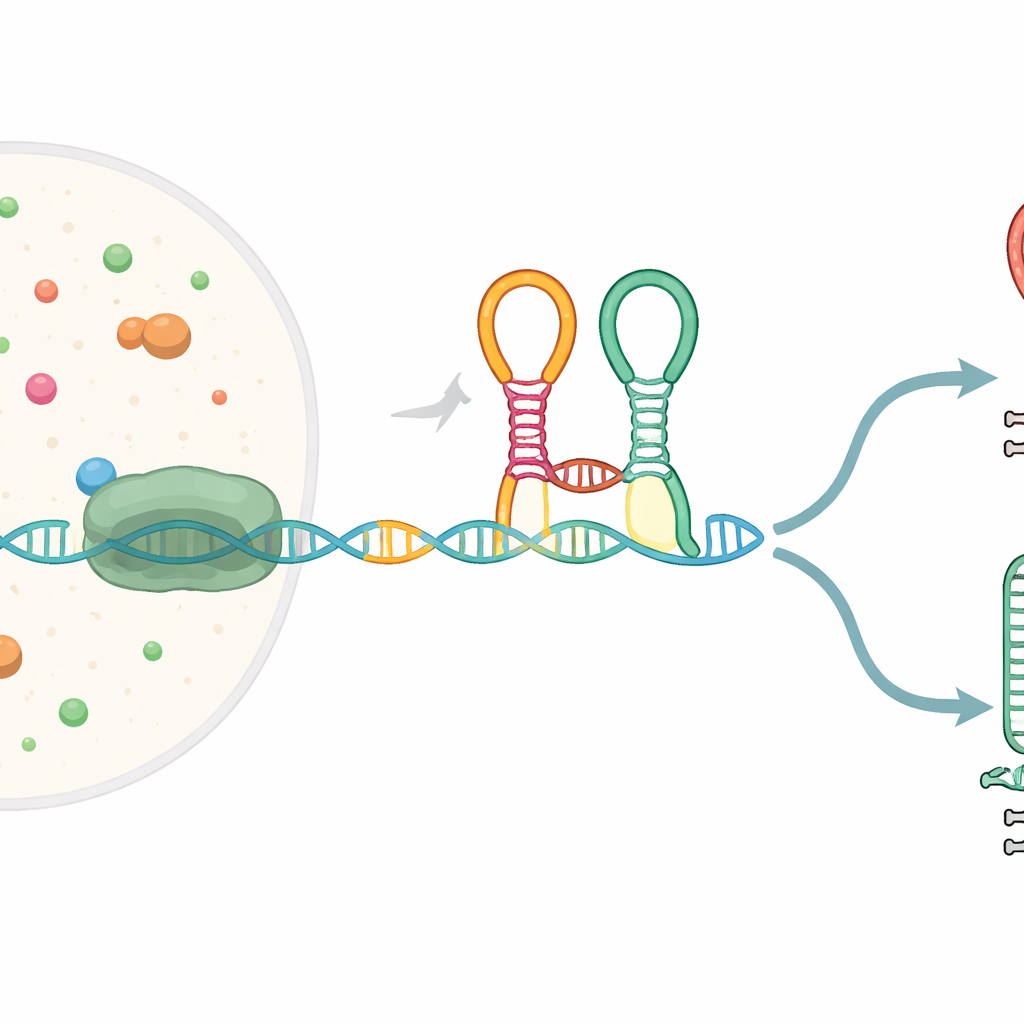
Många bakteriella gener inleds med speciella RNA-segment kallade riboswitchar, vilka viks till former som kan känna av små molekyler och som till följd ändrar genuttrycket. Den riboswitch som undersöks här, känd som glycin-tandem-riboswitchen, sitter framför gener som hjälper till att bryta ner aminosyran glycin. Den innehåller två intilliggande sensoriska moduler (”aptamrar”) som båda känner igen glycin och som är förenade av en skarp böj kallad kink-turn. När RNA-meddelandet kopieras från DNA av RNA-polymeras viks denna riboswitch i realtid och kan styra processen mot antingen en fullängds-transkript eller ett förkortat transkript vid en inbyggd stopp-signal.
Pauser som skapar beslutspunkter
Författarna fann att RNA-kopierande enzym inte rör sig jämnt genom detta område; istället pausar det vid tre specifika ställen inom riboswitchen. Dessa pauser fungerar som trafikljus och ger det framväxande RNA:t tid att vikas och interagera med omgivande molekyler. Vid den första pausen formas den uppströms aptamern och blir redo att binda glycin. Vid senare pauser framträder delar av den andra aptamern och den slutgiltiga beslutsspiralens delar. Ett hjälpprotein kallat NusA förlänger två av dessa pauser, särskilt när glycin finns närvarande, vilket i praktiken vidgar tidsfönstret under vilket riboswitchen kan avkänna sin omgivning och bestämma sig för att antingen fortsätta transkriptionen eller terminera den.
Stegvis avkänning av joner, glycin och en proteinpartner
Genom att använda enkelmolekyl-fluorescensmikroskopi och höggenomströmmande kemisk kartläggning visade teamet att riboswitchen inte agerar i ett enda ögonblick. Först stabiliserar kaliumjoner kink-turn vid RNA:ts bas och orienterar den första aptamern i riktning mot den växande transkriptets bana. Glycin binder därefter till den första aptamern och förtätar dess lokala struktur. Dessa händelser uppmuntrar långdistanskontakter mellan de två aptamrarna, vilket förordnar båda glycin-bindande fickorna redan innan det andra glycinet ankommer. Vid den slutliga pausen nära den inbyggda terminerings-hårnålen kan ett andra glycin binda till den nedströms aptamern i denna förorganiserade miljö, och NusA-förlängd pausning främjar ytterligare fullbordandet av denna kompakta, aktiva konfiguration.
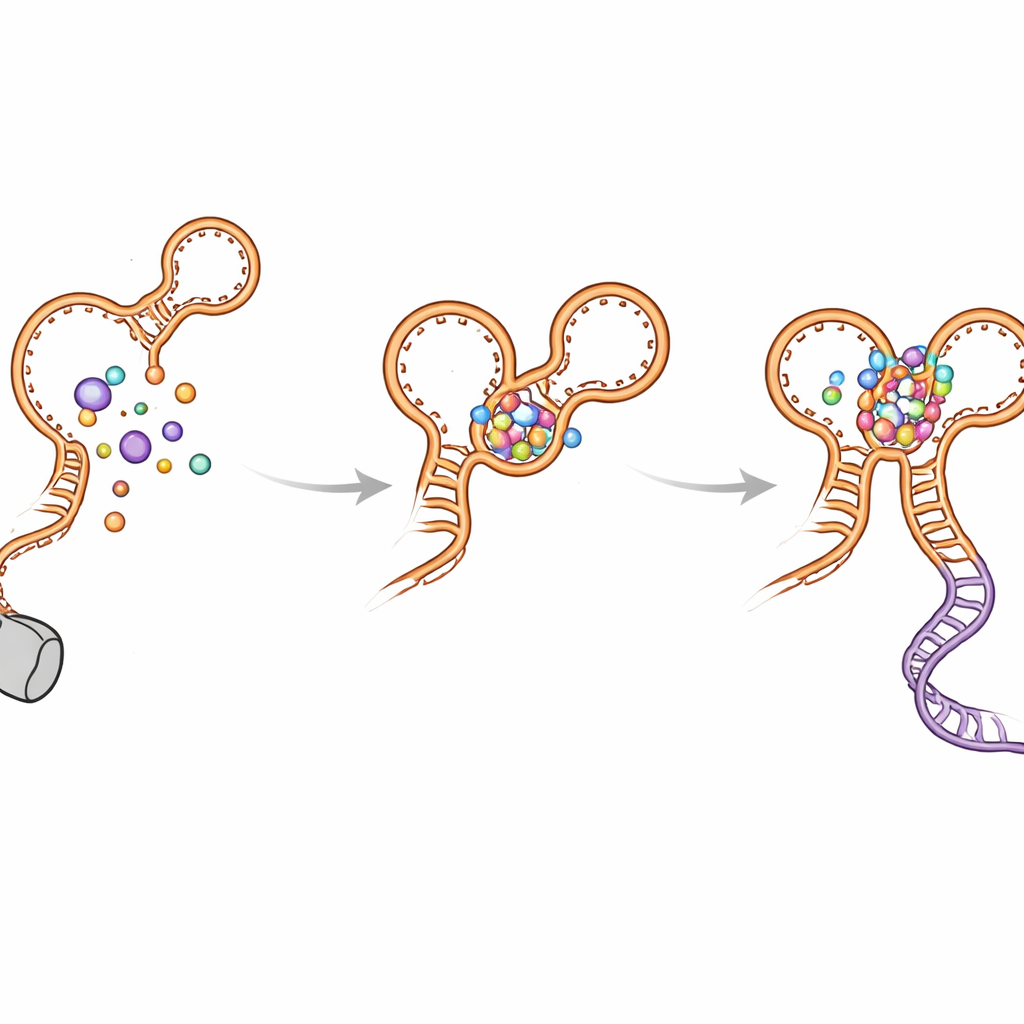
Vikningsavvikelser och hur brytaren undviker att fastna
Författarna upptäckte också flera ”felvändnings”–hårnålar som bildas tillfälligt när RNA:t växer. Dessa icke-native strukturer uppträder i båda aptamrarna och kan fördröja bildandet av den slutliga, aktiva formen. Kink-turn-helixen (kallad P0) och inter-aptamerkontakterna hjälper till att lösa upp dessa intermediärer och styra vikningen mot det funktionella utfallet. När P0 eller nyckelkontaktpunkter störs av mutationer förlorar riboswitchen mycket av sin känslighet och effektivitet: glycin binder fortfarande, men långdistansdokningen försvagas, beslutsspiralens stabilitet minskar och transkriptionsgenomläsningen sjunker. Datorsimuleringar stödde dessa observationer och visade att riboswitchen är mycket mer kompakt och stabil när P0 och båda glycin-siterna är intakta.
En icke-jämvikts-logikport i levande celler
Sammantaget stöder resultaten en bild där glycin-tandem-riboswitchen beter sig som en kinetisk logikport snarare än en enkel jämviktsbaserad sensor. Istället för att båda glycinmolekylerna binder samtidigt till en redan färdigstruktur, sker bindning och vikning i en preciserad 5′-till-3′-sekvens, grindad av transkriptionspauser och formad av kaliumjoner och proteinet NusA. Denna stegvisa, utanför-jämvikt-process låter bakterien integrera flera signaler — cellens jonbalans, glycinhalter och transkriptionshastighet — innan den bestämmer om de nedströms glycin-nedbrytande generna ska uttryckas fullt ut. Arbetet tyder på att sådan kinetiskt driven kooperativitet kan vara en generell strategi som RNA-brytare använder för att samordna flera cellulära faktorer och finjustera genuttrycket.
Citering: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Nyckelord: riboswitch, glycerinavkänning, RNA-vikning, transkriptionspausering, bakteriell genreglering