Clear Sky Science · tr
Ko-transkripsiyonel katlanma, glisin tandem riboswitch tarafından ardışık çok-etkili algılamayı yönlendirir
RNA Anahtarları Bakterilere Akıllıca Kararlar Vermede Nasıl Yardımcı Olur
Bakteriler sürekli değişen ortamlarda yaşar, ancak enerji tasarrufu yapmak ve hayatta kalmak için hangi genleri açıp kapatacaklarına anında karar vermek zorundadır. Bu çalışma, Bacillus subtilis içinde yer alan küçük bir RNA “anahtarının” aynı anda bir amino asit, metal iyonları ve bir protein kofaktörü gibi birden çok moleküler sinyali nasıl dinlediğini ve ardından bir genin okunmasına devam edip etmeyeceğine ya da kapatılacağına hızla nasıl karar verdiğini ortaya koyuyor. Bu yerleşik karar devresini anlamak, gen kontrolünün temel kurallarını açığa çıkarmakla kalmaz, aynı zamanda sentetik biyoloji ve antibiyotik tasarımı için yeni araçlara ilham verebilir.
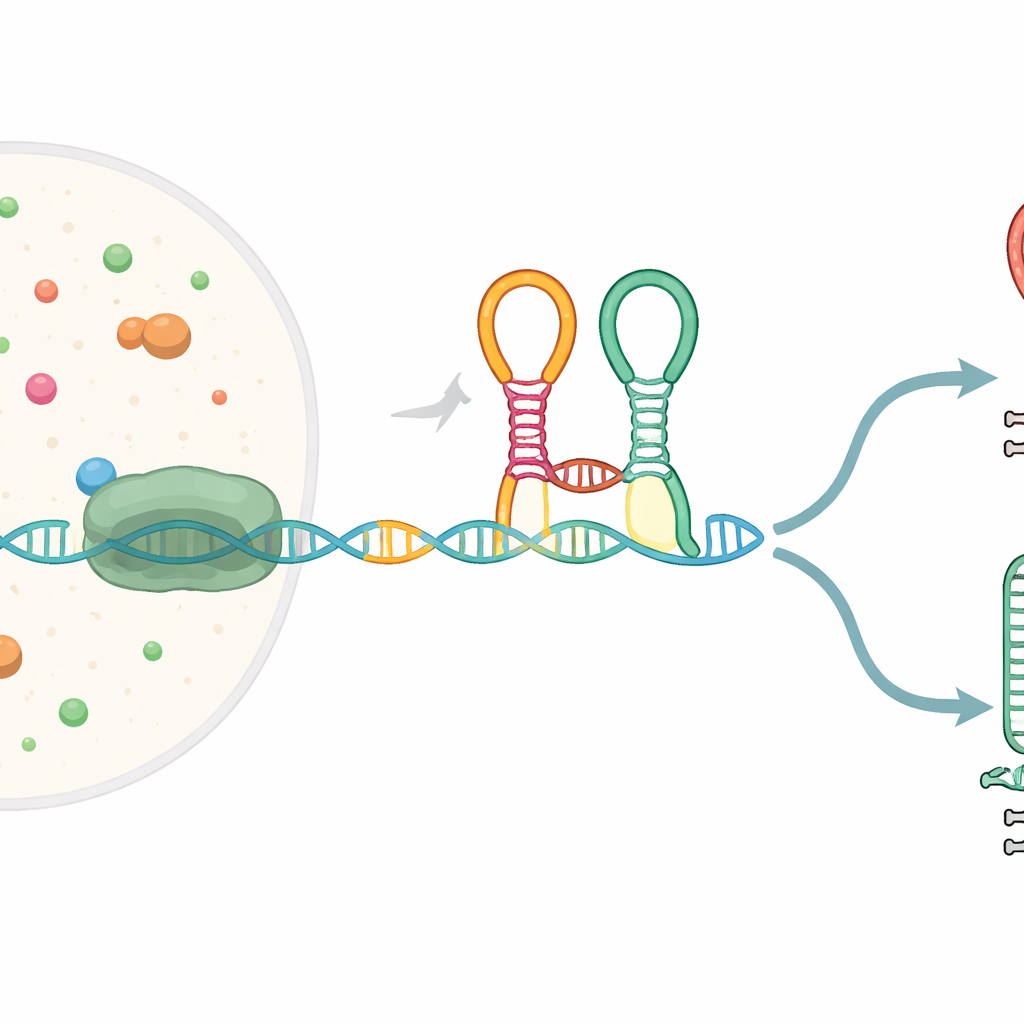
Gen Mesajının İçine Yerleştirilmiş Küçük Bir Sensör
Birçok bakteriyel gen, küçük molekülleri algılayabilen ve yanıt olarak gen ifadesini değiştiren şekillere katlanan riboswitch adı verilen özel RNA segmentleri ile başlar. Burada incelenen riboswitch, glisin tandem riboswitch olarak bilinir ve glisin amino asidini parçalamaya yardımcı genlerin önünde bulunur. İkisi bitişik algılama modülü (“aptamer”) içerir; her ikisi de glisini tanır ve bir kink-turn (kıvrım) adı verilen keskin bir bükülme ile bağlanır. RNA mesajı DNA’dan RNA polimeraz tarafından kopyalanırken, bu riboswitch uçuş sırasında katlanır ve süreci ya tam uzunlukta transkriptin tamamlanmasına ya da yerleşik bir durdurma sinyalinde kısaltılmasına yönlendirebilir.
Karar Kontrol Noktaları Oluşturan Duraklamalar
Yazarlar, RNA’yı kopyalayan enzimin bu bölgeden düzgünce ilerlemediğini; bunun yerine riboswitch içinde üç özel noktada durakladığını buldular. Bu duraklamalar, ortaya çıkan RNA’ya katlanması ve çevresindeki moleküllerle etkileşmesi için zaman veren trafik ışıkları gibi davranır. İlk duraklamada, yukarı akıştaki aptamer oluşur ve glisine bağlanmaya hazır hale gelir. Daha sonraki duraklamalarda, ikinci aptamerin bazı kısımları ve nihai karar heliksi ortaya çıkar. NusA adlı bir yardımcı protein, özellikle glisin bulunduğunda bu duraklamalardan ikisini uzatarak riboswitch’in çevresini algılama ve ya transkripsiyona devam etme ya da sonlandırma yönünde kararlılık gösterme zaman penceresini etkili biçimde genişletir.
İyonları, Glisini ve Bir Protein Ortağı Adım Adım Algılama
Tek moleküllü floresan mikroskobu ve yüksek verimli kimyasal problama kullanarak ekip, riboswitch’in tek seferde davranmadığını gösterdi. Önce potasyum iyonları RNA’nın tabanındaki kink-turn’u stabilize eder ve birinci aptameri büyüyen transkriptin yoluna doğru yönlendirir. Ardından glisin bu birinci aptamera bağlanarak yerel yapısını sıkılaştırır. Bu olaylar, ikinci glisin gelmeden önce her iki glisin bağlama cebini önceden düzenleyen iki aptamer arasında uzun menzilli temasları teşvik eder. Yerleşik terminatör saç tokasına yakın son duraklamada, önceden düzenlenmiş bu ortamda aşağı akış aptamerine ikinci bir glisin bağlanabilir ve NusA ile güçlenen duraklama, bu kompakt ve aktif konfigürasyonun tamamlanmasını daha da destekler.
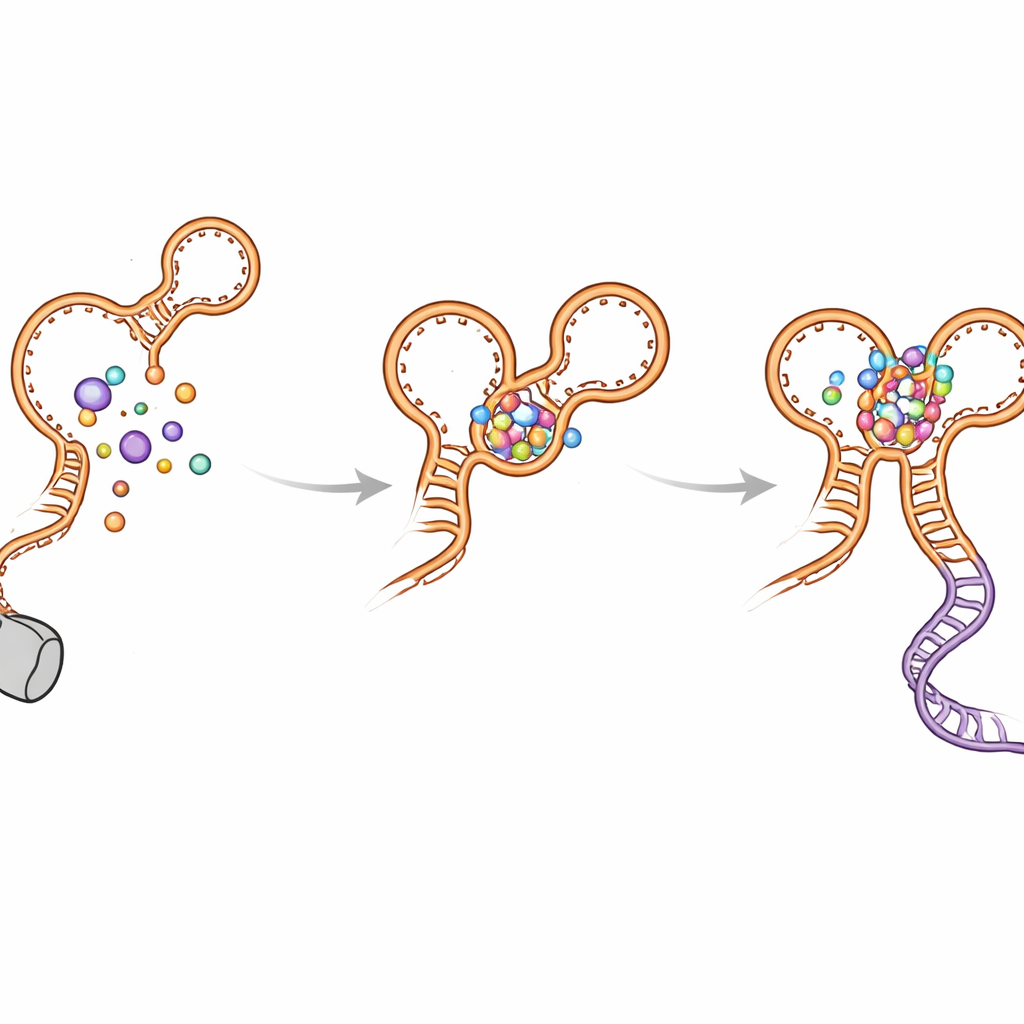
Katlanma Saptırmaları ve Anahtarın Takılmaktan Nasıl Kaçındığı
Yazarlar ayrıca RNA büyüdükçe geçici olarak oluşan birkaç “yanlış dönüş” saç tokası (hairpin) keşfettiler. Bu özgün olmayan yapılar her iki aptamerde de ortaya çıkarak nihai, aktif formun oluşmasını geciktirebilir. Kink-turn heliksi (P0 olarak adlandırılan) ve aptamerler arası temaslar bu ara ürünleri çözmeye yardımcı olur ve katlanmayı işlevsel düzenlemeye yönlendirir. P0 veya temel temas noktaları mutasyonlarla bozulduğunda, riboswitch duyarlılığının ve verimliliğinin büyük kısmını kaybeder: glisin hâlâ bağlanır, ancak uzun menzilli yerleşme zayıflar, karar heliksi daha az kararlı olur ve transkripsiyonun okunması azalır. Bilgisayar simülasyonları da bu gözlemleri destekleyerek P0 ve her iki glisin bölgesi sağlam olduğunda riboswitch’in çok daha kompakt ve stabil olduğunu gösterdi.
Canlı Hücrelerde Denge Dışı Bir Mantık Kapısı
Toplu olarak, bulgular glisin tandem riboswitch’in basit bir denge sensörü yerine kinetik bir mantık kapısı gibi davrandığı resmini destekliyor. Her iki glisin molekülünün önceden oluşmuş bir yapıya eşzamanlı bağlanması yerine, bağlanma ve katlanma transkripsiyon duraklamalarıyla kapılan ve potasyum iyonları ile NusA proteini tarafından şekillendirilen kesin bir 5′-ten-3′-e sırayla gerçekleşir. Bu adım adım, denge dışı süreç bakterinin hücresel iyon dengesi, glisin düzeyleri ve transkripsiyon hızı gibi birkaç sinyali birleştirmesine ve ardından aşağıdaki glisin parçalayıcı genleri tam olarak ifade edip etmeme kararını vermesine olanak tanır. Çalışma, bu kinetik olarak yönlendirilen işbirliğinin, RNA anahtarlarının çoklu hücresel faktörleri koordine edip gen ifadesini hassas biçimde ayarlamak için genel bir strateji olabileceğini öne sürüyor.
Atıf: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Anahtar kelimeler: riboswitch, glisin algılama, RNA katlanması, transkripsiyon duraklaması, bakteriyel gen regülasyonu