Clear Sky Science · ar
الطي المشترك مع النسخ ينظم استشعارًا متتابعًا متعدد المؤثرات بواسطة ريبوسويتش سلسلة الغلايسين
كيف تساعد مفاتيح الـ RNA البكتيريا على اتخاذ قرارات ذكية
تعيش البكتيريا في بيئات متغيرة باستمرار، ومع ذلك عليها أن تقرر في الزمن الحقيقي أي الجينات تُشغّل أو تُطفأ لتوفير الطاقة والبقاء. تكشف هذه الدراسة كيف يستمع مفتاح RNA الصغير داخل بكتيريا Bacillus subtilis إلى إشارات جزيئية متعددة في آن واحد — حمض أميني، أيونات معدنية، وعامل بروتيني — ثم يختار بسرعة ما إذا كان سيستمر في قراءة الجين أم سيوقفه. فهم هذا الدائرة القرارية المدمجة لا يوضح فقط قواعد أساسية في التحكم بالجينات، بل قد يلهم أيضًا أدوات جديدة في الهندسة الحيوية والتصميم المضاد للمضادات الحيوية.
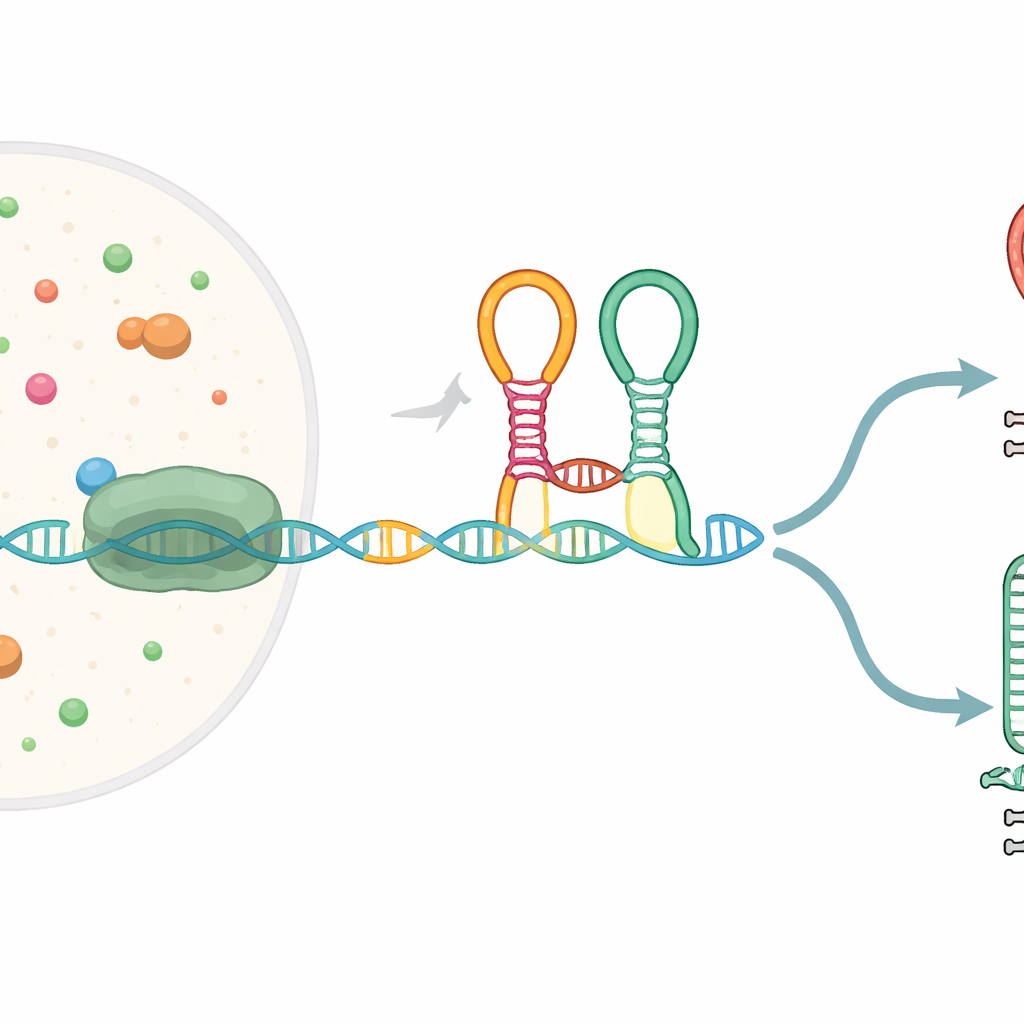
حساس صغير مدمج في رسالة الجين
تبدأ العديد من الجينات البكتيرية بمقاطع RNA خاصة تُسمى ريبوسويتشات، التي تطوى إلى أشكال قادرة على استشعار جزيئات صغيرة وتغيير التعبير الجيني استجابةً لذلك. الريبوسويتش المدروس هنا، المعروف بريبوسويتش سلسلة الغلايسين، يقع أمام جينات تساعد على تكسير حمض الغلايسين الأميني. يحتوي على وحدتين استشعار متجاورتين («أبتامرات») كلتاهما تتعرفان على الغلايسين ومُرتبطتان بانثناء حاد يُسمى طية-الخرج (kink-turn). أثناء نسخ رسالة الـ RNA من الـ DNA بواسطة إنزيم البوليميراز، يطوى هذا الريبوسويتش أثناء التكوين ويمكنه توجيه العملية إما نحو إكمال النسخة الكاملة أو تقصيرها عند إشارة إيقاف مدمجة.
توقُّفات تخلق نقاط فحص قرارية
وجد المؤلفون أن إنزيم نسخ الـ RNA لا يتحرك بسلاسة عبر هذه المنطقة؛ بل يتوقف عند ثلاثة مواقع محددة داخل الريبوسويتش. تعمل هذه التوقُّفات كإشارات مرور، مانحةً للـ RNA الناشئ وقتًا للطي والتفاعل مع الجزيئات المحيطة. عند التوقُّف الأول، تتكوّن الأبتامرة العلوية وتصبح جاهزة لارتباط الغلايسين. عند التوقُّفات اللاحقة، تظهر أجزاء من الأبتامرة الثانية والحلزون القراري النهائي. يطيل بروتين مساعد يسمى NusA اثنين من هذه التوقُّفات، وخصوصًا عندما يكون الغلايسين حاضرًا، موسعًا عمليًا نافذة الوقت التي يمكن للريبوسويتش خلالها استشعار بيئته والالتزام إما باستكمال النسخ أو بإنهائه.
استشعار متدرج للأيونات والغلايسين وشريك بروتيني
باستخدام ميكروسكوب الفلورة أحادي الجزيء وتحليل كيميائي عالي الإنتاجية، أظهر الفريق أن الريبوسويتش لا يعمل بلمحة واحدة. أولًا، تثبّت أيونات البوتاسيوم طية-الخرج عند قاعدة الـ RNA، موجهة الأبتامرة الأولى نحو مسار النسخة النامية. ثم يرتبط الغلايسين بهذه الأبتامرة الأولى، مشدّدًا بنيتها المحلية. تشجع هذه الأحداث الاتصالات بعيدة المدى بين الأبتامرتين، مما يهيئ جيوب ارتباط الغلايسين في كلا الأبتامرتين حتى قبل وصول الغلايسين الثاني. عند التوقُّف النهائي بالقرب من حلزون الإنهاء المدمج، يمكن للغلايسين الثاني أن يرتبط بالأبتامرة المتجهة للأسفل في هذا الوسط المجهز مسبقًا، ويعزز توقُّف NusA اكتمال هذا التكوين المدمج والنشط.
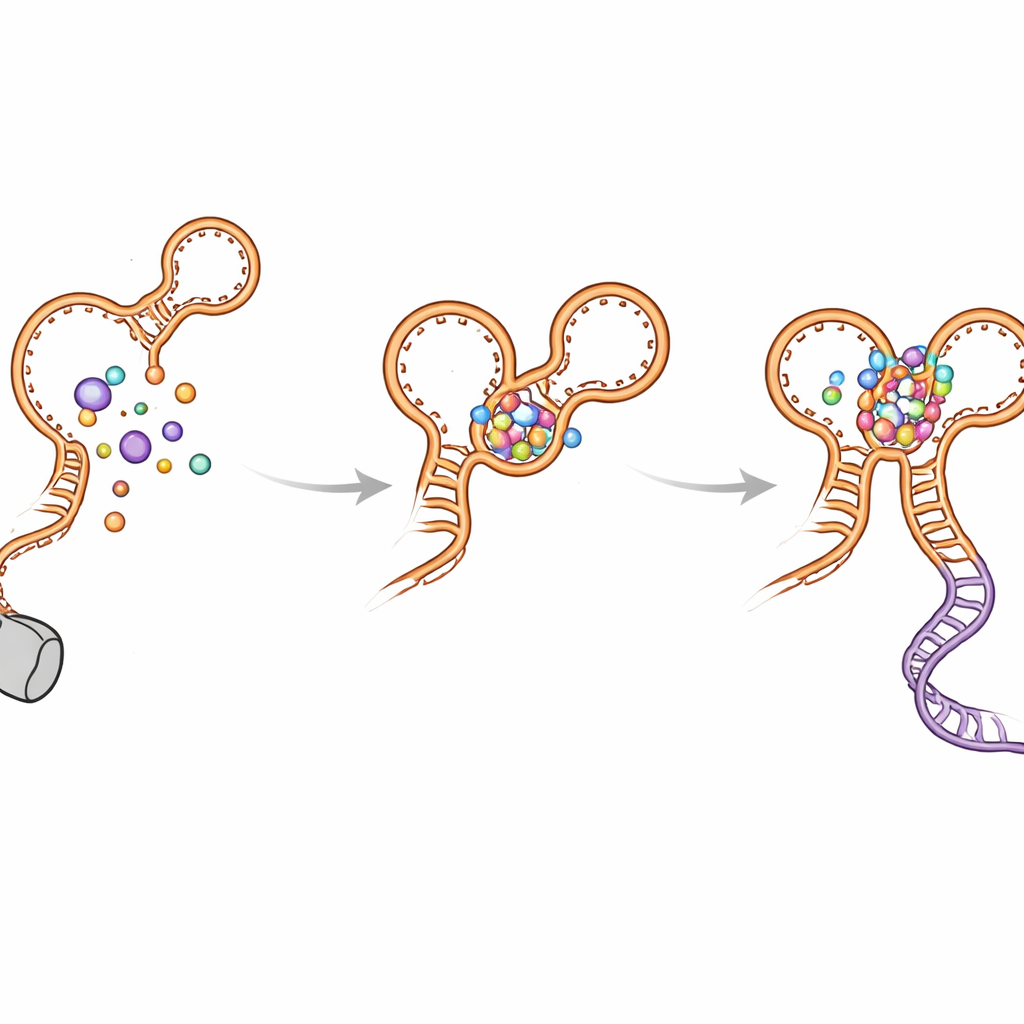
التواءات في الطي وكيف يتجنب المفتاح الانحباس
كما اكتشف المؤلفون عدة حلزونات «منعطف خاطئ» تتشكل مؤقتًا أثناء نمو الـ RNA. تظهر هذه البنى غير الأصلية في كلتا الأبتامرتين ويمكن أن تؤخر تكوين الشكل النهائي النشط. تساعد حلزونة طية-الخرج (المسماة P0) والاتصالات بين الأبتامرات في حل هذه المتوسطات وتوجيه الطي نحو التخطيط الوظيفي. عندما تتعرض P0 أو نقاط اتصال رئيسية للطفرات، يفقد الريبوسويتش جزءًا كبيرًا من حساسيته وكفاءته: لا يزال الغلايسين يرتبط، لكن الرسو طويل المدى يصبح أضعف، والحلزون القراري أقل استقرارًا، ويتناقص تجاوز النسخ. دعمت المحاكاة الحاسوبية هذه الملاحظات، مبيّنة أن الريبوسويتش يكون أكثر انضغاطًا واستقرارًا عندما تكون P0 وموقعي الغلايسين سليمتين.
بوابة منطقية خارجة عن التوازن في خلايا حية
تدعم النتائج مجتمعة صورةً يفعل فيها ريبوسويتش سلسلة الغلايسين بمثابة بوابة منطقية حركية بدلًا من كونها مجسًا بسيطًا في حالة توازن. بدلًا من ارتباط الجزيئتين بالغلايسين في آن واحد بهيكل مُشكّل مسبقًا، يحدث الارتباط والطي في تتابع دقيق من 5′ إلى 3′، يتحكم فيه توقُّفات النسخ ويشكّله أيونات البوتاسيوم وبروتين NusA. تتيح هذه العملية المتدرجة والخارجة عن التوازن للبكتيريا دمج عدة إشارات — توازن أيونات الخلية، مستويات الغلايسين، وسرعة النسخ — قبل أن تقرر ما إذا كانت ستُعبّر بشكل كامل عن الجينات القاطعة للغلايسين أسفلها. يشير العمل إلى أن التعاون المدفوع حركيًا قد يكون استراتيجية عامة تستخدمها مفاتيح الـ RNA لتنسيق عوامل خلوية متعددة لضبط التعبير الجيني بدقة.
الاستشهاد: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
الكلمات المفتاحية: ريبوسويتش, استشعار الغلايسين, طيّ الحمض النووي الريبي, توقف النسخ, تنظيم الجينات البكتيرية