Clear Sky Science · ru
Ко-транскрипционная сворачиваемость координирует последовательное многокомпонентное распознавание тандемным рибосвитчем для глицина
Как РНК‑переключатели помогают бактериям принимать разумные решения
Бактерии живут в постоянно меняющейся среде и при этом должны в реальном времени решать, какие гены включать или выключать, чтобы экономить энергию и выживать. В этом исследовании показано, как крошечный РНК «переключатель» у Bacillus subtilis одновременно отслеживает несколько молекулярных сигналов — аминокислоту, ионы металлов и белковый кофактор — и затем быстро принимает решение: продолжать считывание гена или прекратить его. Понимание этой встроенной схемы принятия решений раскрывает фундаментальные правила управления генами и может вдохновить новые инструменты для синтетической биологии и разработки антибиотиков.
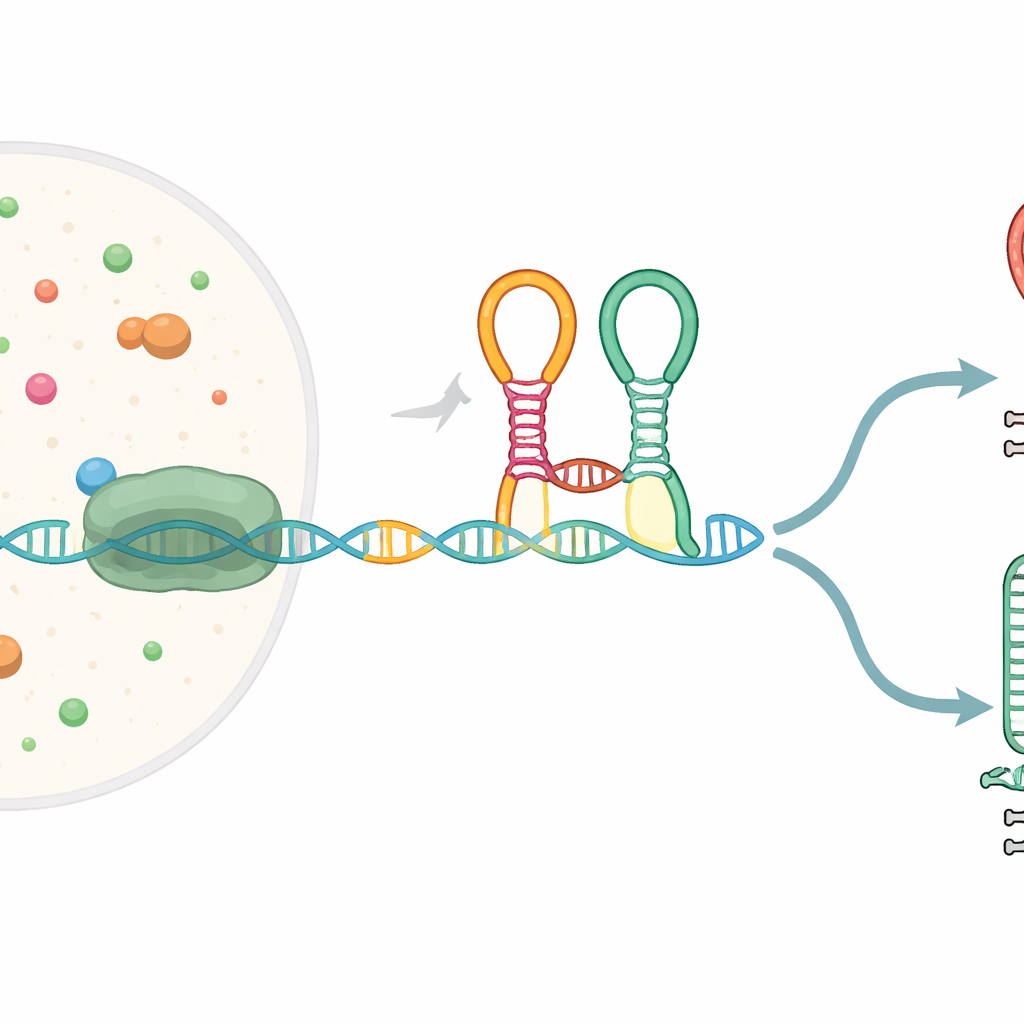
Крошечный сенсор, встроенный в сообщение гена
Многие бактериальные гены начинаются со специальных сегментов РНК, называемых рибосвитчами, которые сворачиваются в формы, способные распознавать малые молекулы и в ответ изменять экспрессию генов. Рибосвитч, изученный здесь, известен как тандемный глициновый рибосвитч; он расположен перед генами, участвующими в расщеплении аминокислоты глицина. Он содержит два прилегающих сенсорных модуля («аптамера»), оба распознающие глицин, и соединён резким изгибом, называемым kink‑turn. Пока РНК‑сообщение копируется с ДНК РНК‑полимеразой, рибосвитч сворачивается «на лету» и может направить процесс либо к завершению полного транскрипта, либо к укорочению на встроенном сигнале остановки.
Паузы, создающие контрольные точки для решения
Авторы обнаружили, что фермент, копирующий РНК, не проходит эту область равномерно; вместо этого он делает паузы в трёх определённых местах внутри рибосвитча. Эти паузы действуют как светофоры, давая вновь появляющейся РНК время свараться и взаимодействовать с окружающими молекулами. На первой паузе формируется вверхпо-потоковый аптамер и становится готовым к связыванию глицина. На последующих паузах появляются участки второго аптамера и окончательная «решающая» спираль. Помогающий белок NusA удлиняет две из этих пауз, особенно в присутствии глицина, фактически расширяя временное окно, в течение которого рибосвитч может считывать окружение и принять решение — продолжить транскрипцию или прервать её.
Пошаговое распознавание ионов, глицина и белкового партнёра
С помощью флуоресцентной микроскопии одиночных молекул и высокопроизводительного химического зондирования команда показала, что рибосвитч не действует в одном мгновении. Сначала ионы калия стабилизируют kink‑turn у основания РНК, ориентируя первый аптамер в направлении растущего транскрипта. Затем глицин связывается с этим первым аптамером, уплотняя его локальную структуру. Эти события способствуют образованию дальних контактов между двумя аптамерами, которые предварительно организуют оба глицин‑связывающих кармана ещё до прихода второго глицина. На окончательной паузе рядом с встроенной терминаторной шпилькой второй глицин может связаться со вторым аптамером в этой предорганизованной среде, а усиленная NusA пауза дополнительно способствует завершению компактной, активной конфигурации.
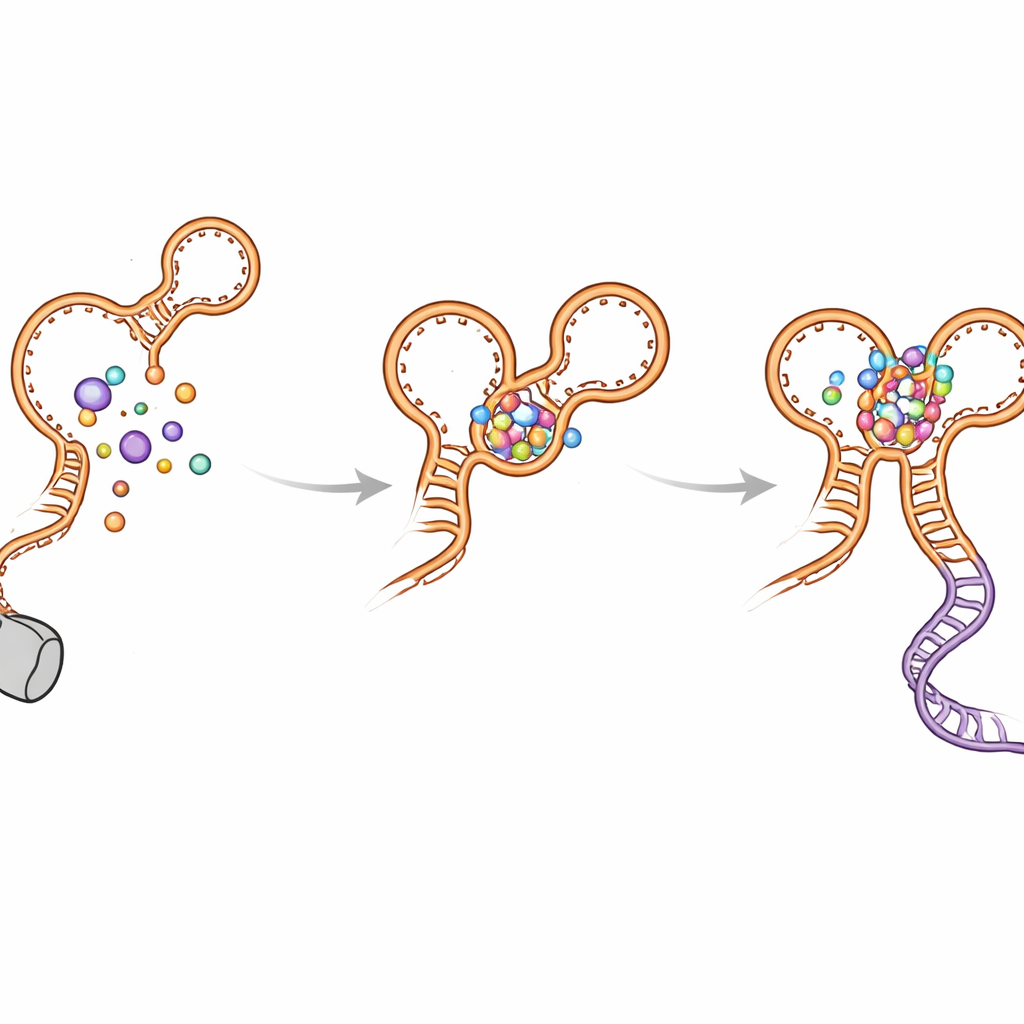
Отклонения в сворачивании и как переключатель избегает застревания
Авторы также обнаружили несколько временных «неправильных» шпилек, которые формируются по мере роста РНК. Эти не‑нативные структуры появляются в обоих аптамерах и могут задерживать образование финальной активной формы. Геликс kink‑turn (обозначаемый P0) и межаптамерные контакты помогают разрешать эти промежуточные состояния и направлять сворачивание в функциональную конфигурацию. Когда P0 или ключевые контактные точки нарушены мутациями, рибосвитч теряет большую часть чувствительности и эффективности: глицин по‑прежнему связывается, но дальние «дocking»‑взаимодействия ослаблены, решающая спираль менее стабильна, и уровень прохождения транскрипта снижается. Компьютерное моделирование поддержало эти наблюдения, показав, что рибосвитч значительно более компактен и стабилен, когда P0 и оба глицин‑сайта сохранены.
Неравновесный логический элемент в живой клетке
В совокупности результаты свидетельствуют, что тандемный глициновый рибосвитч ведёт себя как кинетический логический элемент, а не как простой равновесный сенсор. Вместо того чтобы оба молекулы глицина связывались одновременно с пред‑сформированной структурой, связывание и сворачивание происходят в точной 5′→3′ последовательности, ограничиваемой транскрипционными паузами и формируемой ионами калия и белком NusA. Этот поэтапный, выходящий из равновесия процесс позволяет бактерии интегрировать несколько сигналов — ионный баланс, уровни глицина и скорость транскрипции — прежде чем принять решение о полном выражении соседних генов, расщепляющих глицин. Работа указывает, что такая кинетически управляемая кооперативность может быть общей стратегией, с помощью которой РНК‑переключатели координируют множество факторов клетки для тонкой настройки экспрессии генов.
Цитирование: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Ключевые слова: рибосвитч, распознавание глицина, сворачивание РНК, транскрипционные паузы, бактериальная регуляция генов