Clear Sky Science · pt
Dobramento co-transcricional orquestra sensação sequencial de múltiplos efetores por um ribosswitch tandem de glicina
Como interruptores de RNA ajudam bactérias a tomar decisões inteligentes
Bactérias vivem em ambientes em constante mudança e, ainda assim, precisam decidir em tempo real quais genes ativar ou silenciar para economizar energia e sobreviver. Este estudo revela como um pequeno “interruptor” de RNA dentro da bactéria Bacillus subtilis escuta múltiplos sinais moleculares ao mesmo tempo — um aminoácido, íons metálicos e um cofator proteico — e então escolhe rapidamente se continua lendo um gene ou se o interrompe. Entender esse circuito de decisão embutido não apenas revela regras fundamentais do controle gênico, como também pode inspirar novas ferramentas para biologia sintética e design de antibióticos.
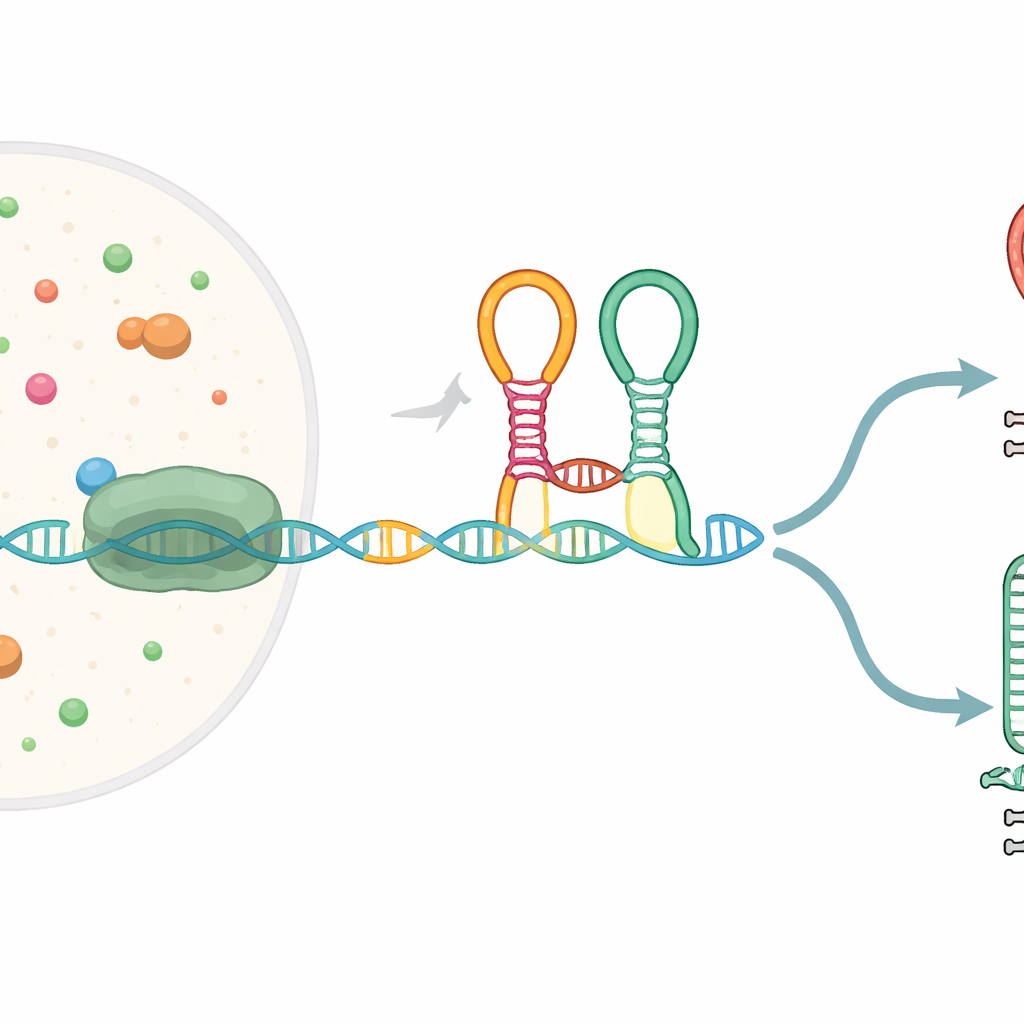
Um pequeno sensor incorporado na mensagem gênica
Muitos genes bacterianos começam com segmentos especiais de RNA chamados riboswitches, que se dobram em formas capazes de detectar pequenas moléculas e, em resposta, alterar a expressão gênica. O riboswitch estudado aqui, conhecido como riboswitch tandem de glicina, fica à frente de genes que ajudam a degradar o aminoácido glicina. Ele contém dois módulos sensoriais adjacentes (“aptâmeros”) que reconhecem glicina e são conectados por uma curva acentuada chamada kink-turn. Enquanto a mensagem de RNA é copiada do DNA pela RNA polimerase, esse riboswitch se dobra em tempo real e pode direcionar o processo para completar o transcrito em comprimento total ou encurtá-lo em um sinal de parada embutido.
Pausas que criam pontos de checagem para decisão
Os autores descobriram que a enzima que copia o RNA não se move suavemente por essa região; em vez disso, ela faz pausas em três pontos específicos dentro do riboswitch. Essas pausas funcionam como semáforos, dando ao RNA emergente tempo para se dobrar e interagir com moléculas ao redor. Na primeira pausa, o aptâmero upstream se forma e fica pronto para se ligar à glicina. Em pausas posteriores, partes do segundo aptâmero e o helicóide de decisão final emergem. Uma proteína assistente chamada NusA prolonga duas dessas pausas, especialmente quando glicina está presente, ampliando efetivamente a janela de tempo durante a qual o riboswitch pode detectar seu ambiente e decidir entre continuar a transcrição ou terminá-la.
Detecção em etapas de íons, glicina e um parceiro proteico
Usando microscopia de fluorescência de molécula única e sondagem química em alta escala, a equipe mostrou que o riboswitch não age num único instante. Primeiro, íons de potássio estabilizam o kink-turn na base do RNA, orientando o primeiro aptâmero na direção do caminho do transcrito em crescimento. A glicina então se liga a esse primeiro aptâmero, apertando sua estrutura local. Esses eventos favorecem contatos de longo alcance entre os dois aptâmeros, que pre-organizam ambos os bolsões de ligação à glicina mesmo antes da chegada da segunda glicina. Na pausa final próxima ao hairpin terminador embutido, uma segunda glicina pode se ligar ao aptâmero a jusante nesse ambiente pré-organizado, e a pausa ampliada por NusA favorece ainda mais a conclusão dessa configuração compacta e ativa.
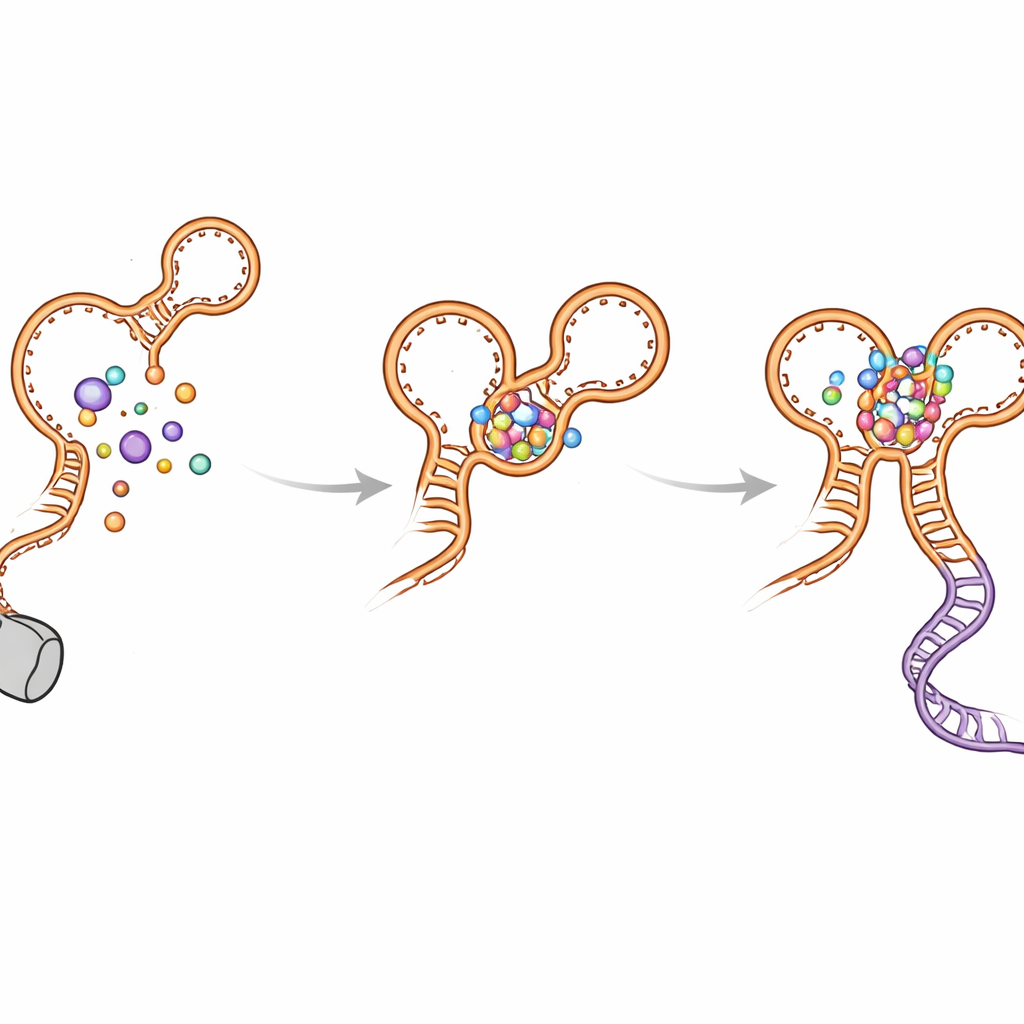
Desvios de dobramento e como o interruptor evita ficar preso
Os autores também descobriram vários hairpins de “rua errada” que se formam temporariamente à medida que o RNA cresce. Essas estruturas não nativas aparecem em ambos os aptâmeros e podem atrasar a formação da forma final e ativa. O helicoide kink-turn (chamado P0) e os contatos entre aptâmeros ajudam a resolver esses intermediários e conduzir o dobramento para o arranjo funcional. Quando P0 ou pontos de contato chave são perturbados por mutações, o riboswitch perde grande parte de sua sensibilidade e eficiência: a glicina ainda se liga, mas o encaixe de longo alcance fica enfraquecido, o helicoide de decisão fica menos estável e a leitura transcricional completa diminui. Simulações computacionais corroboraram essas observações, mostrando que o riboswitch é muito mais compacto e estável quando P0 e ambos os sítios de glicina estão intactos.
Uma porta lógica fora do equilíbrio em células vivas
Em conjunto, os resultados sustentam uma imagem na qual o riboswitch tandem de glicina se comporta como uma porta lógica cinética em vez de um sensor simples de equilíbrio. Em vez de ambas as moléculas de glicina se ligarem simultaneamente a uma estrutura pré-formada, a ligação e o dobramento ocorrem em uma sequência precisa de 5′ para 3′, regulada por pausas de transcrição e moldada por íons de potássio e pela proteína NusA. Esse processo em etapas, fora do equilíbrio, permite que a bactéria integre vários sinais — balanço iônico celular, níveis de glicina e velocidade de transcrição — antes de decidir se expressa totalmente os genes que degradam a glicina. O trabalho sugere que essa cooperatividade dirigida cineticamente pode ser uma estratégia geral pela qual interruptores de RNA coordenam múltiplos fatores celulares para ajustar finamente a expressão gênica.
Citação: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Palavras-chave: riboswitch, detecção de glicina, dobramento de RNA, pausas na transcrição, regulação gênica bacteriana