Clear Sky Science · fr
Le repliement co-transcriptionnel orchestre la détection séquentielle multi-effetrice par un riboswitch en tandem pour la glycine
Comment les interrupteurs d'ARN aident les bactéries à faire des choix judicieux
Les bactéries vivent dans des environnements en perpétuel changement et doivent décider en temps réel quels gènes activer ou réprimer pour économiser de l'énergie et survivre. Cette étude révèle comment un petit « interrupteur » d'ARN à l'intérieur de la bactérie Bacillus subtilis écoute simultanément plusieurs indices moléculaires — un acide aminé, des ions métalliques et un cofacteur protéique — puis choisit rapidement de poursuivre ou d'arrêter la lecture d'un gène. Comprendre ce circuit décisionnel intégré révèle non seulement des règles fondamentales du contrôle génique, mais pourrait aussi inspirer de nouveaux outils pour la biologie synthétique et la conception d'antibiotiques.
Un minuscule capteur intégré au message génique
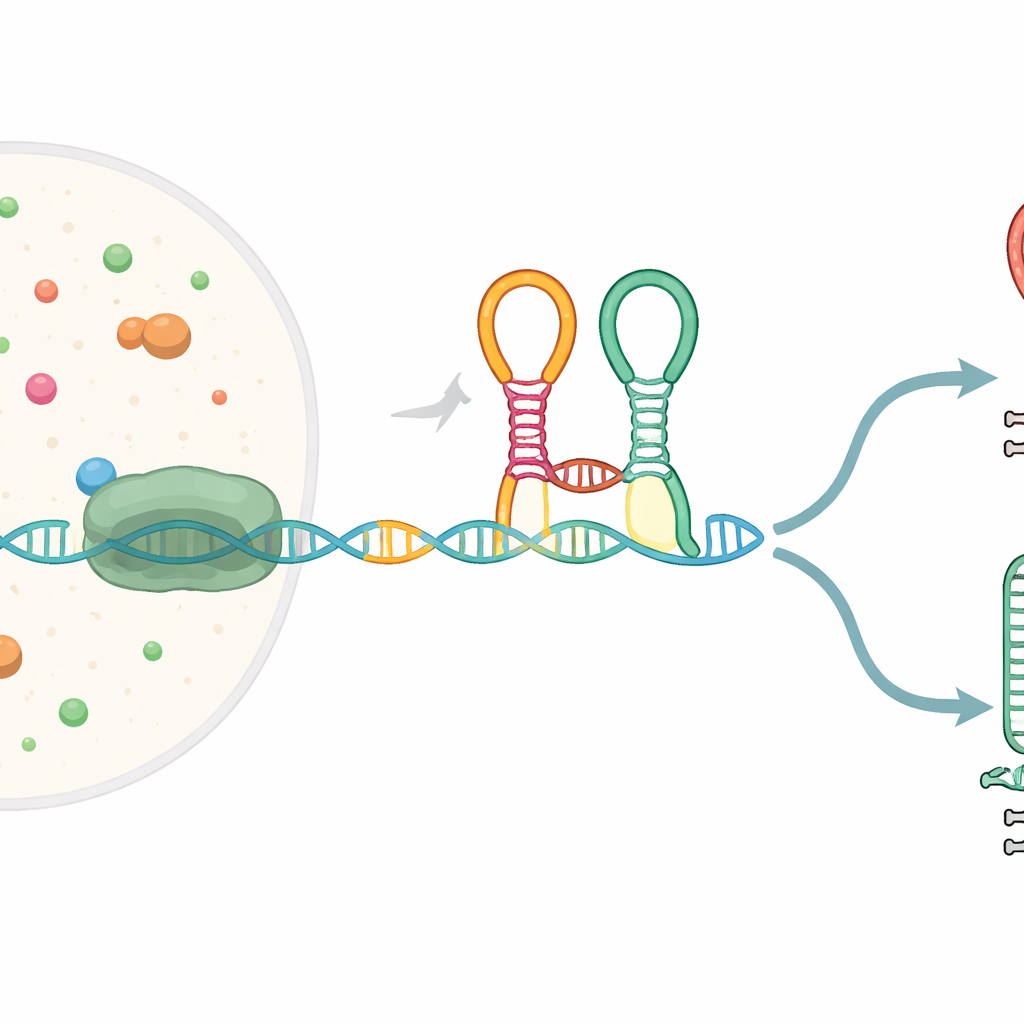
Beaucoup de gènes bactériens commencent par des segments d'ARN spéciaux appelés riboswitches, qui se replient en formes capables de détecter de petites molécules et, en réponse, de modifier l'expression génique. Le riboswitch étudié ici, connu sous le nom de riboswitch en tandem pour la glycine, se situe en amont de gènes impliqués dans la dégradation de l'acide aminé glycine. Il contient deux modules de détection adjacents (« aptamères ») qui reconnaissent tous deux la glycine et sont reliés par un coude prononcé appelé kink-turn. Pendant que le message ARN est copié de l'ADN par l'ARN polymérase, ce riboswitch se replie à la volée et peut orienter le processus soit vers l'achèvement du transcrit en longueur complète, soit vers son interruption à un signal d'arrêt intégré.
Des pauses qui créent des points de décision
Les auteurs ont constaté que l'enzyme copiant l'ARN ne progresse pas de manière continue dans cette région ; au contraire, elle marque trois pauses spécifiques au sein du riboswitch. Ces pauses agissent comme des feux de circulation, donnant au nouvel ARN le temps de se replier et d'interagir avec les molécules environnantes. Lors de la première pause, l'aptamère en amont se forme et devient prêt à lier la glycine. Lors des pauses ultérieures, des portions du second aptamère et l'hélice de décision finale émergent. Une protéine auxiliaire appelée NusA prolonge deux de ces pauses, surtout en présence de glycine, élargissant ainsi la fenêtre temporelle pendant laquelle le riboswitch peut sonder son environnement et se décider à poursuivre ou à terminer la transcription.
Détection pas à pas des ions, de la glycine et d'un partenaire protéique
En combinant microscopie de fluorescence à molécule unique et sonde chimique à haut débit, l'équipe a montré que le riboswitch n'agit pas d'un seul coup. D'abord, les ions potassium stabilisent le kink-turn à la base de l'ARN, orientant le premier aptamère dans la trajectoire du transcrit en croissance. La glycine se lie ensuite à ce premier aptamère, resserrant sa structure locale. Ces événements favorisent des contacts longue distance entre les deux aptamères, qui pré-organisent les deux poches de liaison à la glycine même avant l'arrivée de la seconde glycine. À la pause finale proche de l'épine terminale intégrée, une seconde glycine peut se lier à l'aptamère aval dans cet environnement pré-organisé, et la pause prolongée par NusA favorise davantage l'achèvement de cette configuration compacte et active.
Détours de repliement et comment l'interrupteur évite de rester bloqué
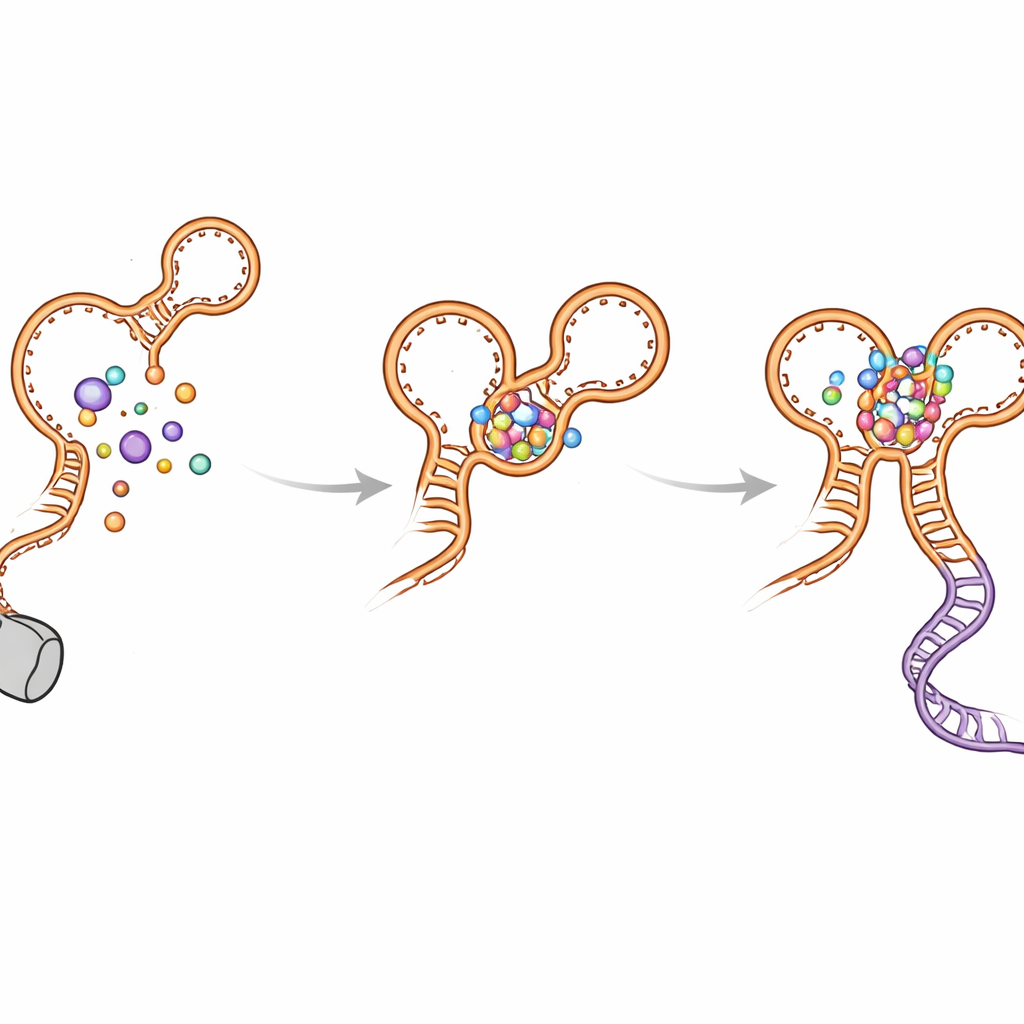
Les auteurs ont également découvert plusieurs épingles « mauvais virage » qui se forment temporairement à mesure que l'ARN croît. Ces structures non natives apparaissent dans les deux aptamères et peuvent retarder la formation de la conformation finale et active. L'hélice kink-turn (appelée P0) et les contacts inter-aptamères aident à résoudre ces intermédiaires et à orienter le repliement vers la configuration fonctionnelle. Lorsque P0 ou des points de contact clés sont perturbés par des mutations, le riboswitch perd beaucoup de sa sensibilité et de son efficacité : la glycine se lie encore, mais le dockage longue distance est affaibli, l'hélice de décision est moins stable et le franchissement de la transcription diminue. Des simulations informatiques ont corroboré ces observations, montrant que le riboswitch est beaucoup plus compact et stable lorsque P0 et les deux sites de glycine sont intacts.
Une porte logique hors-équilibre dans les cellules vivantes
Pris ensemble, les résultats soutiennent le modèle selon lequel le riboswitch en tandem pour la glycine se comporte comme une porte logique cinétique plutôt que comme un simple détecteur à l'équilibre. Plutôt que les deux molécules de glycine se liant simultanément à une structure préformée, la liaison et le repliement se produisent dans une séquence précise 5′→3′, régulée par des pauses de transcription et façonnée par les ions potassium et la protéine NusA. Ce processus pas à pas, hors d'équilibre, permet à la bactérie d'intégrer plusieurs signaux — l'équilibre ionique cellulaire, les niveaux de glycine et la vitesse de transcription — avant de décider d'exprimer ou non pleinement les gènes de dégradation de la glycine en aval. Ce travail suggère que cette coopération régie par la cinétique pourrait être une stratégie générale par laquelle les commutateurs d'ARN coordonnent plusieurs facteurs cellulaires pour ajuster finement l'expression génique.
Citation: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Mots-clés: riboswitch, détection de la glycine, repliement de l'ARN, pause de transcription, régulation génique bactérienne