Clear Sky Science · nl
Co-transcriptionele vouwing orkestreert sequentiële multi-effector-detectie door een glycine tandem-riboswitch
Hoe RNA-schakelaars bacteriën helpen slimme keuzes te maken
Bacteriën leven in voortdurend veranderende omgevingen, maar moeten in real time beslissen welke genen ze aan- of uitzetten om energie te besparen en te overleven. Deze studie onthult hoe een klein RNA “schakelaartje” in Bacillus subtilis tegelijk meerdere moleculaire signalen opvangt—een aminozuur, metaalionen en een eiwitcofactor—en vervolgens snel kiest of het gen blijft worden afgelezen of wordt stopgezet. Inzicht in dit ingebouwde beslissingscircuit onthult niet alleen fundamentele regels van genregulatie, maar kan ook nieuwe instrumenten voor synthetische biologie en antibioticumontwerp inspireren.
Een piepkleine sensor ingebouwd in het genbericht
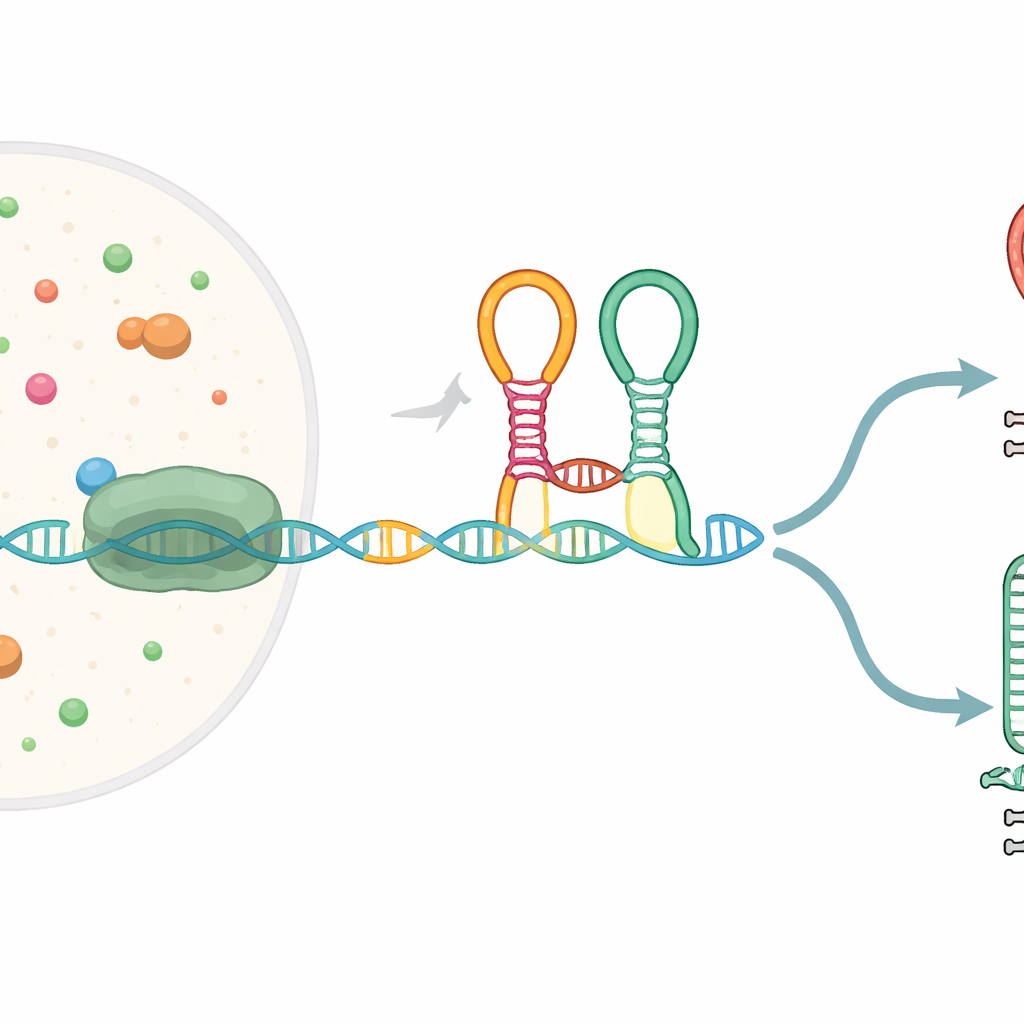
Veel bacteriële genen beginnen met speciale RNA-segmenten die riboswitches worden genoemd; deze vouwen zich tot vormen die kleine moleculen kunnen waarnemen en daardoor de genexpressie wijzigen. De hier bestudeerde riboswitch, de zogenaamde glycine tandem-riboswitch, bevindt zich voor genen die helpen bij de afbraak van het aminozuur glycine. Hij bevat twee aangrenzende sensormodules (“aptamers”) die beide glycine herkennen en met elkaar verbonden zijn door een scherpe buiging, een kink-turn. Terwijl het RNA-bericht door RNA-polymerase van het DNA wordt gekopieerd, vouwt deze riboswitch zich tijdens het proces en kan hij de voortgang sturen naar ofwel het voltooien van het volledige transcript ofwel het vroegtijdig afbreken bij een ingebouwd stopsein.
Pauzes die beslissingscheckpoints creëren
De auteurs ontdekten dat het RNA-kopieerenzym niet vloeiend door dit gebied beweegt; in plaats daarvan pauzeert het op drie specifieke plekken binnen de riboswitch. Deze pauzes werken als verkeerslichten en geven het opkomende RNA tijd om te vouwen en met omringende moleculen te interageren. Bij de eerste pauze vormt het upstream-aptameer zich en wordt het klaar om glycine te binden. Bij latere pauzes verschijnen onderdelen van het tweede aptameer en de uiteindelijke beslissingshelix. Een helper-eiwit genaamd NusA verlengt twee van deze pauzes, vooral wanneer glycine aanwezig is, waardoor effectief het tijdvenster wordt vergroot waarin de riboswitch zijn omgeving kan waarnemen en kan beslissen om de transcriptie voort te zetten of te beëindigen.
Stapsgewijze detectie van ionen, glycine en een eiwitpartner
Met enkel-molecuul fluorescentiemicroscopie en grootschalige chemische probing toonde het team aan dat de riboswitch niet in één keer handelt. Eerst stabiliseren kaliumionen de kink-turn aan de basis van het RNA, waardoor het eerste aptameer naar het pad van het groeiende transcript wordt georiënteerd. Vervolgens bindt glycine aan dit eerste aptameer en verstevigt zo de lokale structuur. Deze gebeurtenissen bevorderen lange-afstand contacten tussen de twee aptamers, die beide glycine-bindplaatsen vooraf organiseren nog voordat de tweede glycine arriveert. Bij de laatste pauze nabij de ingebouwde terminatorhairpin kan een tweede glycine binden aan het downstream-aptameer in deze vooraf georganiseerde omgeving, en door NusA-verlengde pauzes bevorderen verder het voltooien van deze compacte, actieve configuratie.
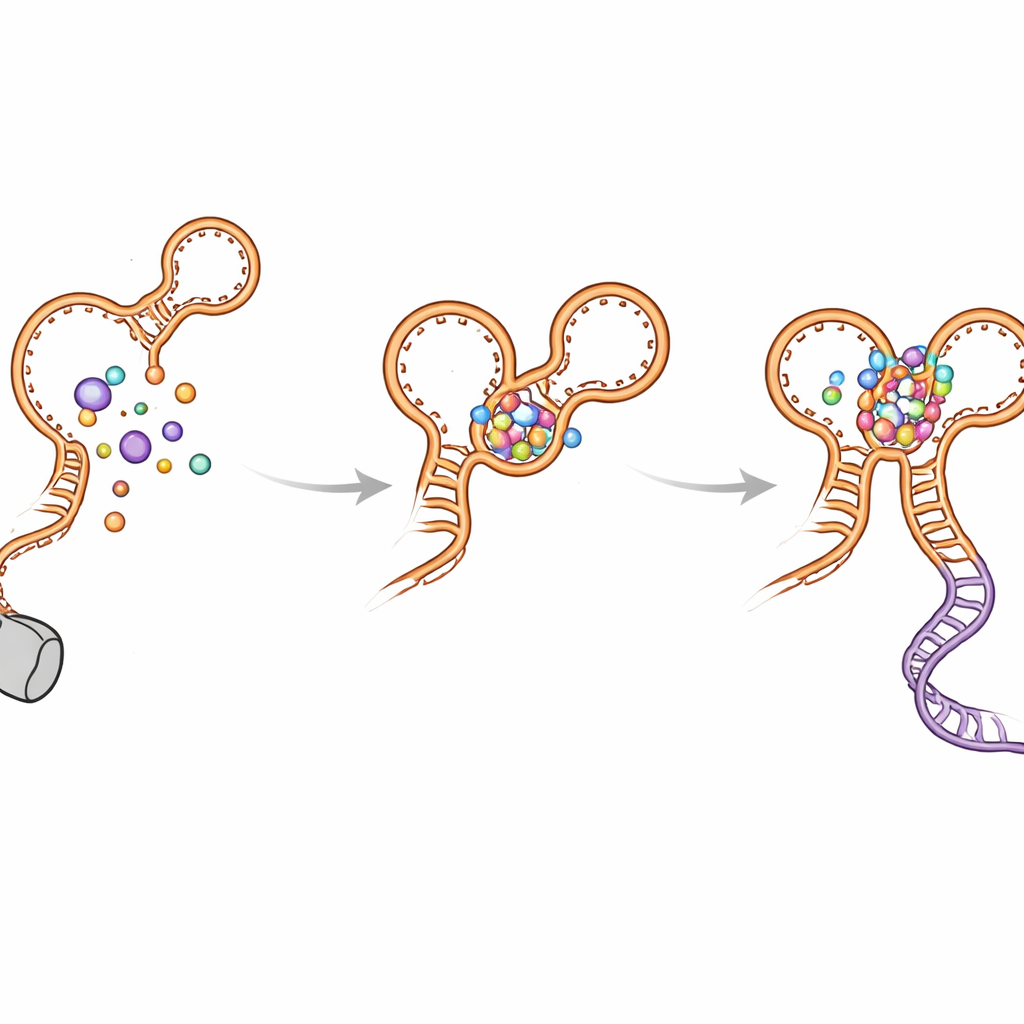
Vouwomwegen en hoe de schakelaar voorkomt dat hij vastloopt
De auteurs ontdekten ook meerdere tijdelijke ‘‘foute afslag’’-hairpins die zich vormen terwijl het RNA groeit. Deze niet-native structuren verschijnen in beide aptamers en kunnen de vorming van de uiteindelijke, actieve structuur vertragen. De kink-turn-helix (P0 genoemd) en de onderlinge aptameercontacten helpen deze tussenstadia op te lossen en sturen de vouwing naar de functionele indeling. Wanneer P0 of belangrijke contactpunten door mutaties worden verstoord, verliest de riboswitch een groot deel van zijn gevoeligheid en efficiëntie: glycine bindt nog steeds, maar de lange-afstand docking wordt verzwakt, de beslissingshelix is minder stabiel en transcriptiedoorloop neemt af. Computersimulaties ondersteunden deze observaties en toonden dat de riboswitch veel compacter en stabieler is wanneer P0 en beide glycineplaatsen intact zijn.
Een niet-evenwichts logische poort in levende cellen
Gezamenlijk ondersteunen de resultaten het beeld dat de glycine tandem-riboswitch zich gedraagt als een kinetische logische poort in plaats van als een eenvoudige evenwichtssensor. In plaats van dat beide glycinemoleculen gelijktijdig binden aan een vooraf gevormde structuur, vinden binden en vouwing plaats in een nauwkeurige 5′-naar-3′ volgorde, geregeld door transcriptie-pauzes en beïnvloed door kaliumionen en het eiwit NusA. Dit stapsgewijze, uit-evenwicht zijnde proces stelt de bacterie in staat meerdere signalen te integreren—cellulair ionengewicht, glycinegehalte en transcriptsiesnelheid—voordat wordt besloten de downstream glycine-afbrekende genen volledig tot expressie te brengen. Het werk suggereert dat zulke kinetisch aangedreven cooperativiteit een algemene strategie kan zijn waarmee RNA-schakelaars meerdere cellulaire factoren coördineren om genexpressie fijn af te stemmen.
Bronvermelding: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Trefwoorden: riboswitch, glycine-detectie, RNA-vouwing, transcriptie-pauzes, bacteriële genregulatie