Clear Sky Science · pl
Składanie współtranskrypcyjne orkiestruje sekwencyjne wykrywanie kilku efektorów przez tandemowy ryboswitch wiążący glicynę
Jak przełączniki RNA pomagają bakteriom podejmować mądre decyzje
Bakterie żyją w stale zmieniającym się środowisku, a mimo to muszą w czasie rzeczywistym decydować, które geny włączać lub wyłączać, by oszczędzać energię i przetrwać. To badanie ujawnia, jak drobny „przełącznik” RNA wewnątrz bakterii Bacillus subtilis nasłuchuje jednocześnie wielu sygnałów molekularnych — aminokwasu, jonów metalu i białkowego kofaktora — i szybko wybiera, czy kontynuować odczyt genów, czy go przerwać. Zrozumienie tego wbudowanego obwodu decyzyjnego nie tylko odsłania podstawowe zasady kontroli genów, lecz może też zainspirować nowe narzędzia do biologii syntetycznej i projektowania antybiotyków.
Maleńki czujnik wbudowany w informację genetyczną
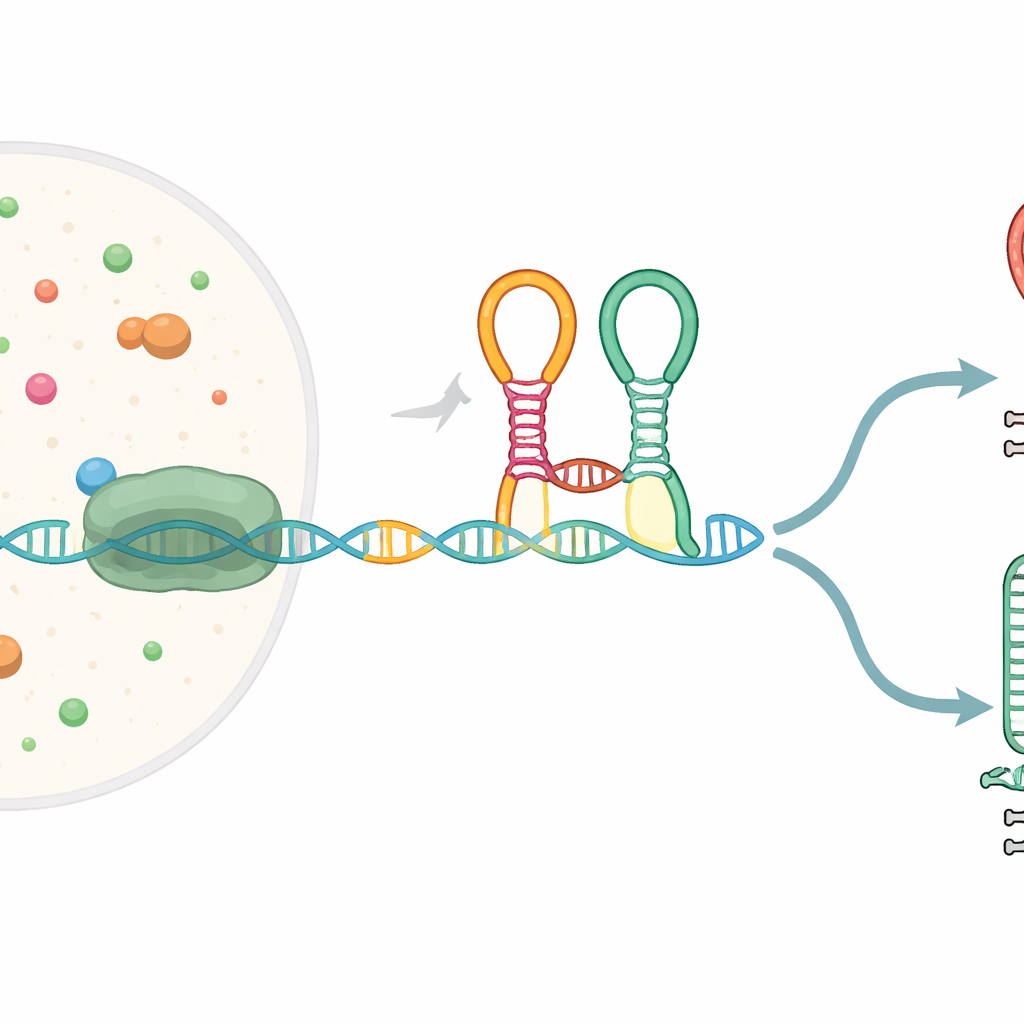
Wiele genów bakteryjnych zaczyna się od specjalnych fragmentów RNA zwanych ryboswitchami, które składają się w kształty zdolne wyczuwać małe cząsteczki i w odpowiedzi zmieniać ekspresję genów. Badany tutaj ryboswitch, znany jako tandemowy ryboswitch glicynowy, znajduje się przed genami pomagającymi rozkładać aminokwas glicynę. Zawiera dwa przyległe moduły detekcyjne („aptamery”), które oba rozpoznają glicynę, połączone ostrym załamaniem zwanym kink‑turn. W miarę jak informacja RNA jest przepisywana z DNA przez polimerazę RNA, ten ryboswitch składa się w locie i może skierować proces ku pełnemu przepisaniu transkryptu albo do jego skrócenia przy wbudowanym sygnale zatrzymania.
Przerwy tworzące punkty kontrolne decyzji
Autorzy wykazali, że enzym kopiujący RNA nie porusza się płynnie przez ten obszar; zamiast tego zatrzymuje się w trzech określonych miejscach wewnątrz ryboswitcha. Te pauzy działają jak światła drogowe, dając nowo powstającemu RNA czas na złożenie się i interakcję z otaczającymi molekułami. W pierwszej pauzie tworzy się górny aptamer i staje się gotowy do związania glicyny. W kolejnych pauzach pojawiają się fragmenty drugiego aptameru i ostateczna helisa decyzyjna. Białko pomocnicze NusA wydłuża dwie z tych pauz, szczególnie gdy obecna jest glicyna, poszerzając w praktyce okno czasowe, w którym ryboswitch może wyczuwać środowisko i podjąć decyzję o kontynuacji transkrypcji lub jej zakończeniu.
Krokowe wykrywanie jonów, glicyny i partnera białkowego
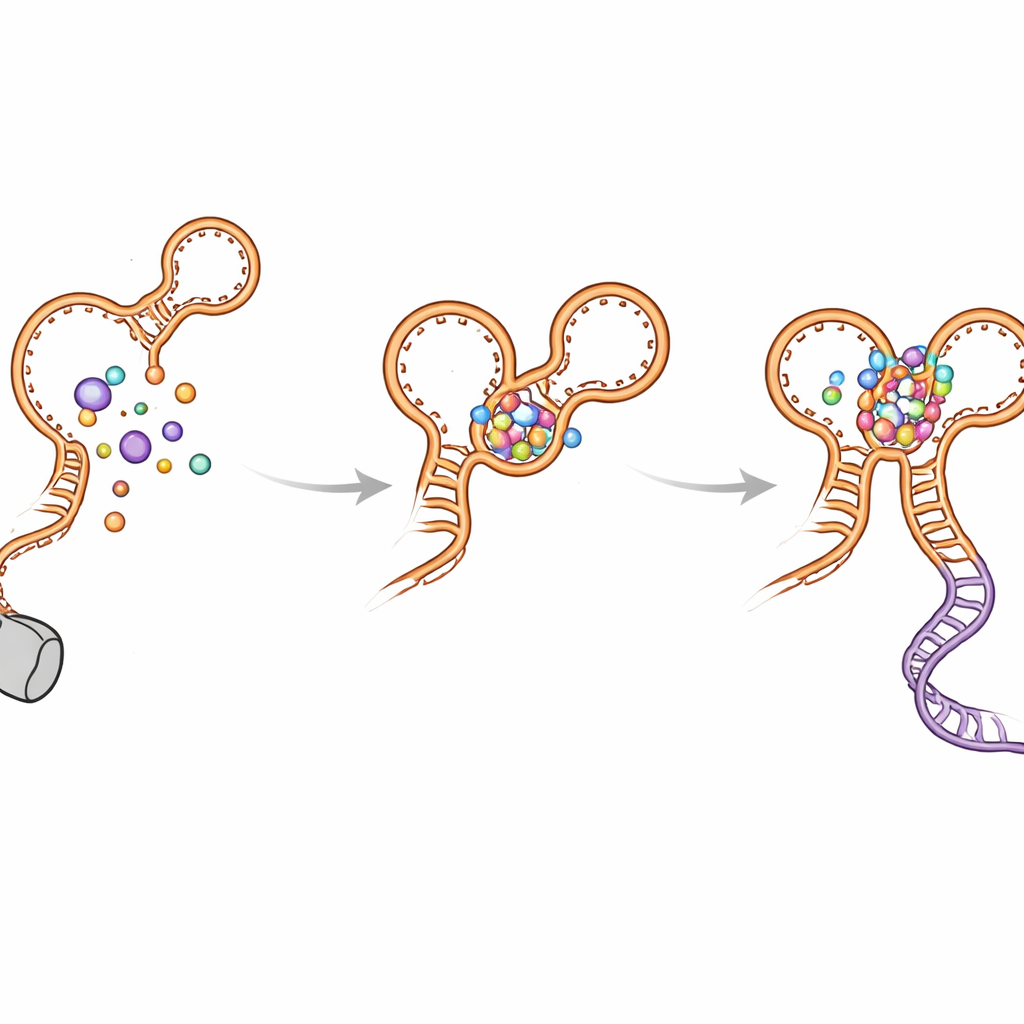
Z użyciem mikroskopii fluorescencji pojedynczych cząsteczek i wysokoprzepustowego sondowania chemicznego zespół wykazał, że ryboswitch nie działa w jednym „pstryknięciu”. Najpierw jony potasu stabilizują kink‑turn u podstawy RNA, ukierunkowując pierwszy aptamer w stronę rosnącego transkryptu. Następnie glicyna wiąże się z tym pierwszym aptamerem, utwierdzając jego lokalną strukturę. Te zdarzenia sprzyjają kontaktom dalekozasięgowym między dwoma aptamerami, które przygotowują oba miejsca wiążące glicynę jeszcze zanim pojawi się drugi ligand. W ostatecznej pauzie przy wbudowanej pętelce terminatora drugi cząsteczkę glicyny może związać się z niżej położonym aptamerem w tym preorganizowanym otoczeniu, a wydłużenie pauzy przez NusA dodatkowo sprzyja domknięciu tej zwartej, aktywnej konfiguracji.
Objazdy składania i jak przełącznik unika zablokowania
Autorzy odkryli także kilka tymczasowych pętelek „błędnego zakrętu”, które tworzą się w miarę wydłużania RNA. Te nienatywne struktury pojawiają się w obu aptamerach i mogą opóźniać powstanie ostatecznego, aktywnego kształtu. Helisa kink‑turn (nazwana P0) i kontakty między aptamerami pomagają rozwiązać te pośrednie formy i skierować składanie w stronę funkcjonalnego układu. Gdy P0 lub kluczowe punkty styku są zaburzone przez mutacje, ryboswitch traci dużą część swojej czułości i wydajności: glicyna nadal wiąże się, ale osłabione jest dokowanie dalekozasięgowe, helisa decyzyjna jest mniej stabilna, a przepływ transkryptu maleje. Symulacje komputerowe potwierdziły te obserwacje, pokazując, że ryboswitch jest znacznie bardziej zwarty i stabilny, gdy P0 i oba miejsca wiążące glicynę są nienaruszone.
Logika poza równowagą w żywych komórkach
W sumie wyniki wspierają obraz, w którym tandemowy ryboswitch glicynowy zachowuje się jak kinetyczna bramka logiczna, a nie prosty czujnik równowagowy. Zamiast obu cząsteczek glicyny wiążących się jednocześnie z gotową strukturą, wiązanie i składanie zachodzą w precyzyjnej sekwencji 5′→3′, sterowane pauzami transkrypcyjnymi i kształtowane przez jony potasu oraz białko NusA. Ten stopniowy, poza‑równowagą proces pozwala bakterii integrować kilka sygnałów — równowagę jonową komórki, poziom glicyny i prędkość transkrypcji — zanim zdecyduje, czy w pełni wyrazić geny rozkładające glicynę. Praca sugeruje, że taka kinetycznie napędzana kooperatywność może być ogólną strategią, dzięki której przełączniki RNA koordynują wiele czynników komórkowych, by precyzyjnie regulować ekspresję genów.
Cytowanie: Romero, R.A., Chauvier, A., Teh, S.S. et al. Co-transcriptional folding orchestrates sequential multi-effector sensing by a glycine tandem riboswitch. Nat Commun 17, 2779 (2026). https://doi.org/10.1038/s41467-026-69648-x
Słowa kluczowe: ryboswitch, wykrywanie glicyny, składanie RNA, zatrzymywanie transkrypcji, regulacja genów u bakterii