Clear Sky Science · zh
柯萨奇病毒样 IRES 类型中与 eIF4G 结合的 RNA 结构域的构象在拓扑上是保守的
某些病毒如何劫持我们的细胞
许多常见病毒——包括引起感冒、心脏炎症和肝炎的那些——都面临同样的基本难题:如何欺骗细胞制造病毒蛋白而不是自身蛋白。该研究以原子级细节揭示了病毒基因片段如何折叠成精确的三维构象,进而钩住宿主蛋白并启动病毒蛋白的合成。理解不同病毒中这种共享的结构伎俩,可能为开发针对多种病毒的广谱抗病毒药物提供思路。
蛋白质工厂的特殊入口
我们大多数的细胞信息(mRNA)都有一个化学“帽”,有助于招募细胞的蛋白合成机械。许多属於小 RNA 病毒科(Picornaviridae)的病毒缺少这种帽,但仍能劫持相同的机器。它们通过内源性核糖体进入位点(IRES)实现这一点——这是位於病毒基因组前端的有结构的 RNA 片段,作为核糖体的替代着陆点。在这些 IRES 区域内,有一段特定区段(在若干病毒中称为 V 区域)能强烈结合宿主的起始因子 eIF4G,eIF4G 可被视为一个支架,用以组织启动蛋白质合成所需的其他成分。
对病毒 RNA 结的高分辨率观察
作者解析了来自柯萨奇病毒 B3 的 V 区域的 3 埃晶体结构,该病毒常作为人肠道病毒的模型。该 RNA 并非简单的发夹,而是折叠成一个伸长的四向连接——想象两根叠置的长杆在中心与另一根短杆交叉,形成一个由富含腺嘌呤的环(A‑rich loop)维系的 H 形交叉结。这个紧凑的螺旋结将小的膨出和环以恰当角度排列,构成刚性的支架。溶液实验(包括小角 X 射线散射和化学足迹分析)以及现代结构预测工具共同表明,这一折叠并非结晶中的人工产物,而是 RNA 在水相中的真实构象。 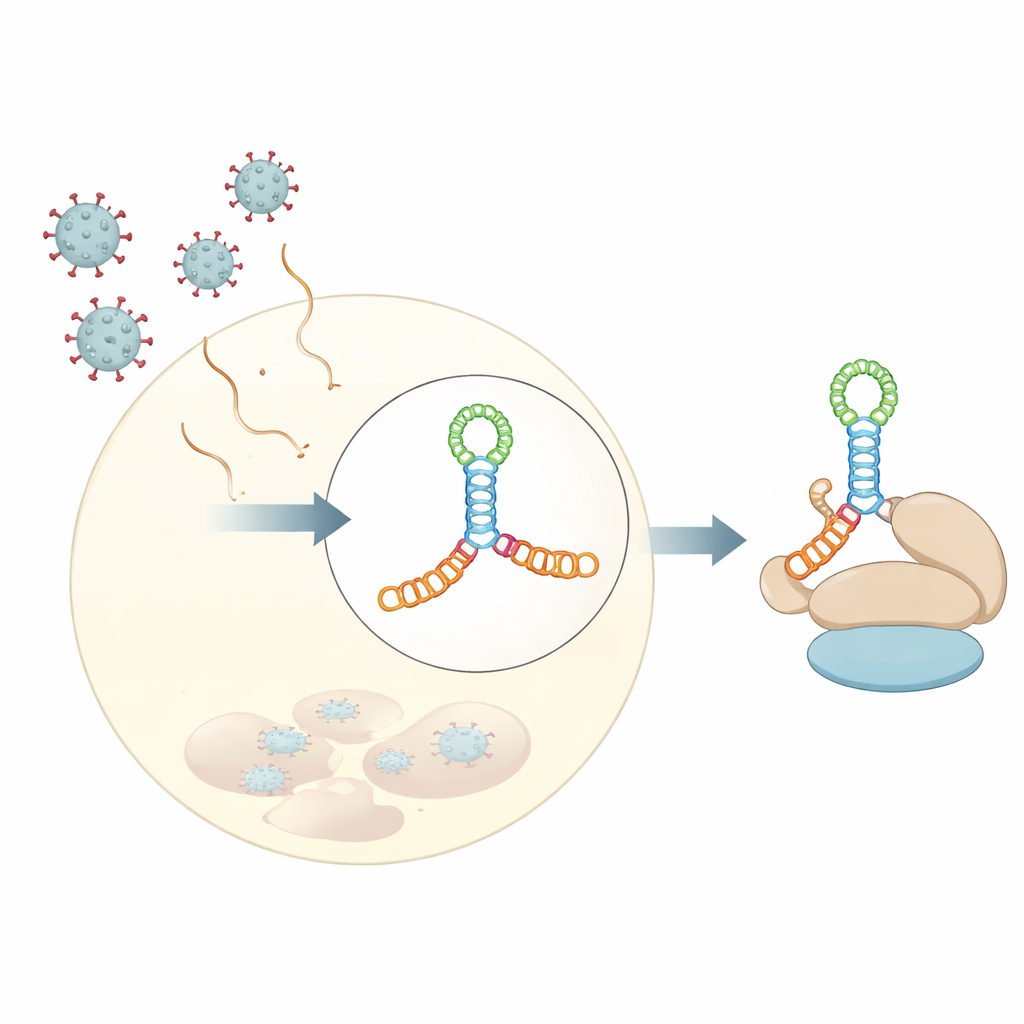
不同病毒,相同的结构蓝图
引人注目的是,当研究团队将此结构与此前解析的两种其他小 RNA 病毒的 RNA 片段——脑炎心肌炎病毒的 JK 区和甲型肝炎病毒的 V 区——进行比较时,发现总体三维拓扑几乎相同,尽管对应的 RNA 序列存在显著差异。在这三例中,一个富含腺嘌呤的环都嵌入附近螺旋的一侧,组织出一个紧凑的连接位点,使两条主要茎段叠置在一起。该重复出现的布局似乎是一种被进化反复利用的结构“基元”,能在序列和细节多变的情况下向宿主因子呈现熟悉的结合界面。
病毒折叠如何抓住宿主因子
为理解这一共同 RNA 构象如何捕获 eIF4G,研究者测量了病毒 RNA 与 eIF4G 的 HEAT1 区域之间的结合。HEAT1 是一段弯曲的模块,已知能接触 RNA。三种病毒的结构域都以纳摩尔亲和力结合 HEAT1,表明相当强的相互作用。通过在 RNA 的连接处和环上引入定点突变,他们能够减弱或消除结合,从而识别出关键特征。移除关键螺旋上的小膨出或破坏富 A 环的突变会大幅降低结合力,尽管这些被替换的核苷酸并不被预测会直接接触蛋白。这提示环和膨出作为内部支柱,固定叠置螺旋的相对取向,使得连续的侧面恰好呈现出适合 HEAT1 停靠的形状。 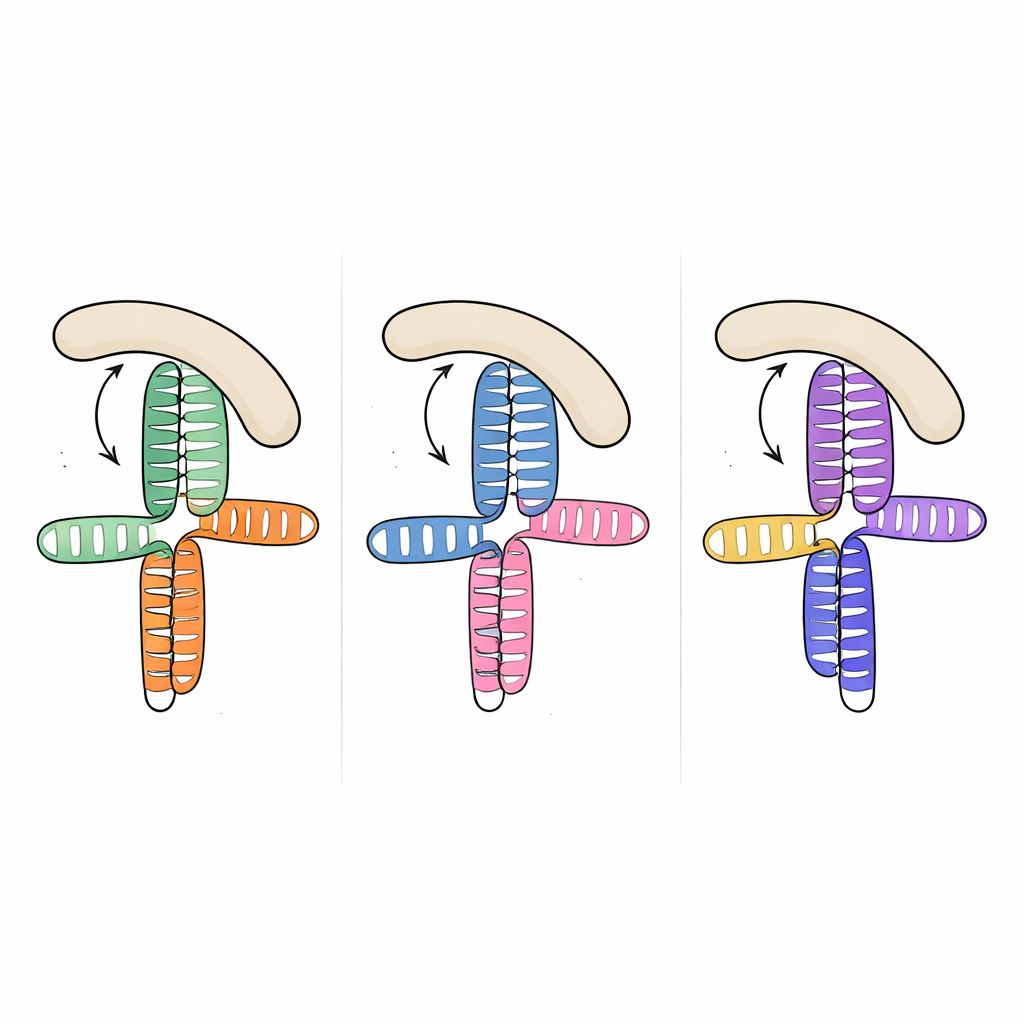
共同机制与新的药物可能性
化学“足迹”实验(绘制蛋白结合时 RNA 骨架受保护的区域)证实了 HEAT1 主要接触叠置螺旋的一侧,位於组织性富 A 环的对侧,这一接触方式与对另一种病毒的冷冻电镜观测非常相似。综合来看,该工作表明数种不同的柯萨奇科病毒使用一种共同的结构策略:它们构建相似的 RNA 支架,向同一宿主因子 eIF4G 呈现保守的三维特征,尽管序列本身各异。对非专业读者而言,结论是:来自家族不同分支的病毒会收敛到相同的折叠伎俩,从而接入细胞的翻译装置。由于这种伎俩依赖于形状多于序列,或许可以设计识别并破坏该保守 RNA 架构的药物或分子,从而用一种治疗阻断多种病毒的蛋白质生成。
引用: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
关键词: 病毒 RNA 结构, 内源性核糖体进入位点, eIF4G 结合, 小 RNA 病毒翻译, 广谱抗病毒药物