Clear Sky Science · nl
Structuren van de eIF4G-bindende RNA-domeinen tussen picornavirale IRES-typen zijn topologisch geconserveerd
Hoe bepaalde virussen onze cellen kapen
Veel veelvoorkomende virussen, waaronder die de verkoudheid, hartontsteking en hepatitis veroorzaken, staan voor dezelfde fundamentele uitdaging: hoe ze onze cellen ertoe kunnen brengen virale eiwitten te maken in plaats van de eigen eiwitten van de cel. Deze studie onthult, tot op atomaire details, hoe een essentieel stukje viraal genetisch materiaal zich vouwt tot een precieze driedimensionale vorm die zich vastgrijpt aan een gastheer-eiwit en de productie van virale eiwitten op gang brengt. Inzicht in deze gedeelde structurele truc over verschillende virussen heen kan de weg wijzen naar breedwerkzame antivirale middelen die ze tegelijk kunnen treffen.
Een speciale toegangspoort voor het eiwitfabriekje
De meeste van onze cellulaire boodschappen (mRNA’s) beginnen met een chemische "cap" die helpt bij het aantrekken van de eiwitsyntheserapparatuur van de cel. Veel RNA-virussen uit de familie Picornaviridae missen deze cap, maar weten toch hetzelfde machinerie te kapen. Ze doen dit met interne ribosoom-invoegsites, ofwel IRES-elementen—gestructureerde RNA-segmenten dicht bij het begin van het virale genoom die fungeren als alternatieve landingsplaatsen voor het ribosoom. Binnen deze IRES-regio’s bindt één specifieke sectie, aangeduid als domein V in meerdere virussen, sterk aan een gastheervoorinitiatiefactor genaamd eIF4G, een soort steiger die andere componenten organiseert die nodig zijn om de eiwitsynthese te starten.
Een hoogresolutieblik op een viraal RNA-knoop
De auteurs bepaalden een kristalstructuur van domein V van coxsackievirus B3 met 3-angstrom resolutie; dit virus wordt vaak gebruikt als model voor humane enterovirussen. In plaats van een eenvoudige haarspeldvouw vormt dit RNA een verlengde vierwegknoop—stel je twee gestapelde staven voor die een kortere staaf in het midden kruisen en zo een H-vormige verbinding vormen, bijeengehouden door een A-rijke lus. Deze compacte knoop van helices positioneert kleine uitstulpingen en lussen onder precies de juiste hoeken om een stijf raamwerk te vormen. Oplossingsexperimenten, waaronder small-angle X-ray scattering en chemische footprinting, samen met moderne structuurvoorspellingsmiddelen, toonden aan dat deze vouwing geen kristallisatieartefact is maar weerspiegelt hoe het RNA zich in oplossing gedraagt. 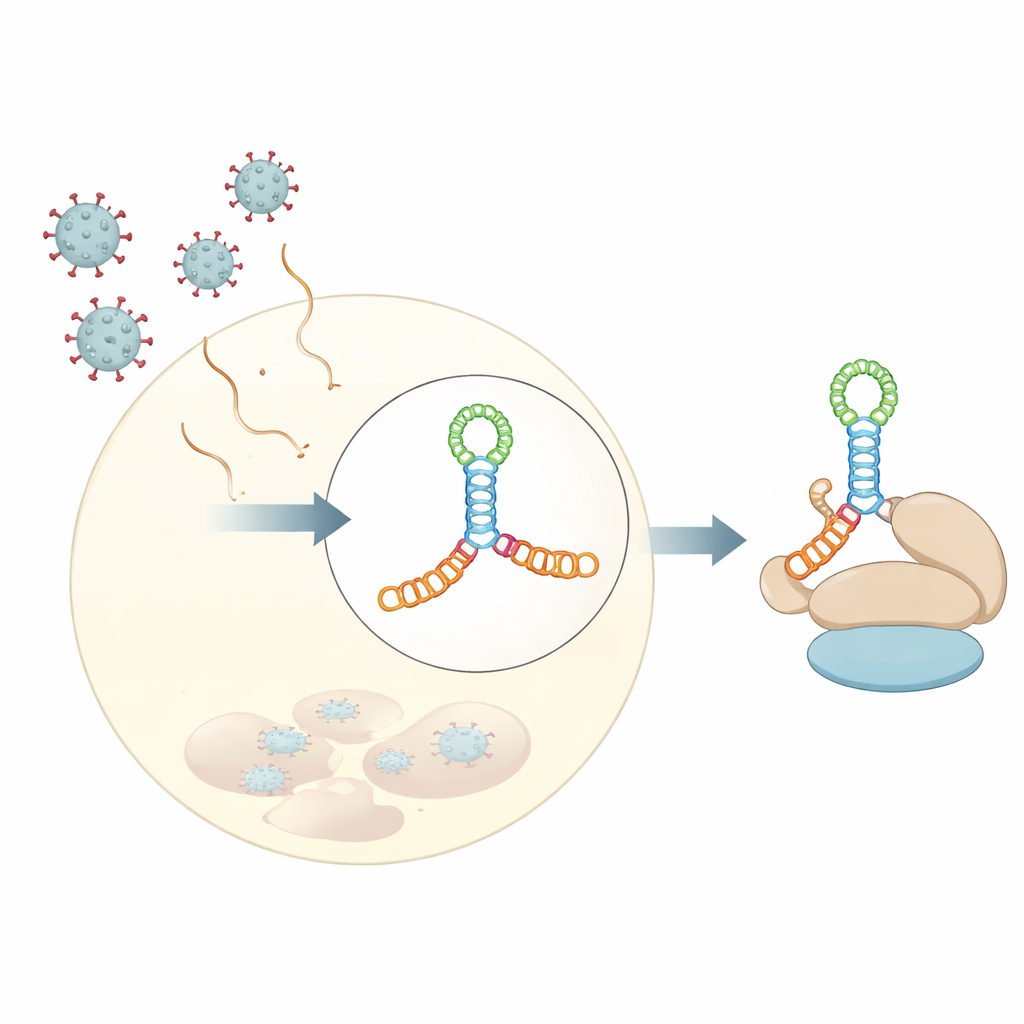
Verschillende virussen, hetzelfde structurele blauwdruk
Opmerkelijk was dat, toen het team deze structuur vergeleek met eerder gekarakteriseerde RNA-segmenten van twee andere picornavirussen—het JK-domein van het encefalomyocarditisvirus en domein V van het hepatitis A-virus—ze vonden dat de algemene driedimensionale topologie vrijwel hetzelfde is, hoewel de onderliggende RNA-sequenties sterk verschillen. In alle drie de gevallen klikt een A-rijke lus in de zijkant van een naburige helix en organiseert een compacte verbinding waarbij twee hoofdstrengen op elkaar gestapeld zijn. Deze terugkerende opstelling lijkt een structureel "motief" te zijn dat de evolutie hergebruikt heeft in verschillende virale soorten om gastheerfactoren een vertrouwd bindingsoppervlak te presenteren, ondanks grote variatie in sequentie en fijne details.
Hoe de virale vouwing een gastheerfactor grijpt
Om te begrijpen hoe deze gedeelde RNA-vorm eIF4G vangt, maten de onderzoekers de binding tussen de virale RNA’s en het HEAT1-gebied van eIF4G, een gebogen module waarvan bekend is dat die contact maakt met RNA. Alle drie de virale domeinen binden HEAT1 met nanomolaire affiniteit, wat zeer sterke interacties betekent. Door gerichte mutaties in de RNA-verbindingen en -lussen in te brengen, konden ze de binding verzwakken of elimineren en zo bepalen welke kenmerken het belangrijkst waren. Wijzigingen die kleine uitstulpingen in sleutelhelices verwijderden of de A-rijke lus verstoorden, verminderden de binding sterk, ook al worden de gemuteerde nucleotiden niet verwacht het eiwit direct te raken. Dit wijst erop dat de lus en de uitstulpingen fungeren als interne stijlen die de relatieve oriëntatie van de gestapelde helices fixeren zodat een continu lateraal oppervlak precies gevormd is voor HEAT1 om aan te hechten. 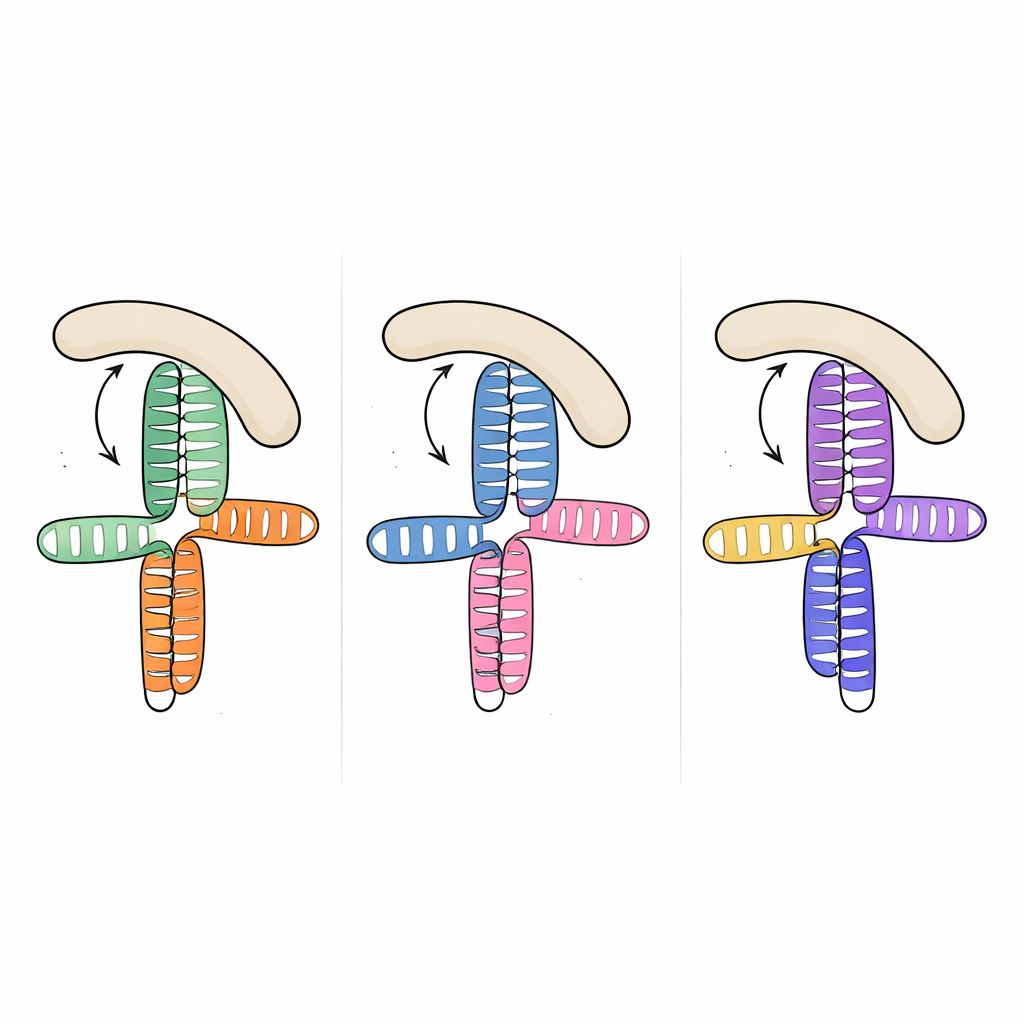
Gedeelde mechanismen en nieuwe medicijnmogelijkheden
Chemische footprinting-experimenten, die in kaart brengen welke delen van de RNA-ruggengraat beschermd zijn wanneer het eiwit gebonden is, bevestigden dat HEAT1 voornamelijk één zijde van de gestapelde helices raakt, tegenover de organiserende A-rijke lus, op een manier die sterk overeenkomt met cryo-elektronenmicroscopische waarnemingen voor één van de andere virussen. Samen laten de resultaten zien dat meerdere verschillende picornavirussen een gemeenschappelijke structurele strategie gebruiken: ze bouwen vergelijkbare RNA-steigers die geconserveerde driedimensionale kenmerken aan dezelfde gastheerfactor, eIF4G, presenteren, ondanks dat de sequenties zelf variëren. Voor de niet-specialist is de kernboodschap dat virussen uit verschillende takken van de familieboom convergeren op dezelfde vouwtruc om zich in het vertaalapparaat van de cel te pluggen. Omdat deze truc meer afhankelijk is van vorm dan van sequentie, kan het mogelijk zijn medicijnen of moleculen te ontwerpen die deze geconserveerde RNA-architectuur herkennen en uitschakelen, en zo de eiwitproductie bij meerdere virale soorten met één behandeling blokkeren.
Bronvermelding: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Trefwoorden: viraal RNA-structuur, intern ribosoom-invoegpunt, eIF4G-binding, picornavirusvertaling, breedwerkzame antivirale middelen