Clear Sky Science · sv
Strukturerna hos eIF4G‑bindande RNA‑domäner bland picornavirala IRES‑typer är topologiskt bevarade
Hur vissa virus kapar våra celler
Många vanliga virus, inklusive dem som orsakar förkylningar, hjärtinflammation och hepatit, står inför samma grundläggande problem: hur man lurar våra celler att producera virusproteiner istället för sina egna. Denna studie avslöjar, på atomär nivå, hur en nyckelbit av virusets genetiska material viks till en precis tredimensionell form som hakar fast vid ett värdprotein och startar produktionen av virusproteiner. Att förstå denna delade strukturella mekanism över olika virus kan peka mot bredspektriga antivirala läkemedel som riktar sig mot flera virus samtidigt.
En särskild ingång för cellens proteinmaskineri
De flesta av våra cellulära budbärare (mRNA) börjar med en kemisk ”mössa” som hjälper till att rekrytera cellens proteinsyntetiserande maskineri. Många RNA‑virus i familjen Picornaviridae saknar denna mössa, men lyckas ändå kapa samma maskineri. De gör detta med hjälp av interna ribosominträdesställen, eller IRES‑element—strukturerade RNA‑segment nära början av virusgenomet som fungerar som alternativa landningsplatser för ribosomen. Inom dessa IRES‑regioner binder en särskild sektion, kallad domän V i flera virus, starkt till en värdinitieringsfaktor som heter eIF4G, ett slags byggnadsställning som organiserar andra komponenter som behövs för att starta proteinsyntesen.
En högupplöst bild av en viral RNA‑knut
Författarna bestämde en 3‑ångströmers kristallstruktur av domän V från coxsackievirus B3, ett virus som ofta används som modell för humana enterovirus. Istället för att vara en enkel hårnål viks detta RNA till en förlängd fyrvägsförgrening—föreställ dig två staplade stavar som korsar en annan kort stav i mitten och bildar en H‑formad korsning hålls ihop av en A‑rik slinga. Denna kompakta knut av helixar placerar små bulor och slingor i precis rätt vinklar för att skapa en stel byggnadsställning. Lösningsexperiment, inklusive small‑angle X‑ray scattering och kemisk footprinting, tillsammans med moderna strukturprediktionsverktyg, visade att denna vikning inte är ett artefakt från kristalliseringen utan återspeglar hur RNA:t beter sig i lösning. 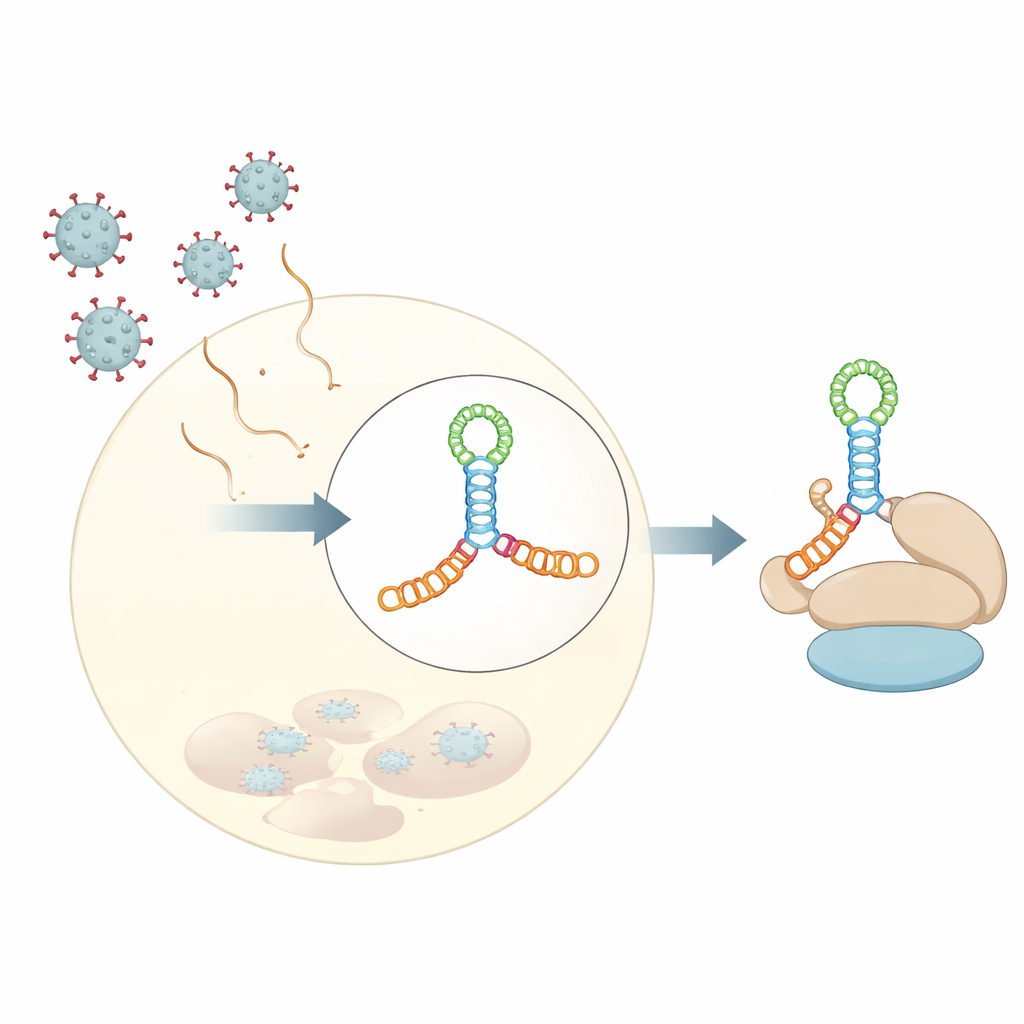
Olika virus, samma strukturella mall
Slående nog fann teamet, när de jämförde denna struktur med tidigare bestämda RNA‑segment från två andra picornavirus—JK‑domänen hos encefalomyokarditvirus och domän V hos hepatit A‑virus—att den övergripande tredimensionella topologin är nästan densamma, även om de underliggande RNA‑sekvenserna skiljer sig avsevärt. I alla tre fallen dockar en A‑rik slinga in i sidan av en närliggande helix och organiserar en kompakt korsning där två huvudstammar staplas ovanpå varandra. Detta återkommande upplägg verkar vara ett strukturellt ”motif” som evolutionen återanvänt över virusarter för att presentera värdfaktorer en välbekant bindningsyta, trots stor variation i sekvens och finare detaljer.
Hur den virala vikningen fångar en värdfaktor
För att förstå hur denna delade RNA‑form fångar eIF4G mätte forskarna bindningen mellan de virala RNA:na och HEAT1‑regionen av eIF4G, en krökt modul känd för att kontakta RNA. Alla tre virala domäner band HEAT1 med nanomolär affinitet, vilket innebär mycket täta interaktioner. Genom att införa riktade mutationer i RNA‑korsningarna och slingorna kunde de försvaga eller upphäva bindningen och se vilka egenskaper som spelade störst roll. Förändringar som tog bort små bulor i nyckelhelixar eller störde den A‑rika slingan minskade bindningen kraftigt, trots att de muterade nukleotiderna inte förväntas röra proteinet direkt. Detta tyder på att slingan och bulorna fungerar som interna stag, som fixerar den relativa orienteringen av de staplade helixarna så att en kontinuerlig lateral yta får precis rätt form för att HEAT1 ska kunna docka. 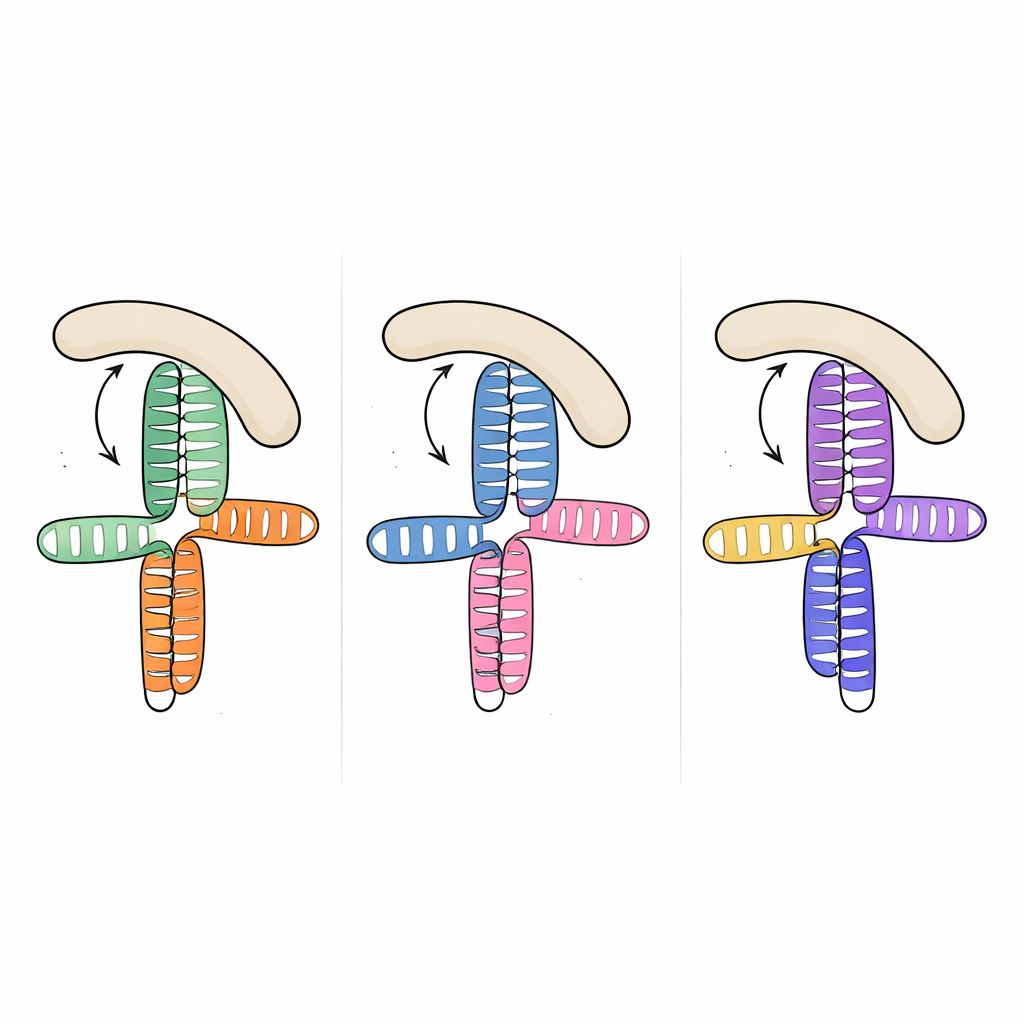
Delad mekanik och nya läkemedelsmöjligheter
Kemiska ”footprinting”‑experiment, som kartlägger vilka delar av RNA‑ryggraden som skyddas när proteinet är bundet, bekräftade att HEAT1 huvudsakligen kontaktar ena sidan av de staplade helixarna motsatt den organiserande A‑rika slingan, på ett sätt som nära speglar cryo‑elektronmikroskopiska observationer för ett av de andra virusen. Tillsammans visar arbetet att flera distinkta picornavirus använder en gemensam strukturell strategi: de bygger liknande RNA‑stativ som presenterar bevarade tredimensionella egenskaper för samma värdfaktor, eIF4G, även om sekvenserna varierar. För en icke‑specialist är slutsatsen att virus från olika grenar av familjeträdet konvergerar mot samma vikningstrick för att ansluta till cellens translationsmaskineri. Eftersom detta trick är mer beroende av form än av sekvens kan det vara möjligt att utforma läkemedel eller molekyler som känner igen och inaktiverar denna bevarade RNA‑arkitektur, vilket potentiellt blockerar proteinproduktion över flera virusarter med en enda behandling.
Citering: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Nyckelord: viralt RNA‑struktur, internt ribosominträde (IRES), eIF4G‑bindning, picornavirus‑translation, bredspektriga antivirala medel