Clear Sky Science · it
Le strutture dei domini di RNA che legano eIF4G nei tipi di IRES dei picornavirus sono conservate topologicamente
Come alcuni virus dirottano le nostre cellule
Molti virus comuni, compresi quelli che causano raffreddori, infiammazione cardiaca ed epatite, affrontano lo stesso problema fondamentale: come indurre le nostre cellule a produrre proteine virali invece delle proprie. Questo studio svela, a livello atomico, come un elemento chiave del materiale genetico virale si ripiega in una precisa forma tridimensionale che si aggancia a una proteina ospite e avvia la produzione di proteine virali. Comprendere questo trucco strutturale condiviso tra diversi virus potrebbe indicare la strada verso antivirali ad ampio spettro che li prendano di mira simultaneamente.
Un ingresso speciale per la fabbrica di proteine
La maggior parte dei nostri messaggi cellulari (mRNA) comincia con una “cap” chimica che aiuta a reclutare la macchina cellulare per la sintesi proteica. Molti virus a RNA della famiglia Picornaviridae non possiedono questa cap, eppure riescono comunque a impadronirsi della stessa macchina. Lo fanno usando siti di ingresso ribosomiale interno, o elementi IRES—segmenti di RNA strutturato vicino all’inizio del genoma virale che fungono da punti di atterraggio alternativi per il ribosoma. All’interno di queste regioni IRES, una specifica sezione, chiamata dominio V in diversi virus, lega con forza un fattore di inizio ospite denominato eIF4G, una sorta di impalcatura che organizza gli altri componenti necessari per avviare la sintesi proteica.
Uno sguardo ad alta risoluzione a un nodo di RNA virale
Gli autori hanno determinato una struttura cristallina a 3 angstrom del dominio V del coxsackievirus B3, un virus spesso usato come modello per gli enterovirus umani. L’RNA non forma un semplice forcina, ma si piega in una giunzione allungata a quattro bracci—immaginate due aste impilate che incrociano un’altra asta corta al centro, formando una giunzione a forma di H tenuta insieme da un anello ricco di adenine. Questo nodo compatto di eliche posiziona rigonfiamenti e anellini negli angoli giusti per creare un’impalcatura rigida. Esperimenti in soluzione, inclusi scattering a piccolo angolo dei raggi X e impronte chimiche, insieme a strumenti moderni di predizione strutturale, hanno mostrato che questo ripiegamento non è un artefatto della cristallizzazione ma riflette il comportamento dell’RNA in acqua. 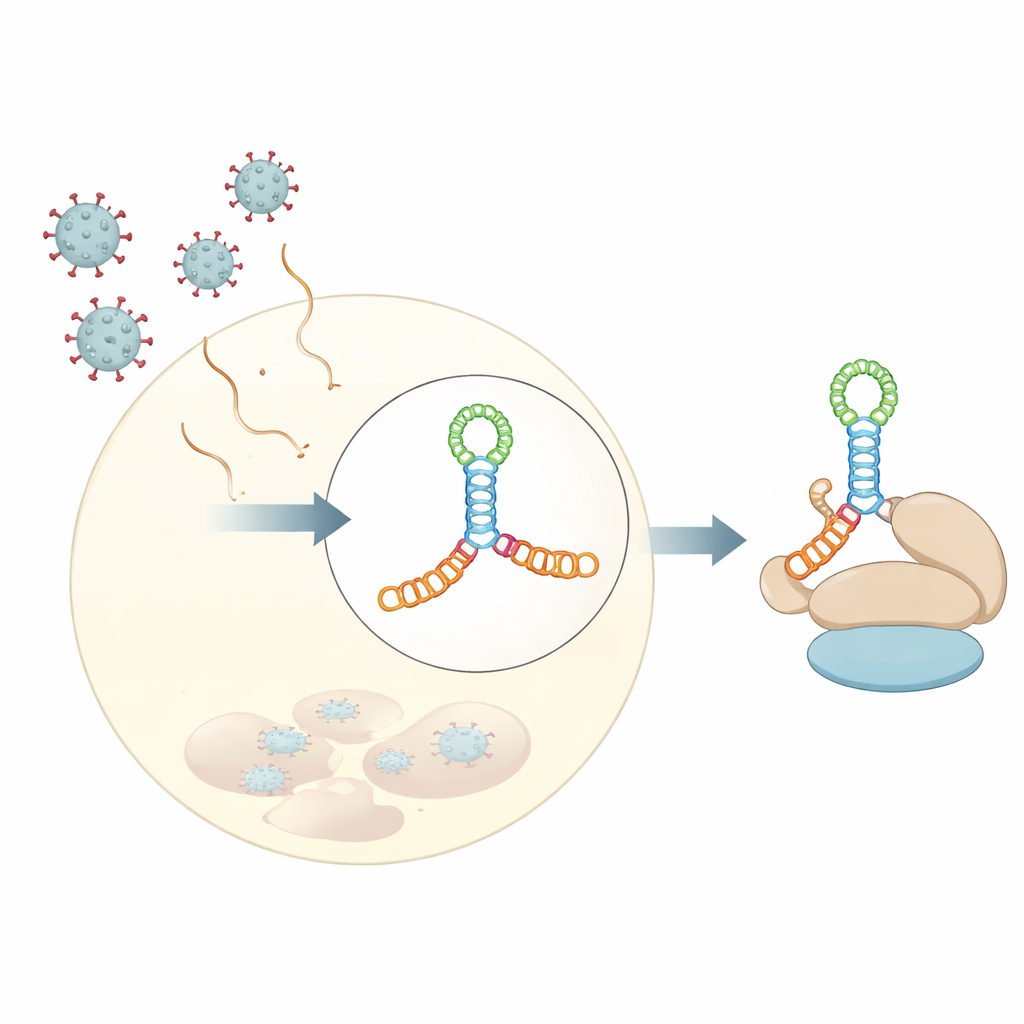
Virus diversi, stesso progetto strutturale
In modo notevole, quando il gruppo ha confrontato questa struttura con segmenti di RNA risolti in precedenza di altri due picornavirus—il dominio JK del virus encefalomiosi cardiaca e il dominio V del virus dell’epatite A—ha scoperto che la topologia tridimensionale complessiva è quasi la stessa, nonostante le sequenze di RNA sottostanti differiscano considerevolmente. In tutti e tre i casi, un anello ricco di adenine si incastra sul fianco di un’elica vicina e organizza una giunzione compatta dove due steli principali si impilano l’uno sull’altro. Questo layout ricorrente sembra essere un “motivo” strutturale che l’evoluzione ha riutilizzato tra specie virali per presentare ai fattori ospiti una superficie di legame familiare, malgrado l’ampia variazione di sequenza e dettagli fini.
Come il ripiegamento virale cattura un fattore ospite
Per capire come questa forma di RNA condivisa catturi eIF4G, i ricercatori hanno misurato il legame tra gli RNA virali e la regione HEAT1 di eIF4G, un modulo curvo noto per contattare l’RNA. Tutti e tre i domini virali hanno legato HEAT1 con affinità nanomolare, ossia interazioni molto strette. Introducendo mutazioni mirate nelle giunzioni e negli anelli dell’RNA, hanno potuto indebolire o abolire il legame e identificare quali caratteristiche fossero più importanti. Mutazioni che rimuovevano piccoli rigonfiamenti in eliche chiave o interrompevano l’anello ricco di adenine hanno ridotto fortemente il legame, nonostante i nucleotidi mutati non siano previsti entrare in contatto diretto con la proteina. Ciò suggerisce che l’anello e i rigonfiamenti agiscano come puntelli interni, fissando l’orientamento relativo delle eliche impilate in modo che una superficie laterale continua sia perfettamente sagomata per l’atterraggio di HEAT1. 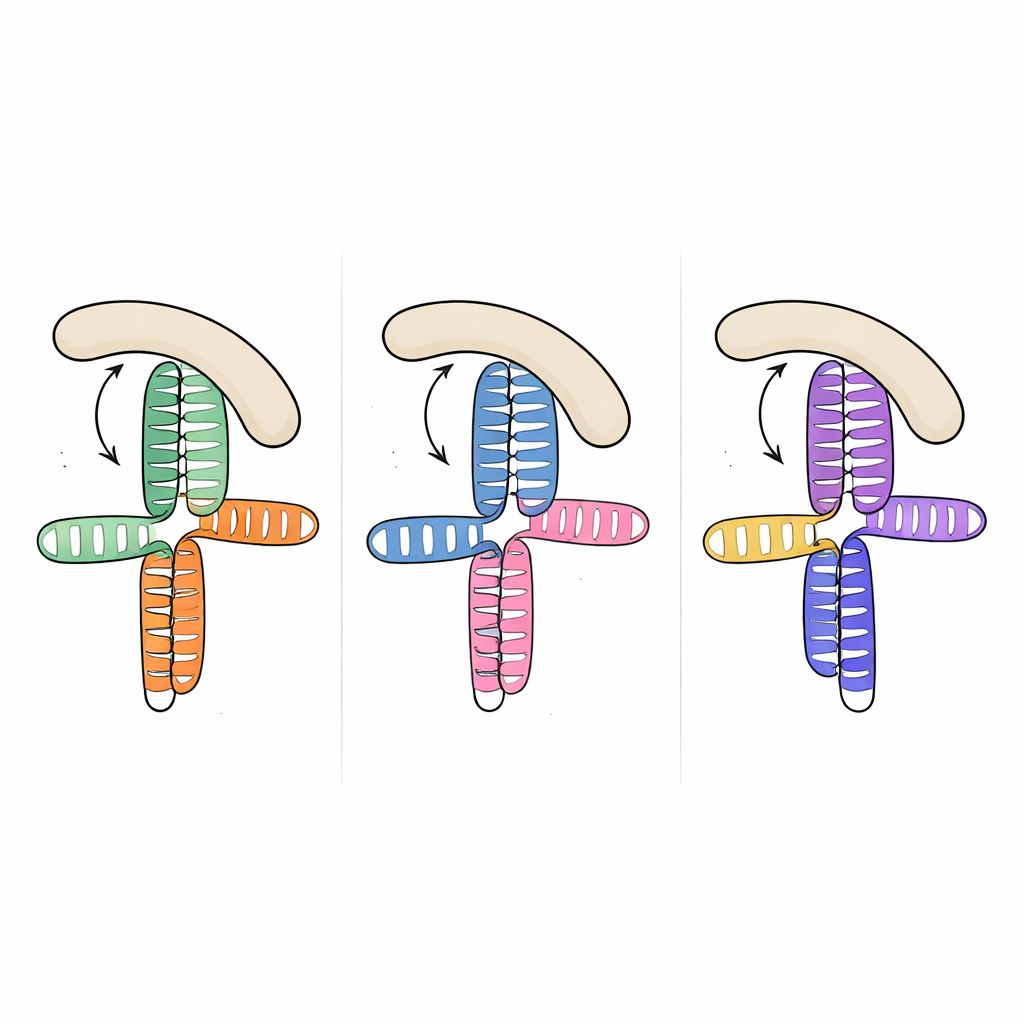
Meccanismi condivisi e nuove possibilità terapeutiche
Esperimenti di “footprinting” chimico, che mappano quali parti dello scheletro dell’RNA sono protette quando la proteina è legata, hanno confermato che HEAT1 contatta principalmente un lato delle eliche impilate opposto all’anello organizzatore ricco di adenine, in un modo che rispecchia da vicino osservazioni ottenute con crio‑microscopia elettronica per uno degli altri virus. Nel complesso, il lavoro mostra che diversi picornavirus distinti impiegano una strategia strutturale comune: costruiscono impalcature di RNA simili che presentano caratteristiche tridimensionali conservate allo stesso fattore ospite, eIF4G, nonostante le sequenze varino. Per un pubblico non specialistico, la conclusione è che virus da rami diversi dell’albero filogenetico convergono sullo stesso trucco di ripiegamento per collegarsi all’apparato di traduzione della cellula. Poiché questo trucco dipende più dalla forma che dalla sequenza, potrebbe essere possibile progettare farmaci o molecole che riconoscano e disabilitino questa architettura di RNA conservata, bloccando potenzialmente la produzione proteica in più specie virali con un singolo trattamento.
Citazione: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Parole chiave: struttura dell'RNA virale, sito di ingresso ribosomiale interno, legame con eIF4G, traduzione dei picornavirus, antivirali ad ampio spettro