Clear Sky Science · es
Las estructuras de los dominios de ARN que se unen a eIF4G entre los tipos de IRES picornavíricos están conservadas topológicamente
Cómo ciertos virus secuestran nuestras células
Muchos virus comunes, incluidos los que causan resfriados, inflamación del corazón y hepatitis, enfrentan el mismo desafío básico: cómo engañar a nuestras células para que produzcan proteínas virales en lugar de las propias. Este estudio desvela, con detalle atómico, cómo un fragmento clave del material genético viral se pliega en una forma tridimensional precisa que se engancha a una proteína hospedadora y pone en marcha la producción de proteínas virales. Comprender este truco estructural compartido entre distintos virus podría señalar la vía hacia antivirales de amplio espectro que los apunten a todos a la vez.
Un punto de entrada especial para la fábrica de proteínas
La mayoría de nuestros mensajes celulares (ARNm) comienzan con una “cap” química que ayuda a reclutar la maquinaria celular de síntesis de proteínas. Muchos virus ARN de la familia Picornaviridae carecen de esa cap, y aun así logran apropiarse de la misma maquinaria. Lo hacen mediante sitios internos de entrada del ribosoma, o elementos IRES: segmentos de ARN estructurado cerca del inicio del genoma viral que sirven como plataformas alternativas para que se ancle el ribosoma. Dentro de estas regiones IRES, una sección particular, llamada dominio V en varios virus, se une con fuerza a un factor de iniciación hospedador llamado eIF4G, una especie de armazón que organiza otros componentes necesarios para comenzar la síntesis proteica.
Una vista de alta resolución de un nudo de ARN viral
Los autores determinaron una estructura cristalina a 3 angstroms del dominio V de coxsackievirus B3, un virus empleado a menudo como modelo de los enterovirus humanos. En lugar de ser un simple horquillado, este ARN se pliega en una unión elongada de cuatro vías: imagina dos varillas apiladas que cruzan otra varilla corta en el centro, formando una unión en forma de H sostenida por un lazo rico en adeninas. Este nudo compacto de hélices posiciona protuberancias y bucles pequeños en ángulos precisos para formar un andamiaje rígido. Experimentos en solución, incluidos dispersión de rayos X a pequeña escala y huellas químicas, junto con herramientas modernas de predicción estructural, mostraron que este plegamiento no es un artefacto de la cristalización sino que refleja el comportamiento del ARN en agua. 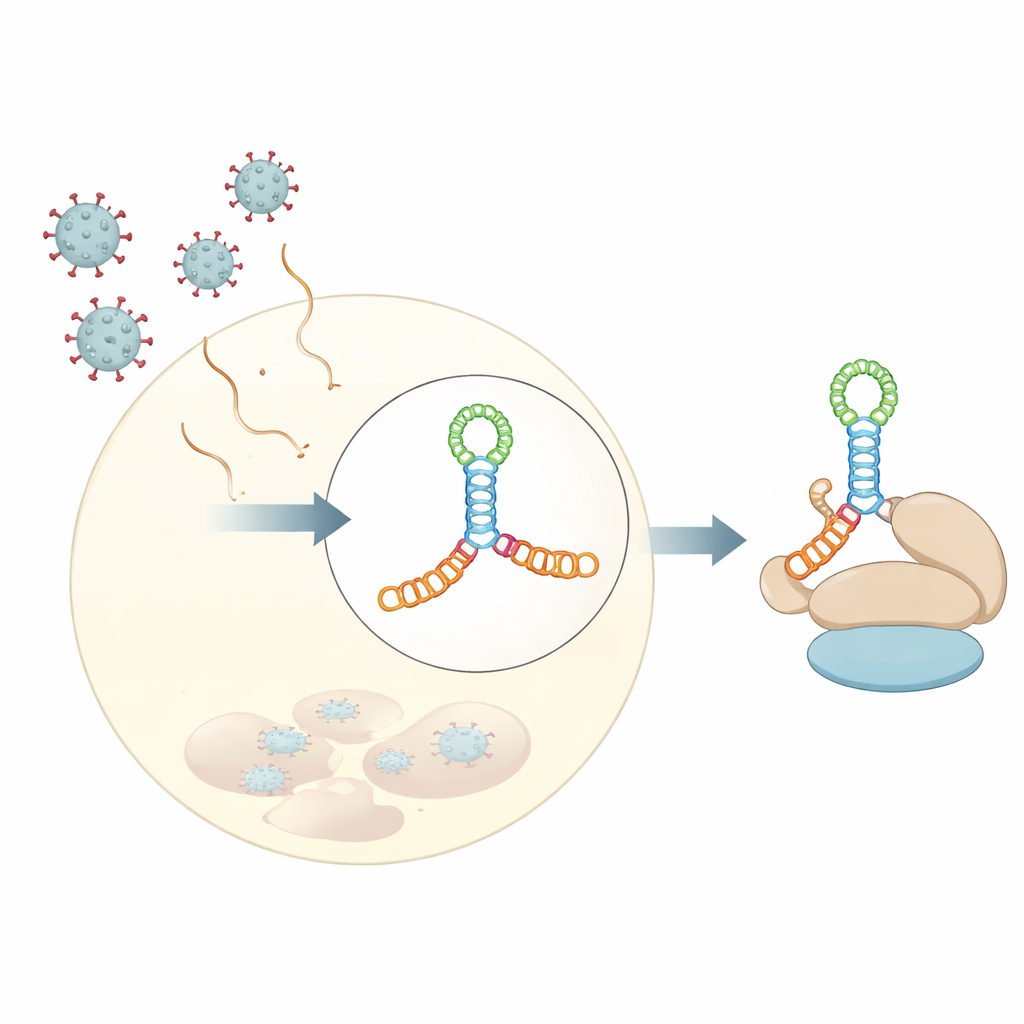
Diferentes virus, el mismo plano estructural
De manera llamativa, cuando el equipo comparó esta estructura con segmentos de ARN resueltos previamente de otros dos picornavirus —el dominio JK del virus de la encefalomiocarditis y el dominio V del virus de la hepatitis A— encontraron que la topología tridimensional general es casi la misma, a pesar de que las secuencias de ARN subyacentes difieren considerablemente. En los tres casos, un lazo rico en adeninas se acopla en el lateral de una hélice cercana y organiza una unión compacta donde dos tallos principales se apilan uno sobre otro. Este diseño recurrente parece ser un “motivo” estructural que la evolución ha reutilizado entre especies virales para presentar a los factores hospedadores una superficie de unión familiar, pese a la gran variación en la secuencia y los detalles finos.
Cómo el plegamiento viral atrapa un factor hospedador
Para entender cómo esta forma de ARN compartida captura a eIF4G, los investigadores midieron la unión entre los ARN virales y la región HEAT1 de eIF4G, un módulo curvado conocido por contactar ARN. Los tres dominios virales se unieron a HEAT1 con afinidad en el rango nanomolar, lo que indica interacciones muy fuertes. Al introducir mutaciones dirigidas en las uniones y bucles del ARN, pudieron debilitar o abolir la unión y así identificar qué características importaban más. Los cambios que eliminaron pequeñas protuberancias en hélices clave o que alteraron el lazo rico en adeninas redujeron drásticamente la unión, aunque los nucleótidos mutados no se predicen como puntos de contacto directo con la proteína. Esto sugiere que el lazo y las protuberancias actúan como puntales internos, fijando la orientación relativa de las hélices apiladas para que una superficie lateral continua tenga la forma perfecta para que HEAT1 se acople. 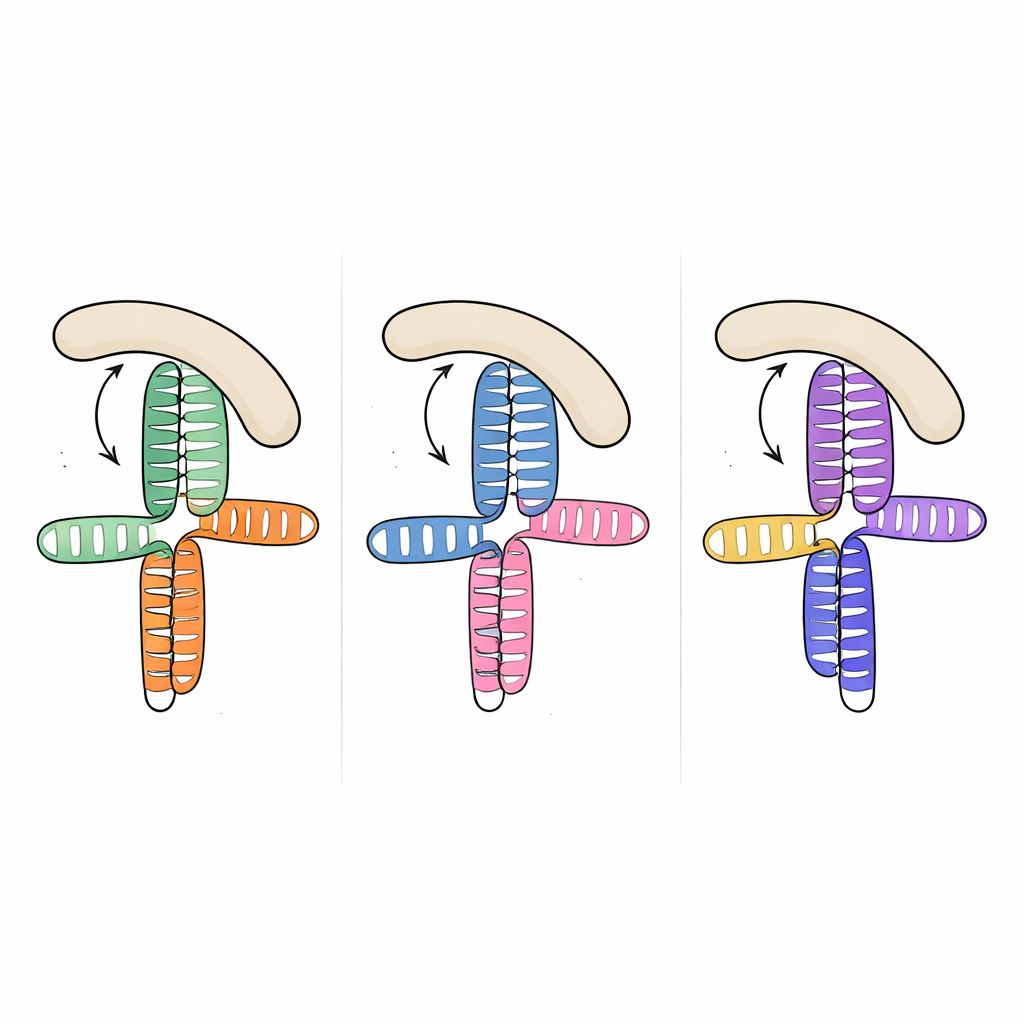
Mecánica compartida y nuevas posibilidades terapéuticas
Experimentos de “huella química”, que mapean qué partes de la columna vertebral del ARN quedan protegidas cuando la proteína está unida, confirmaron que HEAT1 contacta principalmente un lado de las hélices apiladas opuesto al lazo organizador rico en adeninas, de una manera que refleja de cerca observaciones por criomicroscopía electrónica para uno de los otros virus. En conjunto, el trabajo muestra que varios picornavirus distintos utilizan una estrategia estructural común: construyen andamiajes de ARN similares que presentan características tridimensionales conservadas al mismo factor hospedador, eIF4G, aunque las secuencias varíen. Para un público no especialista, la conclusión es que virus procedentes de diferentes ramas del árbol evolutivo convergen en el mismo truco de plegamiento para conectarse al mecanismo de traducción celular. Dado que este truco depende más de la forma que de la secuencia, podría ser posible diseñar fármacos o moléculas que reconozcan y desactiven esta arquitectura de ARN conservada, bloqueando potencialmente la producción de proteínas en múltiples especies virales con un único tratamiento.
Cita: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Palabras clave: estructura del ARN viral, sitio interno de entrada del ribosoma, unión a eIF4G, traducción de picornavirus, antivirales de amplio espectro