Clear Sky Science · pl
Struktury domen RNA wiążących eIF4G w typach IRES pikornawirusów są topologicznie zachowane
Jak niektóre wirusy przejmują nasze komórki
Wiele powszechnych wirusów, w tym te wywołujące przeziębienia, zapalenie mięśnia sercowego i zapalenie wątroby, stoi przed tym samym podstawowym wyzwaniem: jak oszukać komórki, by produkowały białka wirusowe zamiast własnych. W badaniu tym ujawniono w atomowych szczegółach, jak kluczowy fragment materiału genetycznego wirusa składa się w precyzyjną trójwymiarową strukturę, która przyczepia się do białka gospodarza i uruchamia produkcję białek wirusowych. Zrozumienie tego wspólnego trików strukturalnego obecnego w różnych wirusach może wskazać drogę do leków przeciwwirusowych o szerokim spektrum, które mogłyby je wszystkie jednocześnie zaatakować.
Szczególne wejście do fabryki białek
Większość naszych komórkowych komunikatów (mRNA) zaczyna się chemiczną „czapką”, która pomaga przyciągać mechanizmy tworzenia białek. Wiele wirusów RNA z rodziny Picornaviridae pozbawionych jest tej czapki, a mimo to potrafi przejąć te same mechanizmy. Robią to za pomocą wewnętrznych miejsc wejścia rybosomu, czyli elementów IRES — strukturalnych fragmentów RNA blisko początku genomu wirusowego, które służą jako alternatywne platformy dla rybosomu. W obrębie tych regionów IRES jedną szczególną sekcję, nazwaną domeną V w kilku wirusach, silnie wiąże czynnik inicjacji gospodarza o nazwie eIF4G — swego rodzaju stelaż organizujący inne składniki potrzebne do rozpoczęcia syntezy białka.
Wysokorozdzielczy obraz węzła RNA wirusa
Autorzy ustalili strukturę krystaliczną domeny V wirusa Coxsackievirus B3 o rozdzielczości 3 Å. Zamiast prostego szypułkowego pętelki RNA układa się w wydłużone, czterodrożne złącze — wyobraź sobie dwa nałożone pręty przecinające krótki pręt w środku, tworząc skrzyżowanie w kształcie litery H utrzymane przez bogatą w adeniny pętlę. Ten zwarty splot helis ustawia małe wybrzuszenia i pętle pod odpowiednimi kątami, tworząc sztywny stelaż. Eksperymenty w roztworze, w tym skattering małych kątów promieniowania rentgenowskiego (SAXS) oraz mapowanie chemiczne, wraz z nowoczesnymi narzędziami do przewidywania struktur, pokazały, że to sfałdowanie nie jest artefaktem krystalizacji, lecz odzwierciedla zachowanie RNA w wodzie. 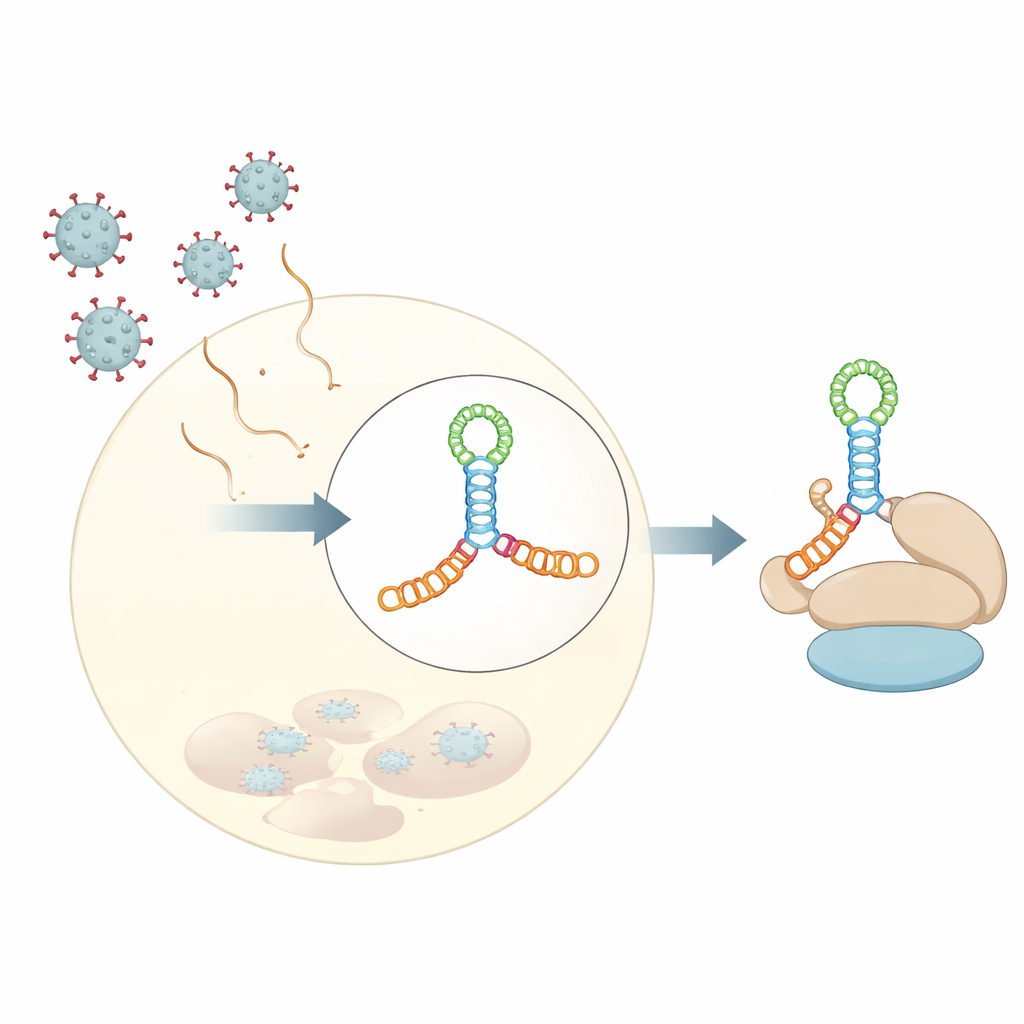
Różne wirusy, ten sam plan strukturalny
Zaskakująco, gdy zespół porównał tę strukturę z wcześniej rozwiązanymi fragmentami RNA z dwóch innych pikornawirusów — domeną JK wirusa zapalenia mózgu i mięśnia sercowego (encephalomyocarditis virus) oraz domeną V wirusa zapalenia wątroby typu A — okazało się, że ogólna topologia trójwymiarowa jest niemal identyczna, mimo znacznych różnic w sekwencjach RNA. We wszystkich trzech przypadkach bogata w adeniny pętla wsuwa się w bok pobliskiej helisy i organizuje zwartą strefę, w której dwie główne łodygi ustawiają się jedna na drugiej. Powtarzający się układ wydaje się być motywem strukturalnym, którego ewolucja wielokrotnie użyła w różnych gatunkach wirusów, by zaprezentować czynnikom gospodarza znajome miejsce wiązania, pomimo dużej zmienności sekwencji i drobnych różnic.
Jak wirusowe sfałdowanie łapie czynnik gospodarza
Aby zrozumieć, jak wspólny kształt RNA chwyta eIF4G, badacze zmierzyli wiązanie między wirusowymi RNA a regionem HEAT1 eIF4G — zakrzywionym modułem znanym z kontaktów z RNA. Wszystkie trzy domeny wirusowe wiązały HEAT1 z powinowactwem w zakresie nanomolarnym, co oznacza bardzo silne interakcje. Wprowadzając ukierunkowane mutacje w złączach i pętlach RNA, mogli osłabić lub znieść wiązanie i sprawdzić, które elementy mają największe znaczenie. Zmiany usuwające małe wybrzuszenia w kluczowych helisach lub zakłócające pętlę bogatą w adeniny znacznie ograniczały wiązanie, mimo że zmienione nukleotydy nie są przewidywane jako bezpośrednio stykające się z białkiem. Sugeruje to, że pętla i wybrzuszenia działają jak wewnętrzne dźwigary, ustalając względną orientację nałożonych helis tak, że ciągła powierzchnia boczna jest idealnie ukształtowana do zadokowania HEAT1. 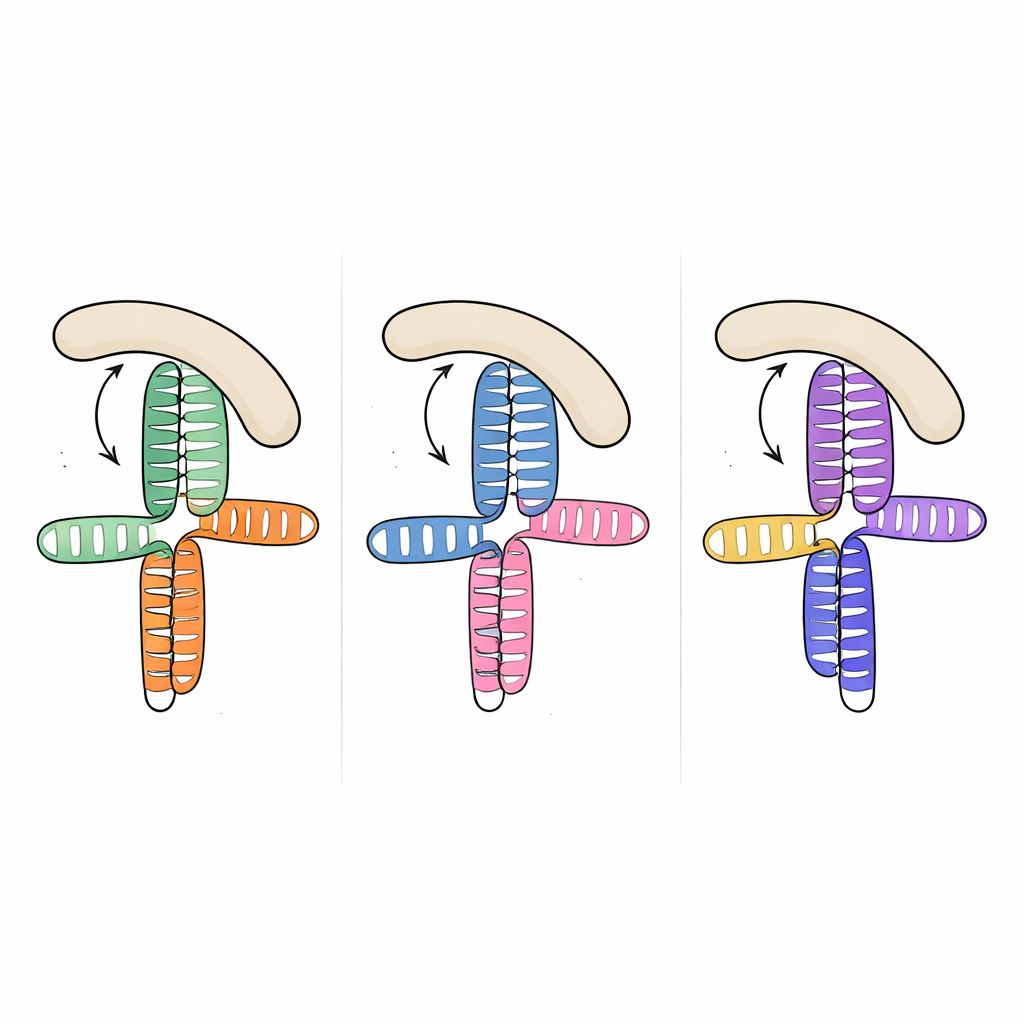
Wspólne mechanizmy i nowe możliwości terapeutyczne
Doświadczenia „mapowania” chemicznego, które określają, które części szkieletonu RNA są chronione po przyłączeniu białka, potwierdziły, że HEAT1 kontaktuje się głównie z jedną stroną ułożonych helis po przeciwnej stronie od organizującej pętli bogatej w adeniny, w sposób bardzo podobny do obserwacji z mikroskopii krioelektronowej dla jednego z innych wirusów. Razem praca ta pokazuje, że kilka różnych pikornawirusów wykorzystuje wspólną strategię strukturalną: buduje podobne rusztowania RNA, które prezentują zachowane cechy trójwymiarowe temu samemu czynnikowi gospodarza, eIF4G, mimo że same sekwencje się różnią. Dla czytelnika niebędącego specjalistą kluczowa wiadomość jest taka, że wirusy z różnych gałęzi drzewa rodowego zbieżają do tego samego triku składania, by wpiąć się w maszynerię translacyjną komórki. Ponieważ ten mechanizm zależy bardziej od kształtu niż od sekwencji, możliwe jest zaprojektowanie leków lub cząsteczek rozpoznających i unieruchamiających tę zachowaną architekturę RNA, co potencjalnie zablokowałoby produkcję białek w wielu gatunkach wirusów jednym lekiem.
Cytowanie: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Słowa kluczowe: struktura RNA wirusa, wewnętrzne miejsce wejścia rybosomu, wiązanie eIF4G, translacja pikornawirusów, leki przeciwwirusowe o szerokim spektrum