Clear Sky Science · de
Topologisch konservierte Strukturen der eIF4G‑bindenden RNA‑Domänen zwischen Picornavirus‑IRES‑Typen
Wie bestimmte Viren unsere Zellen kapern
Viele verbreitete Viren, darunter solche, die Erkältungen, Herzmuskelentzündungen und Hepatitis verursachen, stehen vor derselben Grundaufgabe: Wie bringen sie unsere Zellen dazu, virale Proteine statt der eigenen zu produzieren? Diese Studie zeigt im atomaren Detail, wie ein Schlüsselabschnitt des viralen genetischen Materials sich zu einer präzisen dreidimensionalen Form faltet, die an ein Wirtsprotein andockt und die Produktion viraler Proteine in Gang setzt. Das Verständnis dieses gemeinsamen strukturellen Tricks über verschiedene Viren hinweg könnte den Weg zu Breitband‑Antiviralia weisen, die mehrere Erreger gleichzeitig angreifen.
Ein spezieller Zugangspunkt für die Proteinfabrik
Die meisten unserer zellulären Nachrichten (mRNAs) beginnen mit einer chemischen „Kappe“, die hilft, die zelluläre Proteinsynthese auszurichten. Viele RNA‑Viren der Familie Picornaviridae besitzen diese Kappe nicht, schaffen es aber dennoch, dieselben zellulären Maschinen zu übernehmen. Sie nutzen dafür sogenannte interne Ribosomen‑Einstiegsstellen (IRES) — strukturierte RNA‑Segmente nahe dem Beginn des viralen Genoms, die dem Ribosom alternative Andockplätze bieten. Innerhalb dieser IRES‑Regionen bindet ein bestimmter Abschnitt, in mehreren Viren als Domäne V bezeichnet, stark an einen Wirtsinitiationsfaktor namens eIF4G, einen Art Gerüst, das andere Komponenten organisiert, die zum Start der Proteinsynthese nötig sind.
Ein hochaufgelöster Blick auf einen viralen RNA‑Knoten
Die Autoren bestimmten eine Kristallstruktur von Domäne V des Coxsackievirus B3 mit 3 Å Auflösung. Anstatt eines einfachen Haarnadels faltet sich diese RNA zu einer verlängerten vierarmigen Verzweigung – man kann sich zwei gestapelte Stäbe vorstellen, die in der Mitte einen kürzeren Stab kreuzen und so eine H‑förmige Verbindung bilden, zusammengehalten von einer A‑reichen Schleife. Dieser kompakte Knoten von Helices positioniert kleine Ausbuchtungen und Schleifen in genau den richtigen Winkeln und bildet ein starres Gerüst. Lösungsbasierte Experimente, darunter Kleinwinkel‑Röntgenstreuung und chemische Footprinting‑Analysen, zusammen mit modernen Strukturvorhersagewerkzeugen, zeigten, dass diese Faltung kein Kristallisationsartefakt ist, sondern das Verhalten der RNA in Lösung widerspiegelt. 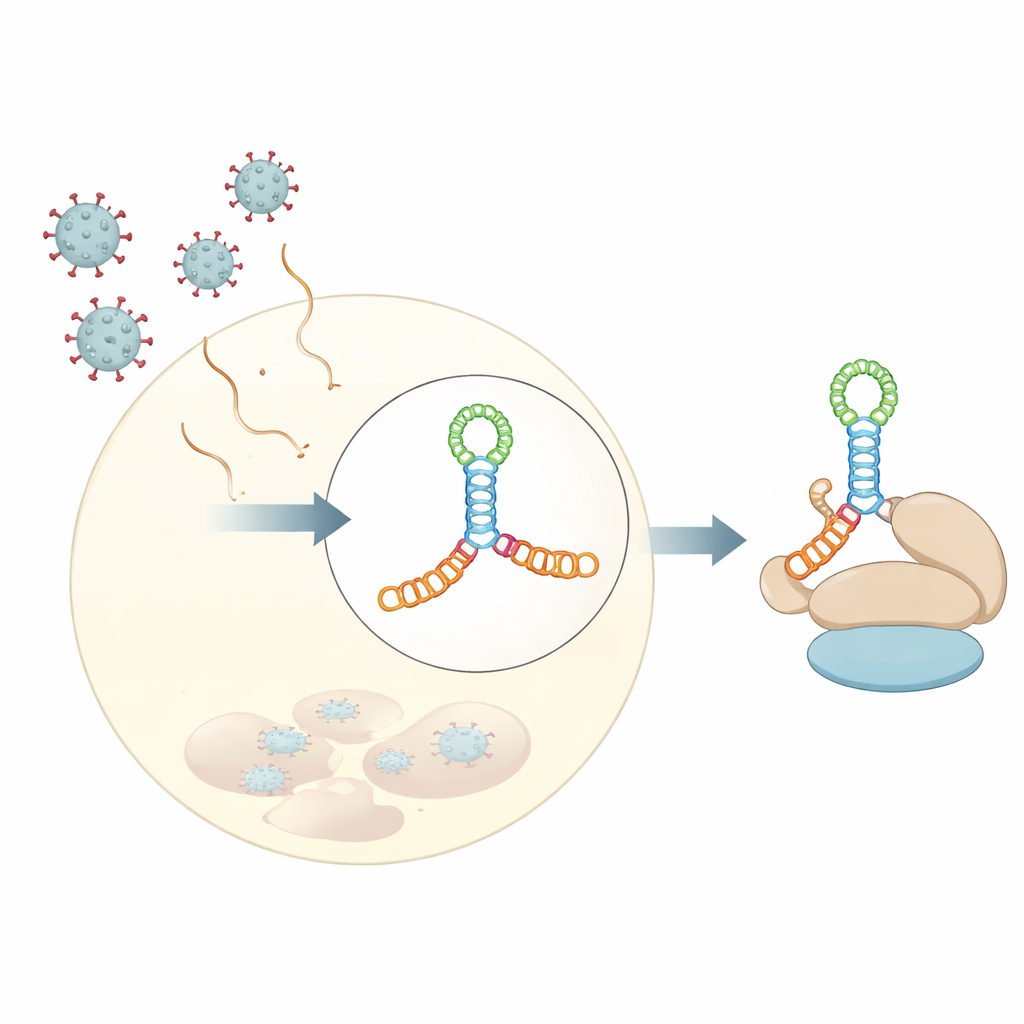
Verschiedene Viren, gleicher struktureller Bauplan
Bemerkenswerterweise stellten die Forschenden beim Vergleich dieser Struktur mit zuvor gelösten RNA‑Segmenten aus zwei anderen Picornaviren — der JK‑Domäne des Enzephalomyokarditis‑Virus und der Domäne V des Hepatitis‑A‑Virus — fest, dass die Gesamt‑Topologie dreidimensional nahezu identisch ist, obwohl die zugrunde liegenden RNA‑Sequenzen deutlich variieren. In allen drei Fällen dockt eine A‑reiche Schleife seitlich an eine nahegelegene Helix und organisiert eine kompakte Verbindung, bei der zwei Hauptstämme aufeinander gestapelt sind. Dieses wiederkehrende Layout scheint ein strukturelles „Motiv“ zu sein, das die Evolution über verschiedene Virusspezies hinweg wiederverwendet hat, um Wirtsfaktoren trotz großer Sequenz‑ und Detailunterschiede eine vertraute Bindungsoberfläche zu präsentieren.
Wie die virale Faltung einen Wirtsfaktor greift
Um zu verstehen, wie diese gemeinsame RNA‑Form eIF4G einfängt, maßen die Forschenden die Bindung zwischen den viralen RNAs und der HEAT1‑Region von eIF4G, einem gebogenen Modul, das für RNA‑Kontakte bekannt ist. Alle drei viralen Domänen banden HEAT1 mit nanomolarer Affinität, also sehr starke Wechselwirkungen. Durch gezielte Mutationen in den RNA‑Verzweigungen und Schleifen konnten sie die Bindung abschwächen oder aufheben und so ermitteln, welche Merkmale am wichtigsten waren. Veränderungen, die kleine Ausbuchtungen in Schlüsselhelixen entfernten oder die A‑reiche Schleife störten, reduzierten die Bindung stark, obwohl die mutierten Nukleotide nicht direkt mit dem Protein in Kontakt vorhergesagt werden. Das deutet darauf hin, dass die Schleife und die Ausbuchtungen als innere Streben wirken und die relative Orientierung der gestapelten Helices fixieren, sodass eine durchgehende laterale Oberfläche genau die richtige Form für das Andocken von HEAT1 aufweist. 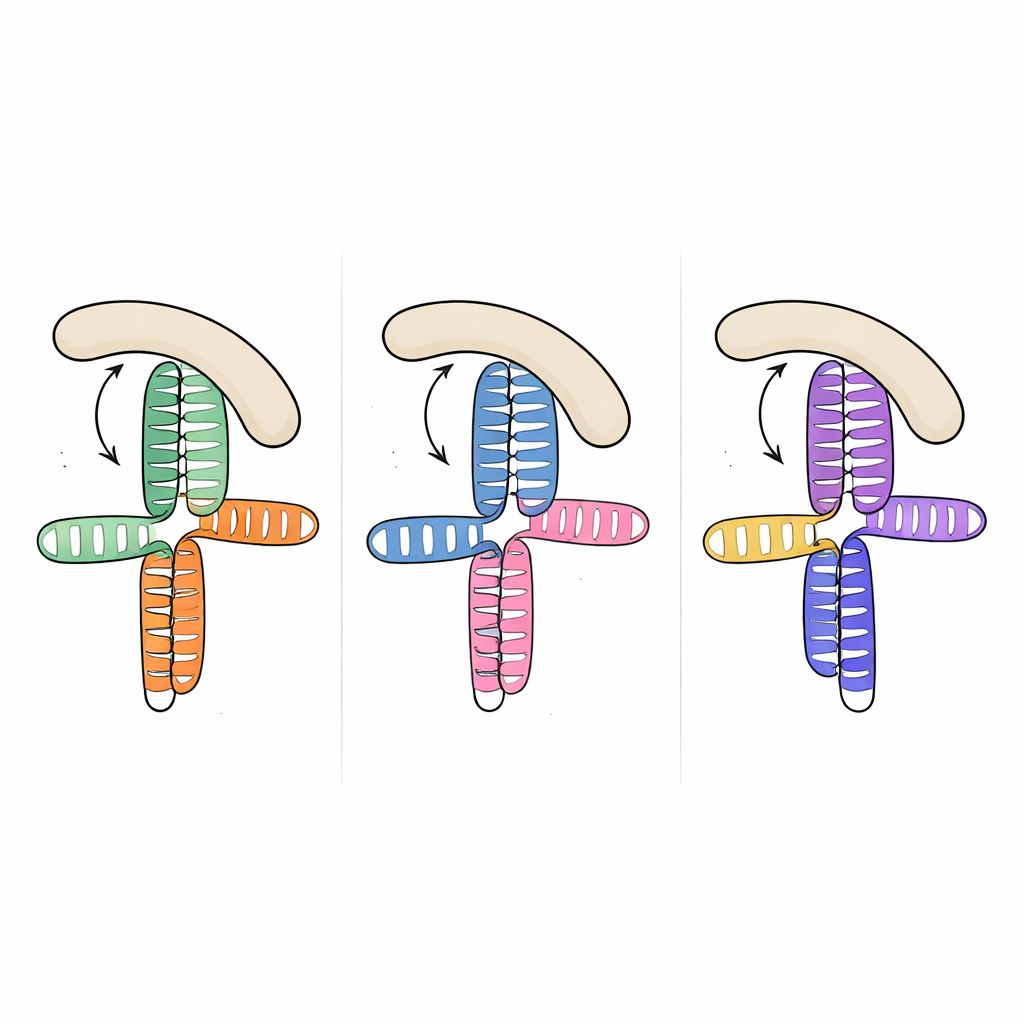
Gemeinsame Mechanik und neue Arzneimittelperspektiven
Chemische Footprinting‑Experimente, die abbilden, welche Bereiche des RNA‑Rückgrats geschützt sind, wenn das Protein gebunden ist, bestätigten, dass HEAT1 hauptsächlich eine Seite der gestapelten Helices gegenüber der organisierenden A‑reichen Schleife kontaktiert, und zwar in einer Weise, die eng mit Kryo‑EM‑Beobachtungen eines der anderen Viren übereinstimmt. Zusammengenommen zeigen die Daten, dass mehrere unterschiedliche Picornaviren eine gemeinsame strukturelle Strategie nutzen: Sie bauen ähnliche RNA‑Gerüste, die konservierte dreidimensionale Merkmale dem gleichen Wirtsfaktor eIF4G präsentieren, obwohl die Sequenzen variieren. Für Nicht‑Spezialisten lautet das Fazit, dass Viren aus verschiedenen Zweigen des Stammbaums auf denselben Faltungs‑Trick zurückgreifen, um sich in die zelluläre Übersetzungsmaschinerie einzuklinken. Weil dieser Trick mehr von der Form als von der Sequenz abhängt, könnte es möglich sein, Wirkstoffe oder Moleküle zu entwickeln, die diese konservierte RNA‑Architektur erkennen und deaktivieren und so die Proteinproduktion mehrerer Virusspezies mit einer einzigen Behandlung blockieren.
Zitation: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Schlüsselwörter: virus‑RNA‑Struktur, internaler Ribosomen‑Einstiegspunkt, eIF4G‑Bindung, Picornavirus‑Translation, Breitband‑Virostatika