Clear Sky Science · tr
Picornaviral IRES tipleri arasındaki eIF4G bağlayan RNA domaine'larının yapıları topolojik olarak korunmuştur
Bazı Virüslerin Hücrelerimizi Nasıl Ele Geçirdiği
Soğuk algınlığı, kalp iltihabı ve hepatit gibi yaygın hastalıklara neden olan birçok virüs ortak bir temel sorunla karşı karşıyadır: hücrelerimizi kendi proteinlerini yapmak yerine viral protein üretmeye nasıl kandıracakları. Bu çalışma, viral genetik materyalin kritik bir parçasının konağın bir proteinine yapışan ve viral protein üretimini başlatan kesin üç boyutlu şekle atomik ayrıntıda nasıl katlandığını ortaya koyuyor. Farklı virüsler arasında paylaşılan bu yapısal hileyi anlamak, hepsini aynı anda hedefleyebilecek geniş spektrumlu antiviral ilaçlara giden yolu işaret edebilir.
Protein Fabrikası İçin Özel Bir Giriş Noktası
Hücremizdeki mesajların (mRNA'ların) çoğu, hücrenin protein yapım makinesini çekmeye yardımcı olan kimyasal bir “kap” ile başlar. Picornaviridae ailesindeki birçok RNA virüsü bu kapa sahip değildir, yine de aynı makineyi ele geçirmeyi başarır. Bunu, viral genomun ön kısmına yakın, ribozom için alternatif iniş platformları oluşturan yapısal RNA segmentleri olan internal ribosome entry site (IRES) elemanları kullanarak yaparlar. Bu IRES bölgeleri içinde, bazı virüslerde V domeni olarak adlandırılan belirli bir bölüm, eIF4G adındaki bir başlatma faktörüne güçlü şekilde bağlanır; eIF4G, protein sentezini başlatmak için gereken diğer bileşenleri düzenleyen bir iskelet gibidir.
Viral Bir RNA Düğümüne Yüksek Çözünürlüklü Bakış
Yazarlar, insan enterovirüsleri için model olarak sık kullanılan coxsackievirus B3'ün V domeninin 3 Å çözünürlüğünde kristal yapısını belirlediler. Basit bir saç tokası yapısı yerine bu RNA, uzamış bir dört yönlü eklemin içine katlanıyor—iki üst üste yığılı çubuğun merkezde kısa bir çubuğu kestiğini ve A açısından zengin bir halkayla bir arada tutulan H biçimli bir kavşak oluşturduğunu hayal edin. Bu kompakt heliks düğümü, küçük kabarcıklar ve halkaları katmanları iskelet oluşturacak şekilde doğru açılarda konumlandırır. Küçük açı X ışını saçılması ve kimyasal footprinting dahil çözeltide yapılan deneyler ile modern yapı tahmin araçları, bu katlanmanın kristalleşme artefaktı olmadığını, RNA'nın suda sergilediği davranışı yansıttığını gösterdi. 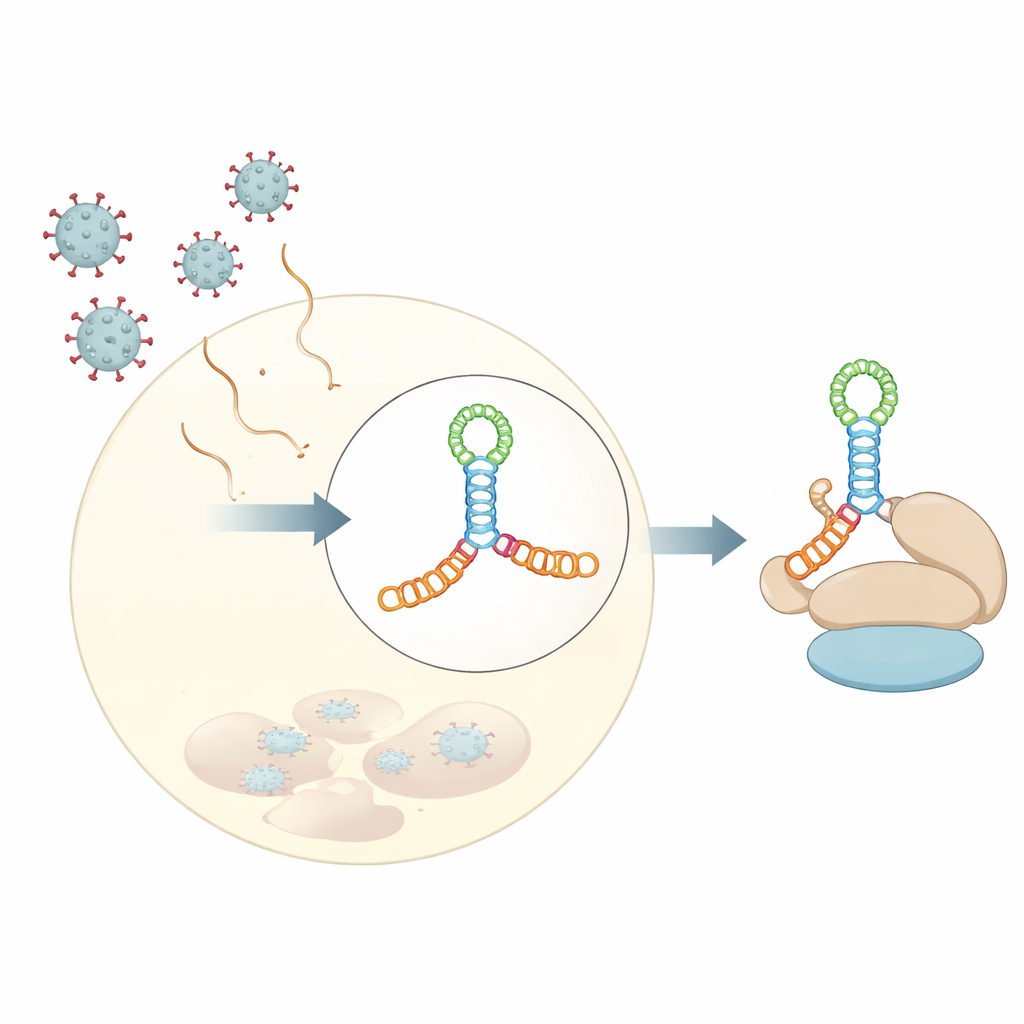
Farklı Virüsler, Aynı Yapısal Plan
Çarpıcı şekilde, ekip bu yapıyı daha önce çözülmüş iki diğer picornavirüs segmenti—encephalomyocarditis virus’un JK domeni ve hepatit A virüsünün V domeni—ile karşılaştırdığında, altında yatan RNA dizileri önemli ölçüde farklı olmasına rağmen genel üç boyutlu topolojinin neredeyse aynı olduğunu buldular. Üç durumda da A açısından zengin bir halka yakındaki bir heliksin yanına oturuyor ve iki ana sapın üst üste yığıldığı kompakt bir kavşak oluşturuyordu. Bu tekrar eden düzen, evrimin farklı viral türler arasında dizi ve ince ayrıntılardaki büyük farklılıklara rağmen konağın bağlanma yüzeyine benzer bir yapı sunmak için yeniden kullandığı bir yapısal “motif” gibi görünüyor.
Viral Katlanma Konağın Faktörünü Nasıl Kavrar
Bu paylaşılan RNA şeklinin eIF4G'yi nasıl yakaladığını anlamak için araştırmacılar viral RNA'lar ile eIF4G'nin RNA ile temas ettiği bilinen kavisli modülü HEAT1 arasındaki bağlanmayı ölçtüler. Üç viral domenin tümü HEAT1'e nanomolar afiniteyle bağlandı; bu çok sıkı etkileşimler anlamına geliyor. RNA kavşaklarında ve halkalarında hedefe yönelik mutasyonlar uygulayarak, bağlanmayı zayıflatan veya ortadan kaldıran değişiklikleri yapabildiler ve hangi özelliklerin en önemli olduğunu belirlediler. Ana helikslerdeki küçük kabarcıkları kaldıran veya A açısından zengin halkayı bozan değişiklikler, mutante edilmiş nükleotidler proteine doğrudan temas etmiyor gibi görünse bile bağlanmayı büyük ölçüde azalttı. Bu, halka ve kabarcıkların iç destekler gibi davranıp üst üste yığılmış helikslerin göreli yönelimini sabitleyerek HEAT1'in yanaşması için süreklilik gösteren bir yan yüzeyin kusursuz biçimde oluşmasını sağladığını düşündürüyor. 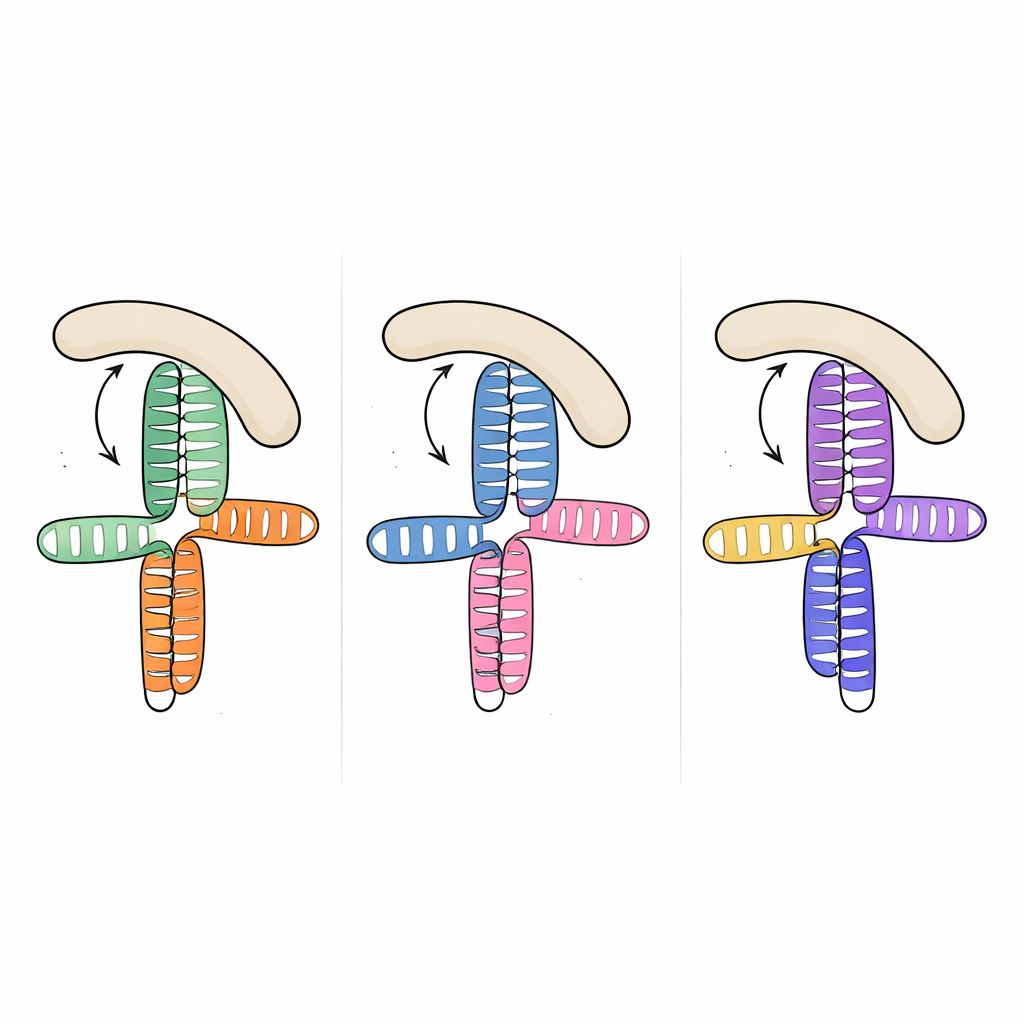
Ortak Mekanikler ve Yeni İlaç Olanakları
Protein bağlandığında RNA omurgasının hangi bölümlerinin korunduğunu haritalayan kimyasal “footprinting” deneyleri, HEAT1'in esas olarak A açısından zengin halkayı organize etmenin karşısındaki yığılmış helikslerin bir tarafıyla temas ettiğini doğruladı; bu, diğer virüslerden birine ait kriyo-elektron mikroskopi gözlemleriyle yakından örtüşüyor. Bir arada düşünüldüğünde, çalışma farklı picornavirüslerin aynı konağın faktörüne, eIF4G'ye, benzer üç boyutlu özellikler sunan benzer RNA iskeletleri inşa etme yoluyla ortak bir yapısal strateji kullandıklarını gösteriyor; diziler kendileri değişse bile. Uzman olmayanlar için çıkarım şu: aile ağacının farklı dallarındaki virüsler, hücrenin çeviri donanımına takılmak için aynı katlanma hilesine yöneliyor. Bu hile dizi yerine şekle dayandığı için, bu korunan RNA mimarisini tanıyan ve işlevsiz hale getiren ilaçlar veya moleküller tasarlamak mümkün olabilir; bu da tek bir tedaviyle birden çok viral türde protein üretimini engelleyebilir.
Atıf: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Anahtar kelimeler: viral RNA yapısı, internal ribosome entry site, eIF4G bağlanması, picornavirus çevirimi, geniş spektrum antiviral ilaçlar