Clear Sky Science · ja
ピコルナウイルスIRES型におけるeIF4G結合RNAドメインの構造はトポロジー的に保存されている
特定のウイルスがどのようにして細胞を乗っ取るか
風邪、心筋炎、肝炎などを引き起こす一般的なウイルスの多くは、共通の基本的な課題に直面しています。すなわち、自分たちのタンパク質を合成するように宿主細胞をいかに騙すか、ということです。本研究は、ウイルスの遺伝情報の重要な部分がどのように正確な三次元形状に折りたたまれ、宿主タンパク質に取り付き、ウイルスのタンパク質合成を開始するのかを原子レベルで明らかにしています。異なるウイルス間で共有されるこの構造的なトリックを理解することは、複数のウイルスに同時に作用する広域抗ウイルス薬の開発につながる可能性があります。
タンパク質工場への特殊な入口
ほとんどの細胞内メッセージ(mRNA)は、細胞のタンパク質合成機構を呼び寄せる化学的な「キャップ」を先頭に持ちます。ピコルナ科ウイルスの多くはこのキャップを持たないにもかかわらず、同じ機構を乗っ取ることに成功します。彼らは内部リボソーム侵入部位(IRES)と呼ばれる、ウイルスゲノムの前方付近にある構造化されたRNA断片を使い、リボソームの代替的な着地点として機能させます。これらのIRES領域の中で、いくつかのウイルスで「ドメインV」と呼ばれる特定の領域が、宿主の開始因子eIF4Gに強く結合します。eIF4Gは他の成分を組織化する足場のような役割を果たします。
ウイルスRNAの結び目を高解像度で見る
著者らは、ヒトエンテロウイルスのモデルとしてよく用いられるコクサッキーウイルスB3のドメインVの3オングストロームの結晶構造を決定しました。このRNAは単純なヘアピンではなく、伸長した四方ジャンクションに折りたたまれていました。中央で短い棒が交差する二本の積み重なった棒を想像するとよく、Aに富むループによって結びつけられたH字型の接合になっています。このコンパクトならせん束は、小さなバルジやループをちょうど適切な角度に配置して剛直な足場を形成します。小角X線散乱や化学的フットプリンティングなどの溶液中実験に加え、現代的な構造予測ツールの解析により、この折りたたみは結晶化の人工物ではなく、水中でのRNAの挙動を反映していることが示されました。 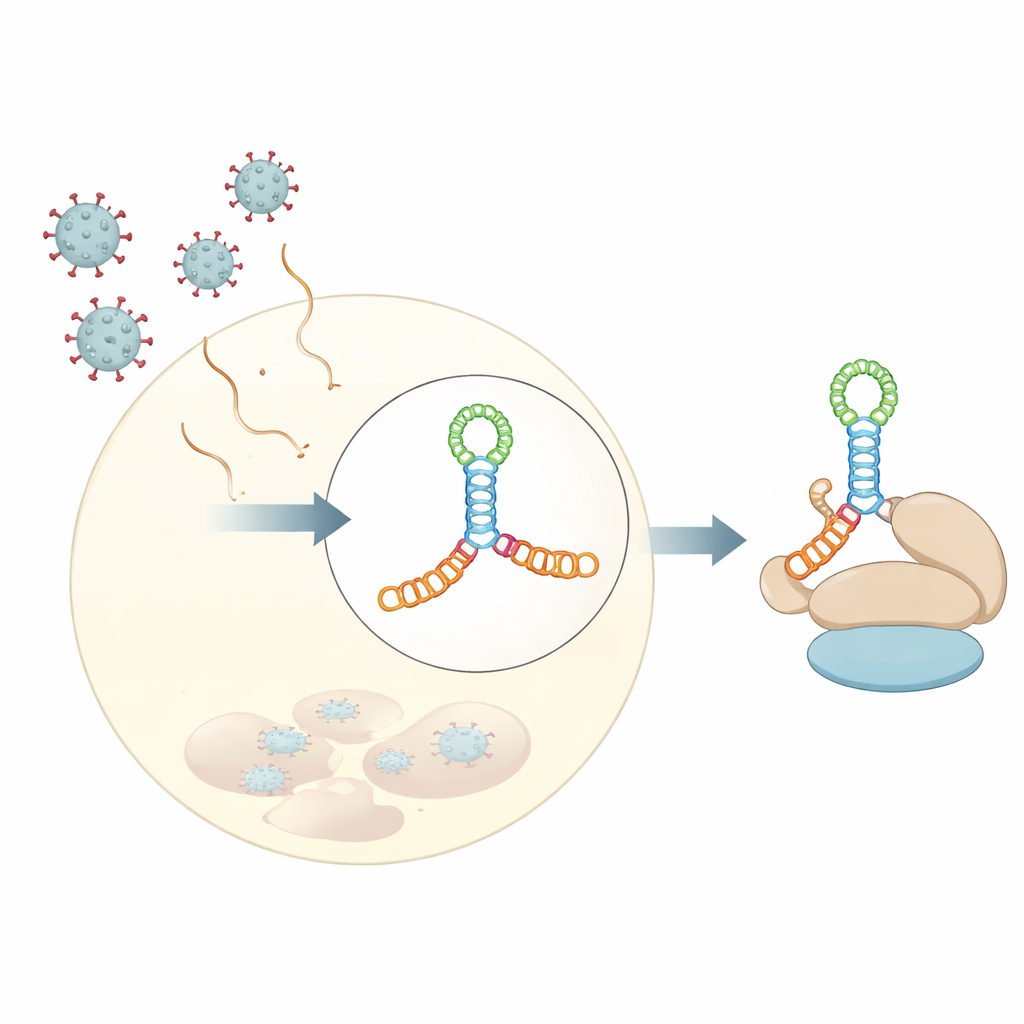
異なるウイルス、同じ構造設計図
注目すべきことに、研究チームがこの構造を以前に決定されていた2つの他のピコルナウイルス由来RNA断片—脳炎心筋炎ウイルスのJKドメインとA型肝炎ウイルスのドメインV—と比較したところ、基礎となる配列はかなり異なるにもかかわらず、三次元トポロジーはほぼ同じであることがわかりました。3例とも、Aに富むループが近傍のヘリックスの側面にドッキングし、2本の主要な茎が互いに重なり合うコンパクトな接合部を形成しています。この繰り返される配置は、配列や細部が大きく異なっても、進化がウイルス種を超えて宿主因子に馴染みのある結合面を提示するために再利用してきた構造的「モチーフ」であると考えられます。
ウイルスの折りたたみが宿主因子をどのように捉えるか
この共有されたRNA形状がどのようにしてeIF4Gを捕捉するかを理解するために、研究者らはウイルスRNAとeIF4GのHEAT1領域(RNAに接触すると知られる弧状のモジュール)との結合を測定しました。三つのウイルスドメインはいずれもHEAT1にナノモーラーの親和性で結合し、非常に強い相互作用を示しました。RNAの接合部やループに標的変異を導入することで、結合が弱まったり消失したりし、どの特徴が重要かを明らかにできました。重要なヘリックスの小さなバルジを取り除いたり、Aに富むループを乱したりすると結合が大幅に低下しましたが、これらの変異ヌクレオチドはタンパク質に直接触れるとは予測されていませんでした。これは、ループとバルジが内部の支柱として働き、積み重なったヘリックスの相対的な配向を固定して、連続した側面がHEAT1のドッキングに最適な形になることを示唆しています。 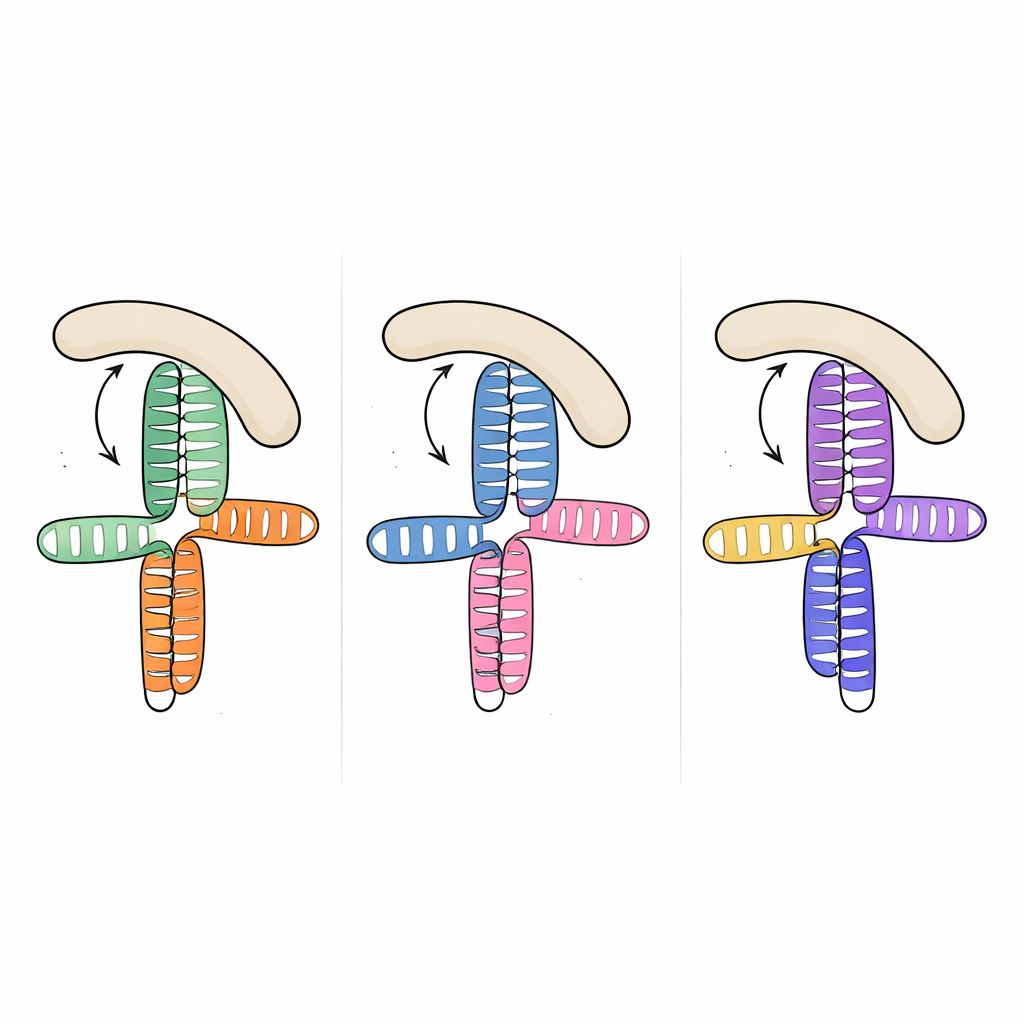
共有するメカニズムと新たな薬剤の可能性
タンパク質結合時にRNA骨格のどの部分が保護されるかをマップする化学的フットプリンティング実験は、HEAT1が主にAに富むループを配置する側とは反対の、積み重なったヘリックスの一側面に接触することを確認しました。これは他のウイルスの一例で得られたクライオ電子顕微鏡の観察とよく一致します。総じて、本研究は複数の異なるピコルナウイルスが共通の構造戦略を用いていることを示しています。すなわち、配列は異なっていても類似したRNA足場を組み立て、同じ宿主因子eIF4Gに保存された三次元的特徴を提示しているのです。専門外の読者への要点は、系統樹の異なる枝に属するウイルスが、細胞の翻訳機構に差し込むために同じ折りたたみのトリックに収束しているということです。このトリックが配列よりも形に依存しているため、この保存されたRNAアーキテクチャを認識して無効化する薬剤や分子を設計すれば、単一の治療で複数のウイルス種にまたがるタンパク質合成を阻止できる可能性があります。
引用: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
キーワード: ウイルスRNA構造, 内部リボソーム侵入部位, eIF4G結合, ピコルナウイルスの翻訳, 広域抗ウイルス薬