Clear Sky Science · ru
Топологическая сохранность структур доменов РНК, связывающих eIF4G, среди типов IRES пикорнавирусов
Как некоторые вирусы захватывают наши клетки
Многие распространённые вирусы, в том числе вызывающие простуды, воспаление сердца и гепатит, сталкиваются с одной и той же задачей: как заставить клетки синтезировать вирусные белки вместо своих собственных. В этом исследовании подробно, на атомном уровне, показано, как ключевой участок вирусной генетической информации складывается в точную трёхмерную форму, которая цепляется за белок хозяина и запускает производство вирусных белков. Понимание этого общего структурного приёма у разных вирусов может указать путь к созданию широкоспектровых противовирусных препаратов, нацеленных сразу на многих из них.
Особая «точка входа» для белкового завода
Большинство наших клеточных сообщений (мРНК) начинаются с химической «шапочки», которая помогает привлекать аппаратуру клетки для синтеза белка. Многие РНК-вирусы из семейства Picornaviridae лишены такой шапочки, но тем не менее захватывают ту же аппаратуру. Для этого они используют внутренние сайты инициации трансляции, или элементы IRES — структурированные участки РНК у переднего конца вирусного генома, которые служат альтернативными посадочными площадками для рибосомы. Внутри этих областей IRES один конкретный участок, называемый доменом V у нескольких вирусов, сильно связывается с фактором инициации хозяина eIF4G — своего рода каркасом, организующим другие компоненты, необходимые для начала синтеза белка.
Высокодетализированный взгляд на вирусный «узел» РНК
Авторы определили кристаллическую структуру домена V кокссакиевого вируса B3 с разрешением около 3 ангстрем. Вместо простой шпильки эта РНК складывается в удлинённый четырёхветвевой стык — представьте две сложенные друг на друга «перемычки», пересекающие более короткую «перемычку» в центре, формируя Н‑образный узел, скреплённый A-богатой петлёй. Этот компактный узел спиралей позиционирует небольшие выпуклости и петли под нужными углами, формируя жёсткую опорную структуру. Эксперименты в растворе, включая рассеяние малых углов рентгеновских лучей и химическое «футпринтинг»- картирование, вместе с современными инструментами прогнозирования структуры показали, что эта фолдинг-конфигурация не является артефактом кристаллизирования, а отражает поведение РНК в водной среде. 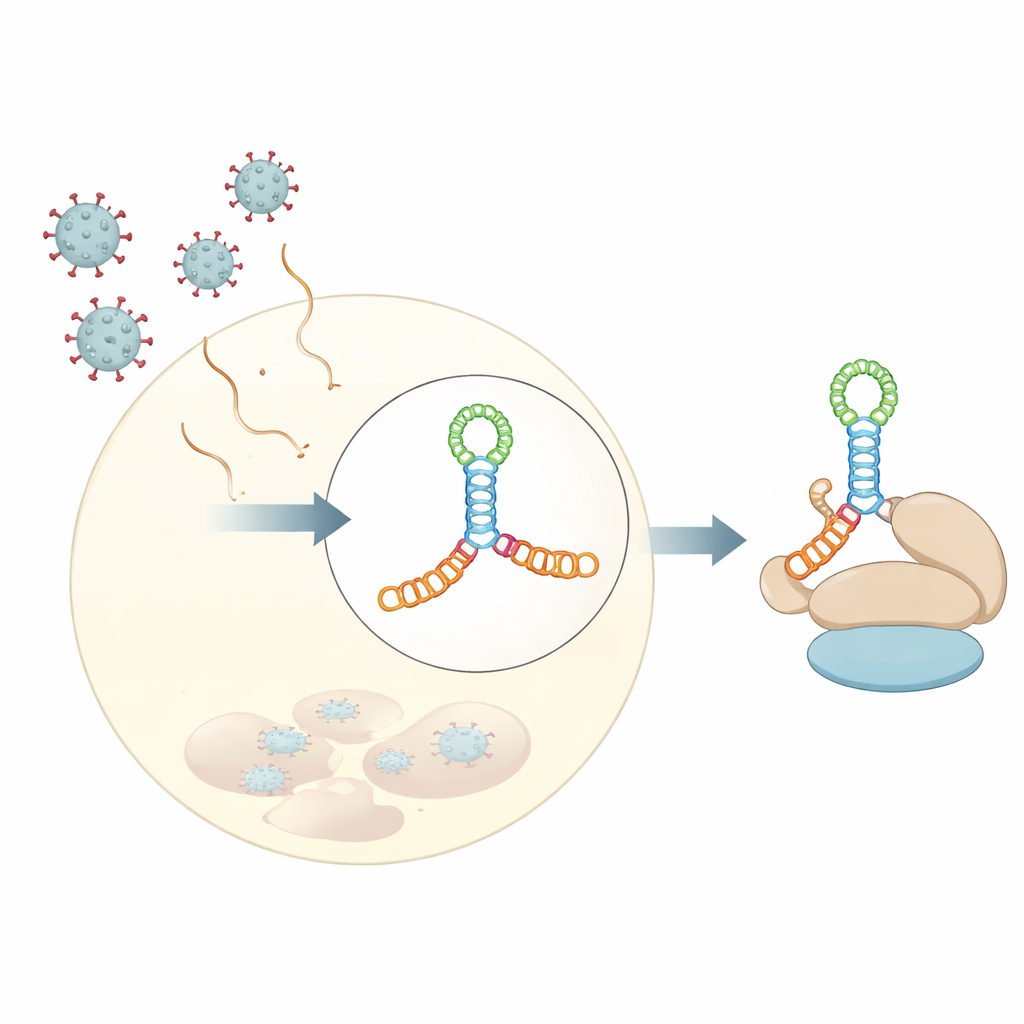
Разные вирусы, один и тот же структурный чертёж
Удивительно, но при сравнении этой структуры с ранее решёнными сегментами РНК двух других пикорнавирусов — JK-доменом вируса энцефаломиокардита и доменом V вируса гепатита A — команда обнаружила, что общая трёхмерная топология почти одинакова, несмотря на существенные различия в последовательностях РНК. Во всех трёх случаях A‑богатая петля «встраивается» в боковую сторону соседней спирали и организует компактный стык, где два основных стебля укладываются друг на друга. Этот повторяющийся рисунок выглядит как структурный «мотив», который эволюция повторно использовала у разных вирусных видов, чтобы предоставить факторам хозяина знакомую поверхность для связывания, несмотря на широкие вариации в последовательности и мелких деталях.
Как вирусная укладка захватывает фактор хозяина
Чтобы понять, как общая форма РНК захватывает eIF4G, исследователи измеряли связывание вирусных РНК с регионом HEAT1 белка eIF4G — изогнутым модулем, известным способностью контактировать с РНК. Все три вирусных домена связывались с HEAT1 с наномолярной аффинностью, то есть очень сильно. Вводя целевые мутации в стыки и петли РНК, они могли ослаблять или полностью нарушать связывание и выяснять, какие элементы имеют решающее значение. Изменения, которые удаляли маленькие выпуклости в ключевых спиралях или разрушали A‑богатую петлю, существенно снижали связывание, хотя замещённые нуклеотиды не предполагаются как прямые контакты с белком. Это указывает на то, что петля и выпуклости действуют как внутренние распорки, фиксируя относительную ориентацию сложенных спиралей так, чтобы сплошная боковая поверхность была идеально сформирована для «стыковки» HEAT1. 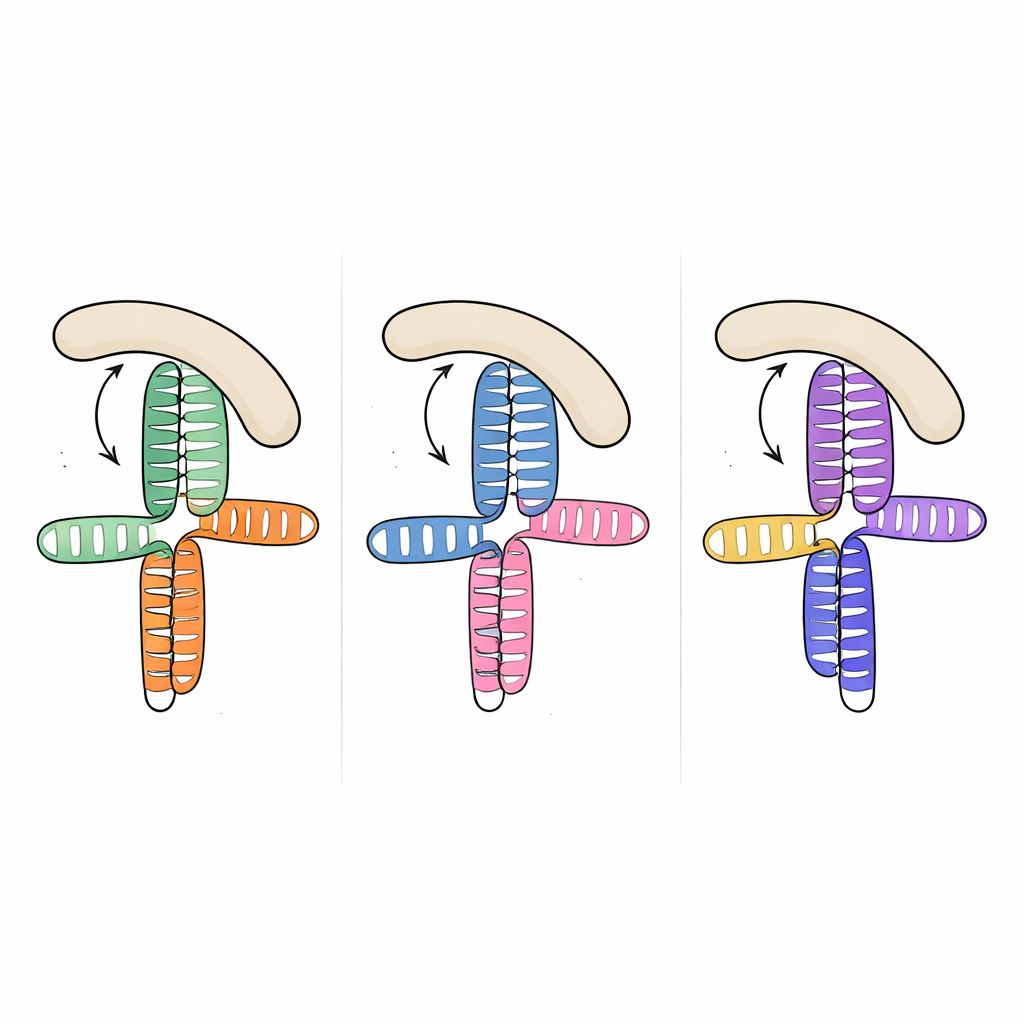
Общая механика и новые возможности для лекарств
Химические эксперименты «футпринтинга», которые отображают, какие участки сахарофосфатного остова РНК защищаются при связывании белка, подтвердили, что HEAT1 преимущественно контактирует с одной стороны сложенных спиралей, противоположной организующей A‑богатой петле, что в значительной степени повторяет наблюдения методом крио-ЭМ для одного из других вирусов. В совокупности работа показывает, что несколько различных пикорнавирусов используют общую структурную стратегию: они строят похожие РНК‑каркасы, которые демонстрируют сохранённые трёхмерные признаки одному и тому же фактору хозяина, eIF4G, хотя сами последовательности различаются. Для неспециалиста главное: вирусы из разных ветвей семейного древа приходят к одному и тому же приёму свёртывания, чтобы подключиться к аппаратуре трансляции клетки. Поскольку этот приём зависит скорее от формы, чем от последовательности, возможно разработать препараты или молекулы, распознающие и дезактивирующие эту сохранённую архитектуру РНК, потенциально блокируя синтез белков у нескольких вирусных видов одним лечением.
Цитирование: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Ключевые слова: структура вирусной РНК, внутренний сайт инициации трансляции, связывание с eIF4G, трансляция пикорнавирусов, широкоспектровые противовирусные средства