Clear Sky Science · ar
هياكل مجالات الحمض النووي الريبي المرتبطة بـ eIF4G بين أنواع IRES للبيكورنافيروس محافِظة طوبولوجيًا
كيف تخطف فيروسات معينة خلايانا
تواجه العديد من الفيروسات الشائعة، بما في ذلك تلك المسببة لنزلات البرد والتهاب القلب والتهاب الكبد، نفس التحدي الأساسي: كيف تخدع خلايانا لصنع بروتينات فيروسية بدلًا من بروتيناتها. تكشف هذه الدراسة، بدقة ذرية، كيف يطوي جزء رئيسي من المادة الوراثية الفيروسية نفسه إلى شكل ثلاثي الأبعاد محدد يلتصق ببروتين مضيف ويشغّل إنتاج البروتين الفيروسي. فهم هذه الحيلة البنائية المشتركة عبر فيروسات مختلفة قد يوجه نحو تطوير مضادات فيروسية واسعة الطيف تستهدفها جميعًا في آن واحد.
مدخل خاص لمصنع البروتين
تبدأ معظم رسائل الخلية (mRNAs) بـ«غطاء» كيميائي يساعد في استدعاء آلية صنع البروتين في الخلية. تفتقد العديد من فيروسات عائلة Picornaviridae لهذا الغطاء، ومع ذلك تنجح في الاستيلاء على نفس الآلية. تفعل ذلك باستخدام مواقع دخول الريبوسوم الداخلية، أو عناصر IRES—مقاطع ريبوزية مُنظمة قريبة من مقدمة الجينوم الفيروسي تعمل كأرصفة بديلة للريبوسوم. ضمن هذه المناطق، يرتبط قسم محدد، يسمى المجال V في عدة فيروسات، بقوة بعامل بدء مضيف يسمى eIF4G، وهو بمثابة هيكل يساعد في تنظيم مكونات أخرى ضرورية لبدء تخليق البروتين.
نظرة عالية الدقة على عقدة حمض نووي ريبوزي فيروسية
حدَّد المؤلفون بنية بلّورية بوضوح 3 أنغستروم للمجال V من فيروس كوبساكي B3، وهو فيروس يُستخدم غالبًا كنموذج لفيروسات الأمعاء البشرية. بدلًا من كونه شعرة بسيطة، يطوي هذا الحمض النووي الريبي نفسه إلى مفترق من أربعة فروع ممدود—تخيل قضيبين مكدسين يعبران قضيبًا أقصر في الوسط، مكونين مفترقًا على شكل حرف H مثبتًا بحلقة غنية بالنوكليوتيدات A. هذه العقدة المدمجة من الحلزونات تضع نتوءات ودوائر صغيرة بزاويا مناسبة لتكوين هيكل صلب. أظهرت تجارب في المحلول، بما في ذلك تشتت الأشعة السينية بزوايا صغيرة وخراطة كيميائية للبصمة، إلى جانب أدوات التنبؤ بالهياكل الحديثة، أن هذا الطي ليس أثرًا للتبلور بل يعكس سلوك الحمض النووي الريبي في الماء. 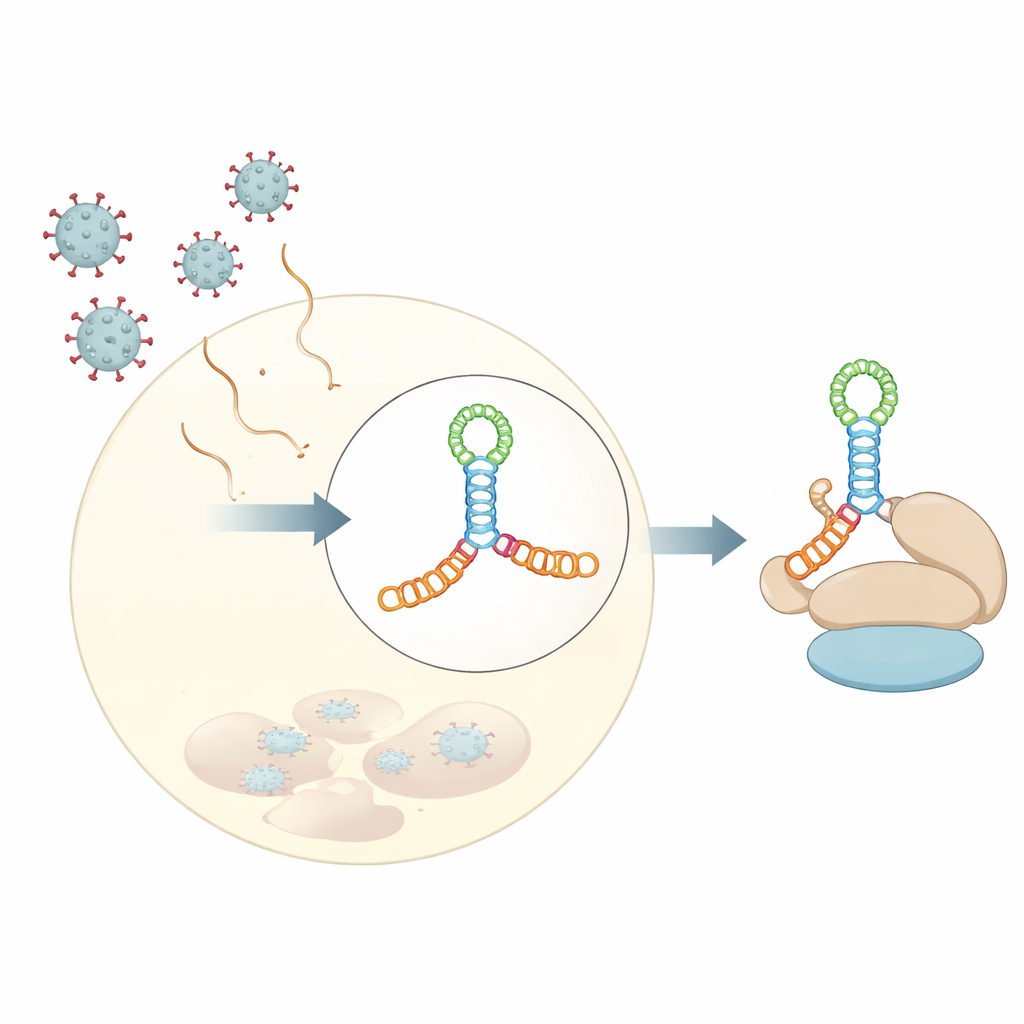
فيروسات مختلفة، نفس المخطط البنائي
من اللافت أنه عندما قارن الفريق هذه البنية بمقاطع ريبوزية محلولة سابقًا من فيروستين بيكورنافيريتين أخريين—مجال JK من فيروس التهاب الدماغ والعضلة القلبية والرحم (encephalomyocarditis) والمجال V من فيروس التهاب الكبد A—وجدوا أن الطوبولوجيا ثلاثية الأبعاد العامة متشابهة تقريبًا، رغم اختلاف سلاسل الحمض النووي الريبي الأساسية اختلافًا كبيرًا. في كل الحالات الثلاث، تدخل حلقة غنية بالنيوكليوتيدات A إلى جانب أحد الحلزونات المجاورة وتنظم مفترقًا مدمجًا حيث يتراص جذعان رئيسيان فوق بعضهما البعض. يبدو أن هذا الترتيب المتكرر هو «نمط» بنيوي أعادته التطور عبر أنواع فيروسية لتقديم سطح ارتباط مألوف لعوامل المضيف، على الرغم من التباين الكبير في التسلسل والتفاصيل الدقيقة.
كيف يمسك الطي الفيروسي بعامل مضيف
لفهم كيف تلتقط هذه البنية الريبوزية المشتركة eIF4G، قاس الباحثون الترابط بين الأحماض الريبية الفيروسية ومنطقة HEAT1 من eIF4G، وهي وحدة منحنية معروفة بالتلامس مع RNA. ارتبطت المجالات الفيروسية الثلاث جميعها بـ HEAT1 بألفة نانومولارية، ما يعني تفاعلات شديدة القوة. عبر إدخال طفرات موجهة في المفترقات والدوائر الريبوزية، تمكنوا من إضعاف أو إلغاء الارتباط ورصد الميزات الأكثر أهمية. التغييرات التي أزالت نتوءات صغيرة في الحلزونات الرئيسية أو عطلت الحلقة الغنية بالـ A خفضت الارتباط بشكل كبير، رغم أن النوكليوتيدات المتحولة لا يُتوقع أن تلامس البروتين مباشرة. وهذا يوحي بأن الحلقة والنتوءات تعمل كدعامات داخلية، تثبت التوجه النسبي للجذوع المتراصة بحيث يصبح سطحًا جانبيًا مستمرًا مشكلاً بدقة ليتكامل HEAT1 معه.
آليات مشتركة وإمكانات دوائية جديدة
أكدت تجارب «خراطة البصمة» الكيميائية، التي ترسم أي أجزاء من العمود الفقري للـ RNA تُحمي عند ارتباط البروتين، أن HEAT1 يتلامس أساسًا مع جانب واحد من الجذوع المكدسة المقابلة للحلقة المنظمة الغنية بـ A، بطريقة تقابل عن كثب ملاحظات المجهر الإلكتروني بالتبريد لأحد الفيروسات الأخرى. مجمل العمل يبين أن عدة فيكورنافيروسات متميزة تستخدم استراتيجية بنائية مشتركة: تبني أطرًا ريبوزية مماثلة تعرض ميزات ثلاثية الأبعاد محفوظة لنفس عامل المضيف، eIF4G، رغم تفاوت التسلسلات نفسها. للخارج عن التخصص، الخلاصة أن فيروسات من فروع مختلفة على شجرة العائلة تتقارب على نفس حيلة الطي لتوصيل نفسها إلى آلية ترجمة الخلية. وبما أن هذه الحيلة تعتمد على الشكل أكثر من التسلسل، فقد يكون من الممكن تصميم أدوية أو جزيئات تتعرف على هذه الهندسة الريبوزية المحفوظة وتلغي فعاليتها، ما يعرقل إنتاج البروتين عبر أنواع فيروسية متعددة بعلاج واحد محتمل.
الاستشهاد: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
الكلمات المفتاحية: بنية حمض نووي ريبوزي فيروسي, موقع دخول الريبوسوم الداخلي, الارتباط بـ eIF4G, ترجمة بيكورنافيروس, مضادات فيروسية واسعة الطيف