Clear Sky Science · pt
Estruturas dos domínios de RNA que se ligam a eIF4G entre os tipos de IRES picornaviral são topologicamente conservadas
Como certos vírus sequestram nossas células
Muitos vírus comuns, inclusive os que causam resfriados, inflamação cardíaca e hepatite, enfrentam o mesmo desafio básico: como enganar nossas células para produzirem proteínas virais em vez das suas. Este estudo revela, em detalhe atômico, como um elemento chave do material genético viral se dobra em uma forma tridimensional precisa que se liga a uma proteína do hospedeiro e inicia a produção de proteínas virais. Entender esse truque estrutural compartilhado entre diferentes vírus pode apontar caminhos para fármacos antivirais de amplo espectro que os atinjam simultaneamente.
Um ponto de entrada especial para a fábrica de proteínas
A maior parte das mensagens celulares (mRNAs) começa com uma “capa” química que ajuda a recrutar a maquinaria de síntese proteica. Muitos vírus de RNA da família Picornaviridae não têm essa capa, mas ainda assim conseguem se apossar da mesma maquinaria. Eles fazem isso usando sítios internos de entrada do ribossomo, ou elementos IRES—segmentos estruturados de RNA próximos à extremidade inicial do genoma viral que servem como pontos de ancoragem alternativos para o ribossomo. Dentro dessas regiões IRES, uma seção particular, chamada domínio V em vários vírus, liga‑se fortemente a um fator de iniciação do hospedeiro chamado eIF4G, uma espécie de andaime que organiza outros componentes necessários para iniciar a síntese proteica.
Uma visão de alta resolução de um nó de RNA viral
Os autores determinaram uma estrutura cristalina a 3 angstroms do domínio V do coxsackievírus B3, um vírus frequentemente usado como modelo para enterovírus humanos. Em vez de um simples hairpin, esse RNA se dobra em uma junção alongada de quatro vias—imagine dois bastões empilhados cruzando outro bastão curto no centro, formando uma junção em H mantida por uma alça rica em adeninas. Esse nó compacto de hélices posiciona ressaltos e alças em ângulos precisos para formar um andaime rígido. Experimentos em solução, incluindo espalhamento de raios X em pequeno ângulo e footprinting químico, juntamente com ferramentas modernas de predição estrutural, mostraram que esse enovelamento não é um artefato da cristalização, mas reflete o comportamento do RNA em solução aquosa. 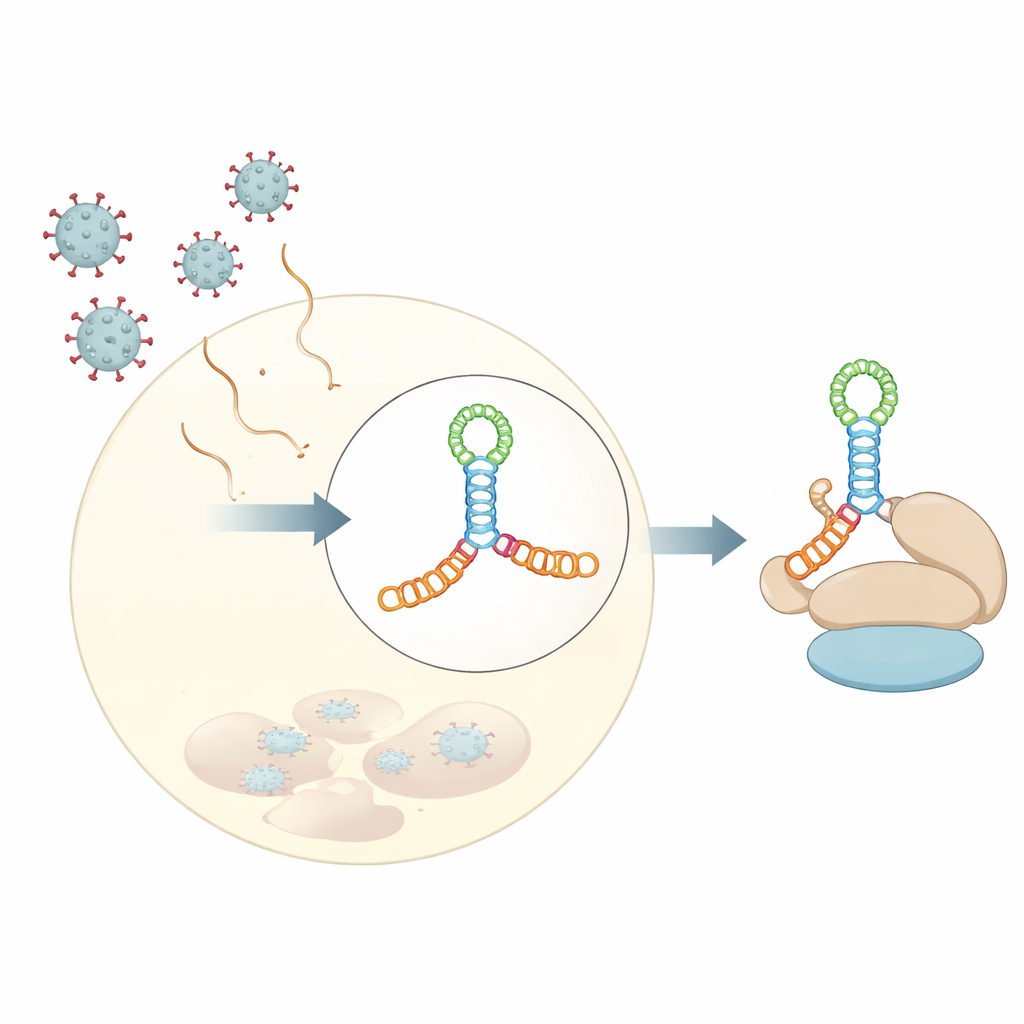
Vírus diferentes, mesmo plano estrutural
De maneira marcante, quando a equipe comparou essa estrutura com segmentos de RNA previamente resolvidos de outros dois picornavírus—o domínio JK do vírus encefalomielocardite e o domínio V do vírus da hepatite A—eles descobriram que a topologia tridimensional geral é praticamente a mesma, embora as sequências de RNA subjacentes variem consideravelmente. Em todos os três casos, uma alça rica em adeninas encaixa‑se na lateral de uma hélice próxima e organiza uma junção compacta onde dois troncos principais se empilham um sobre o outro. Esse arranjo recorrente parece ser um “motivo” estrutural que a evolução reutilizou entre espécies virais para apresentar aos fatores do hospedeiro uma superfície de ligação familiar, apesar da ampla variação de sequência e de pormenores finos.
Como o enovelamento viral captura um fator do hospedeiro
Para entender como essa forma de RNA compartilhada captura eIF4G, os pesquisadores mediram a ligação entre os RNAs virais e a região HEAT1 de eIF4G, um módulo curvado conhecido por contactar RNA. Os três domínios virais ligaram‑se à HEAT1 com afinidade na faixa de nanomolar, indicando interações muito fortes. Ao introduzir mutações direcionadas nas junções e alças do RNA, eles conseguiram enfraquecer ou abolir a ligação e identificar quais elementos eram mais importantes. Alterações que removeram pequenos ressaltos em hélices chave ou que perturbaram a alça rica em adeninas reduziram fortemente a ligação, embora os nucleotídeos mutados não sejam previstos como contatos diretos com a proteína. Isso sugere que a alça e os ressaltos atuam como vigas internas, fixando a orientação relativa das hélices empilhadas de modo que uma superfície lateral contínua fique perfeitamente modelada para o encaixe da HEAT1. 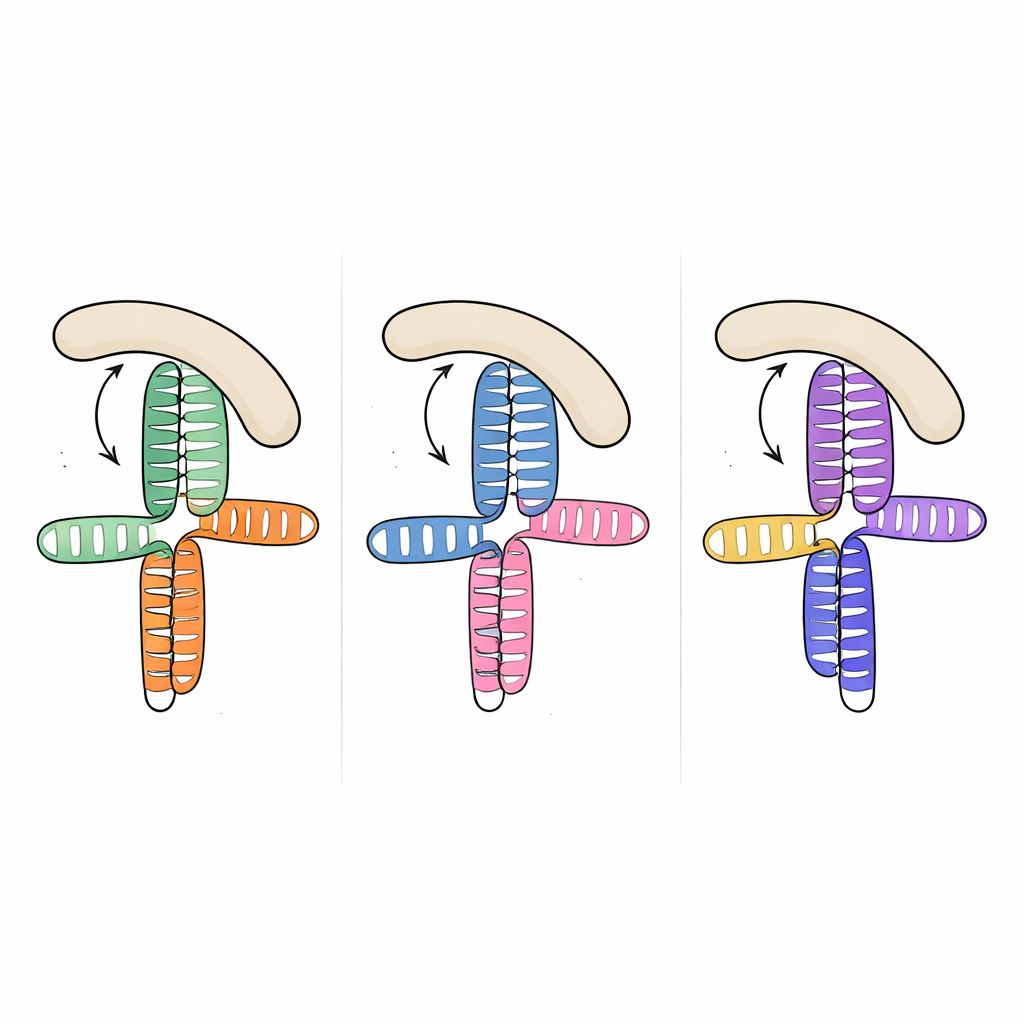
Mecânica compartilhada e novas possibilidades farmacológicas
Experimentos de footprinting químico, que mapeiam quais partes da espinha dorsal do RNA ficam protegidas quando a proteína está ligada, confirmaram que a HEAT1 contacta principalmente um lado das hélices empilhadas oposto à alça organizadora rica em adeninas, de modo que espelha de perto observações por criomicroscopia eletrônica para um dos outros vírus. Em conjunto, o trabalho mostra que vários picornavírus distintos usam uma estratégia estrutural comum: constroem andaimes de RNA semelhantes que apresentam características tridimensionais conservadas ao mesmo fator do hospedeiro, eIF4G, mesmo que as sequências em si variem. Para um público não especializado, a conclusão é que vírus de ramos diferentes da árvore evolutiva convergem para o mesmo truque de dobramento para se conectar à maquinaria de tradução celular. Como esse truque depende mais da forma do que da sequência, pode ser possível projetar fármacos ou moléculas que reconheçam e desativem essa arquitetura de RNA conservada, potencialmente bloqueando a produção de proteínas em múltiplas espécies virais com um único tratamento.
Citação: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Palavras-chave: estrutura do RNA viral, sítio de entrada interna do ribossomo, ligação a eIF4G, tradução de picornavírus, antivirais de amplo espectro