Clear Sky Science · fr
Les structures des domaines ARN liés à eIF4G parmi les types d’IRES picornaviraux sont topologiquement conservées
Comment certains virus détournent nos cellules
De nombreux virus courants, y compris ceux responsables des rhumes, des inflammations cardiaques et de l’hépatite, font face au même défi fondamental : comment tromper nos cellules pour qu’elles fabriquent des protéines virales plutôt que les leurs. Cette étude révèle, en détail atomique, comment un élément clé du matériel génétique viral se replie en une forme tridimensionnelle précise qui s’accroche à une protéine hôte et déclenche la production de protéines virales. Comprendre ce stratagème structural partagé entre différents virus pourrait indiquer la voie vers des médicaments antiviraux à large spectre qui les cibleraient tous en même temps.
Un point d’entrée spécial pour l’usine à protéines
La plupart de nos messages cellulaires (ARNm) commencent par une « coiffe » chimique qui aide à recruter la machinerie de fabrication des protéines. Nombre de virus à ARN de la famille des Picornaviridae n’ont pas cette coiffe, et pourtant ils parviennent à s’approprier la même machinerie. Ils le font grâce à des sites d’entrée ribosomiques internes, ou éléments IRES — segments d’ARN structurés situés près de l’extrémité 5′ du génome viral qui servent de points d’ancrage alternatifs pour le ribosome. Dans ces régions IRES, une section particulière, appelée domaine V dans plusieurs virus, se lie fortement à un facteur d’initiation de l’hôte nommé eIF4G, une sorte d’échafaudage qui organise d’autres composants nécessaires au démarrage de la synthèse protéique.
Un regard à haute résolution sur un nœud d’ARN viral
Les auteurs ont déterminé une structure cristalline à 3 angströms du domaine V du coxsackievirus B3, un virus souvent utilisé comme modèle pour les entérovirus humains. Plutôt que d’être une simple épingle à cheveux, cet ARN se replie en une jonction allongée à quatre voies — imaginez deux tiges empilées croisant une autre tige courte au centre, formant une jonction en H maintenue par une boucle riche en adénines. Ce nœud compact d’hélices positionne de petites saillies et boucles selon des angles précis pour constituer un échafaudage rigide. Des expériences en solution, notamment la diffusion des rayons X aux petits angles et le empreinte chimique, combinées à des outils modernes de prédiction de structure, ont montré que ce repliement n’est pas un artefact de cristallisation mais reflète le comportement de l’ARN en solution. 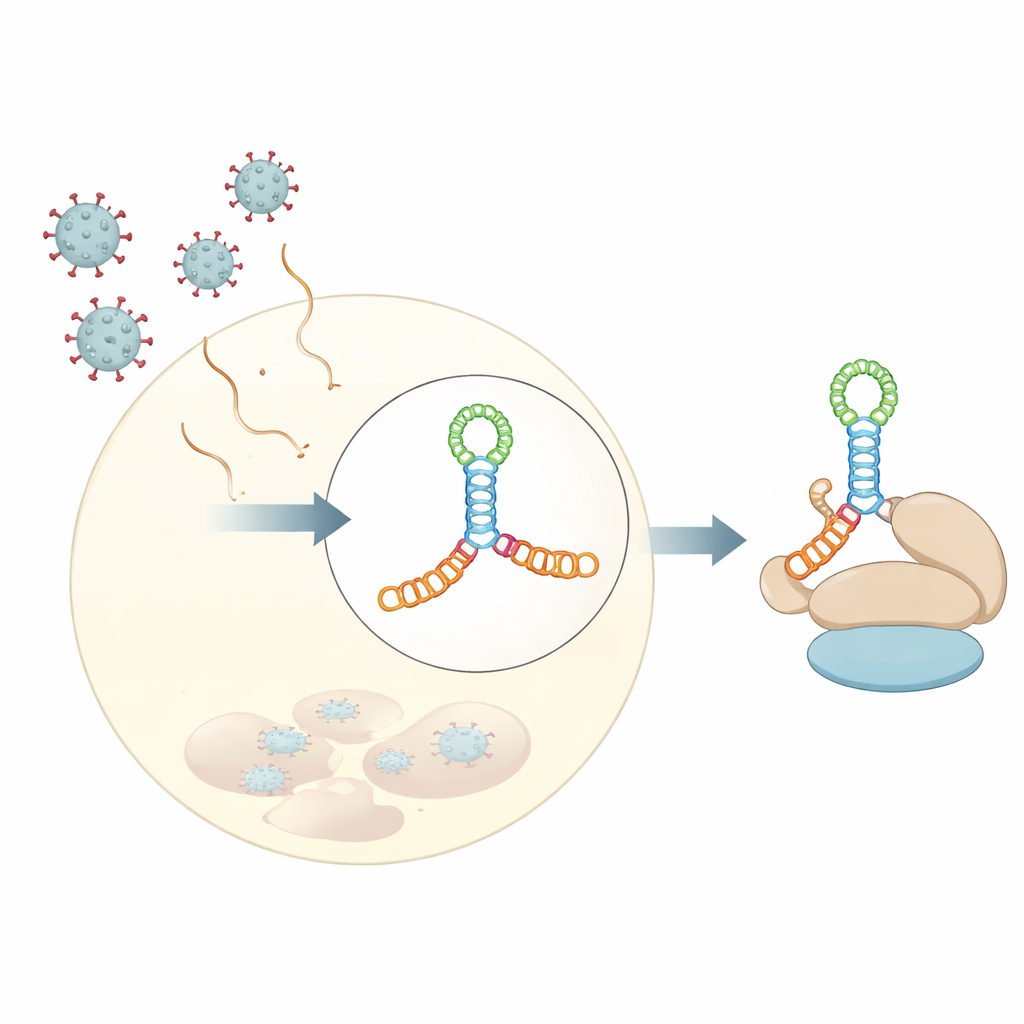
Des virus différents, le même plan structural
De manière frappante, lorsque l’équipe a comparé cette structure à des segments d’ARN précédemment résolus de deux autres picornavirus — le domaine JK du virus de l’encéphalomyocardite et le domaine V du virus de l’hépatite A — ils ont constaté que la topologie tridimensionnelle globale est presque identique, même si les séquences d’ARN sous-jacentes diffèrent considérablement. Dans les trois cas, une boucle riche en adénines s’insère sur le côté d’une hélice voisine et organise une jonction compacte où deux tiges principales s’empilent l’une sur l’autre. Cette architecture récurrente semble constituer un « motif » structural que l’évolution a réutilisé au sein des espèces virales pour présenter aux facteurs de l’hôte une surface de liaison familière, malgré une grande variation de séquence et de détails fins.
Comment le repliement viral capture un facteur de l’hôte
Pour comprendre comment cette forme d’ARN partagée attire eIF4G, les chercheurs ont mesuré la liaison entre les ARN viraux et la région HEAT1 d’eIF4G, un module courbé connu pour interagir avec l’ARN. Les trois domaines viraux se liaient à HEAT1 avec une affinité nanomolaire, c’est‑à‑dire des interactions très fortes. En introduisant des mutations ciblées dans les jonctions et boucles de l’ARN, ils ont pu affaiblir ou abolir la liaison et identifier les éléments les plus importants. Les modifications qui supprimaient de petites saillies dans des hélices clés ou perturbaient la boucle riche en adénines réduisaient fortement la liaison, alors même que les nucléotides mutés ne sont pas supposés toucher directement la protéine. Cela suggère que la boucle et les saillies agissent comme des montants internes, fixant l’orientation relative des hélices empilées de sorte qu’une surface latérale continue prenne la forme idéale pour l’ancrage de HEAT1. 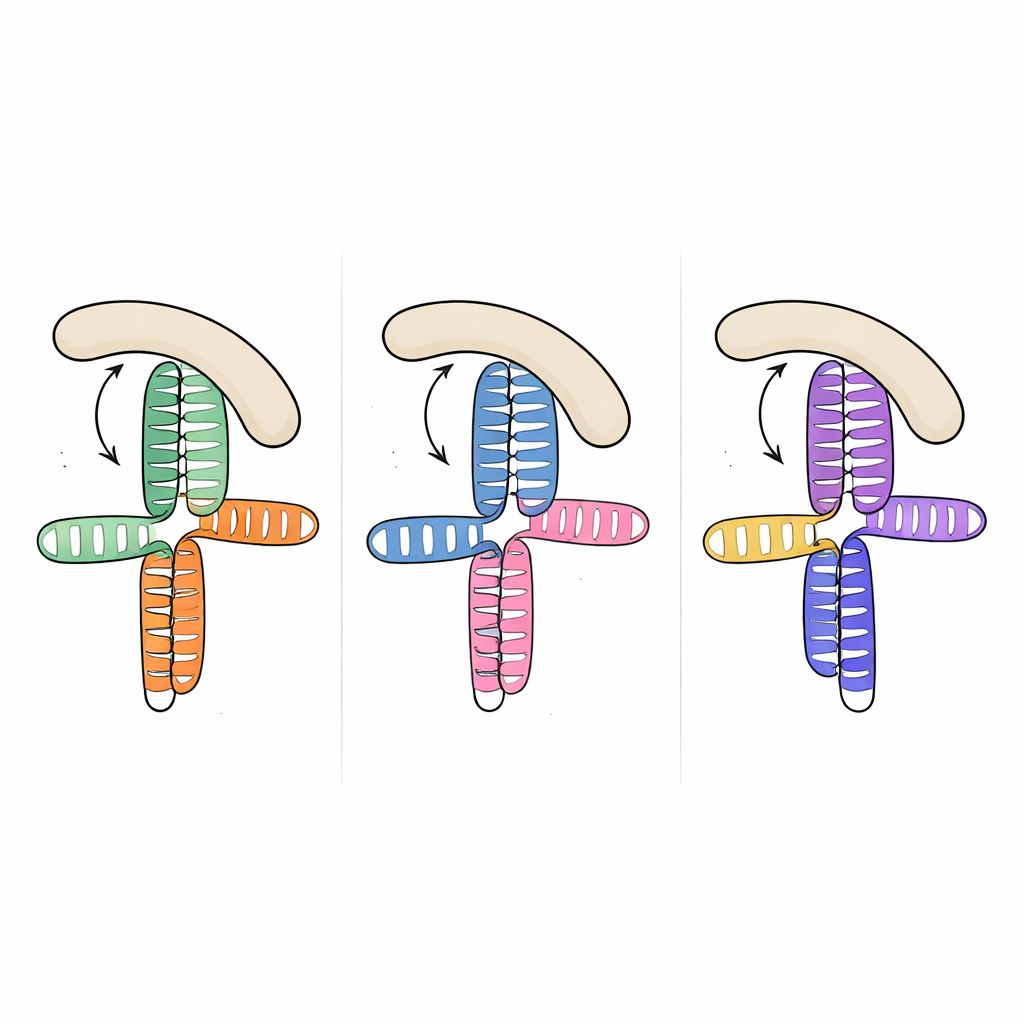
Mécanique partagée et nouvelles possibilités médicamenteuses
Les expériences d’empreinte chimique, qui cartographient quelles parties de l’épine dorsale de l’ARN sont protégées lorsque la protéine est liée, ont confirmé que HEAT1 contacte principalement un côté des hélices empilées opposé à la boucle organisatrice riche en adénines, d’une manière qui reflète de près des observations en cryo‑microscopie électronique pour l’un des autres virus. Pris ensemble, les résultats montrent que plusieurs picornavirus distincts utilisent une même stratégie structurelle : ils construisent des échafaudages ARN similaires qui présentent des caractéristiques tridimensionnelles conservées au même facteur de l’hôte, eIF4G, bien que les séquences varient. Pour un lecteur non spécialiste, la conclusion est que des virus issus de branches différentes de l’arbre évolutif convergent vers le même tour de pliage pour se brancher sur la machinerie de traduction de la cellule. Parce que ce tour repose davantage sur la forme que sur la séquence, il pourrait être possible de concevoir des médicaments ou des molécules qui reconnaissent et désactivent cette architecture ARN conservée, bloquant potentiellement la production de protéines à travers plusieurs espèces virales par un seul traitement.
Citation: Banna, H.A., Das, N.K., Kalinina, M. et al. Structures of the eIF4G-binding RNA domains among picornaviral IRES types are topologically conserved. Nat Commun 17, 2758 (2026). https://doi.org/10.1038/s41467-026-69554-2
Mots-clés: structure de l’ARN viral, site d’entrée ribosomique interne, liaison à eIF4G, traduction des picornavirus, antiviraux à large spectre