Clear Sky Science · zh
髓样巨噬细胞溶酶体TMEM175缺失通过炎症小体与交叉呈递通路发挥抗肿瘤免疫
将机体的清道夫转变为抗癌战士
癌症治疗越来越依赖唤醒免疫系统,但许多肿瘤仍能逃避免疫监视。本研究探讨免疫细胞内部一个出人意料的“刹车”——位于溶酶体上的离子通道TMEM175。作者在小鼠中通过特异性去除巨噬细胞中的TMEM175,发现肿瘤缩小、转移减少,并且对现有免疫疗法的应答更好。该工作提示了一种重塑肿瘤微环境的新途径,使免疫系统更有效识别并消灭癌细胞。
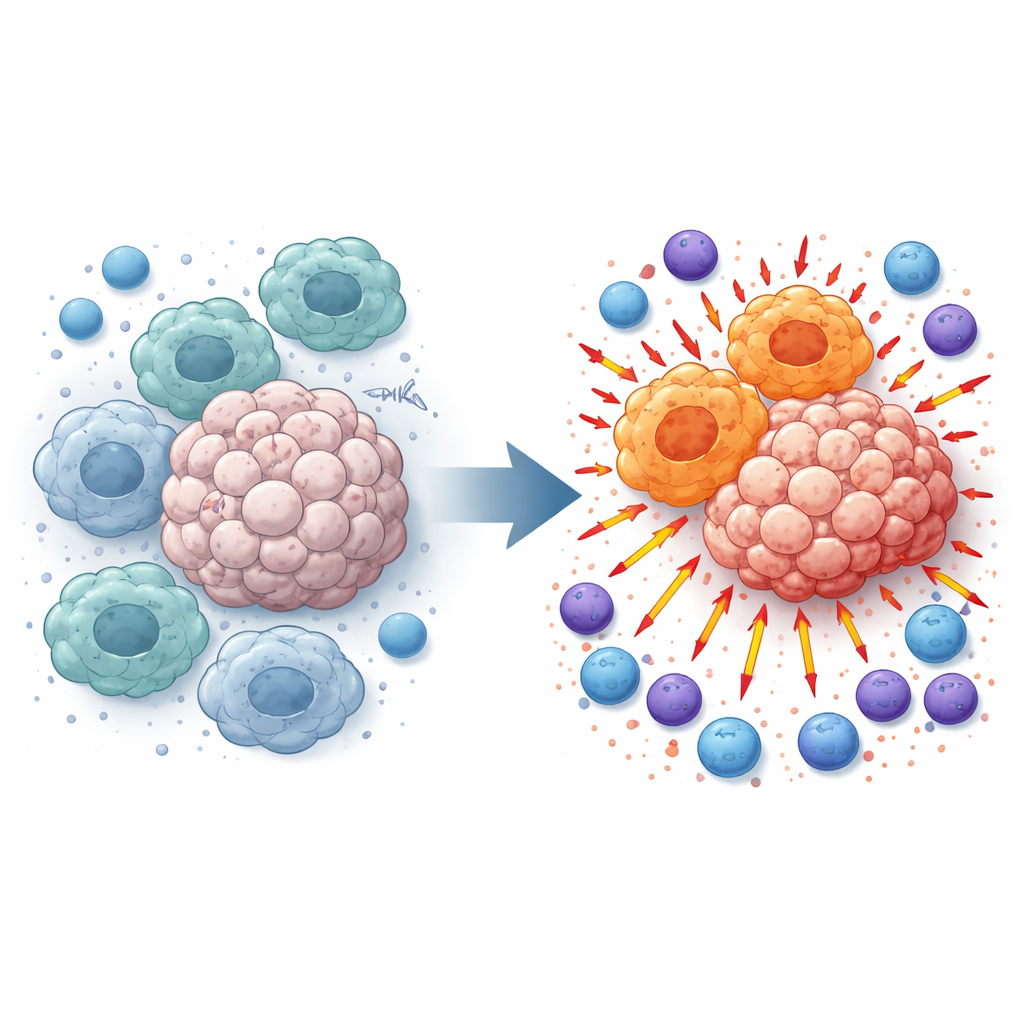
为什么某些免疫细胞会助长肿瘤生长
巨噬细胞在组织中巡逻并吞噬碎片,但在肿瘤内它们常被重编程为一种促进肿瘤生长的状态。这类“M2样”巨噬细胞抑制炎症并阻碍本可攻击肿瘤的T细胞和自然杀伤(NK)细胞。研究者在患者的黑色素瘤样本和带瘤小鼠中发现,肿瘤组织中的TMEM175水平高于邻近正常组织,并且与这一抑制性巨噬细胞表型密切相关。基于这一观察,他们提出问题:如果只在髓样细胞(如巨噬细胞)中关闭TMEM175,会发生什么?
移除溶酶体守门员使免疫天平倾斜
研究团队构建了在髓样细胞中特异性删除TMEM175的小鼠模型,并植入皮下黑色素瘤或肺癌细胞,或将肿瘤细胞注入血液以诱导肺转移。在这些模型中,TMEM175缺失小鼠的肿瘤增速更慢、转移结节更少。细胞学分析显示,肿瘤内的巨噬细胞向与强烈免疫活化相关的“M1样”谱系转变,而抑制性的M2样群体减少。与此同时,肿瘤组织中积累了更多的CD4和CD8 T细胞及NK细胞,并显示出被激活、准备杀伤的分子特征。
细胞碎片如何点燃强烈的免疫信号
为解析内在机制,研究者在体外培养的骨髓来源巨噬细胞中开展实验。当这些细胞吞噬肿瘤细胞的残片时,其溶酶体发生不稳定,泄漏如胱天蛋白酶B等酶类并改变周围液体的钙离子水平。在TMEM175缺失的巨噬细胞中,这种扰动更为显著,导致一种分子报警系统——NLRP3炎症小体被强烈激活。炎症小体一旦活化,就促使包括细胞因子IL‑1β和IL‑18在内的强效信使分子释放。抑制caspase‑1或用抗体中和IL‑1β或IL‑18,能在很大程度上消除TMEM175缺失在小鼠中带来的抗肿瘤益处,表明这一炎症级联反应是关键机制。
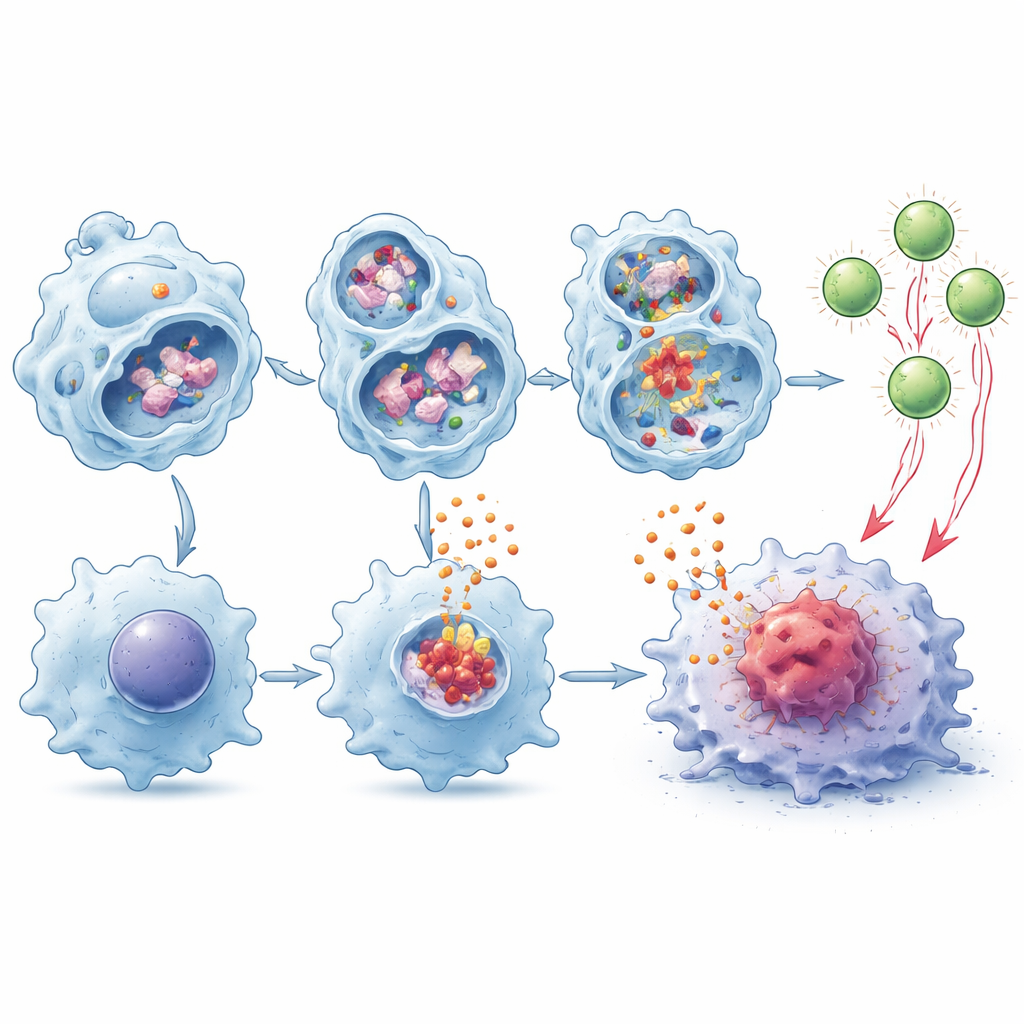
帮助T细胞识别并攻击肿瘤
巨噬细胞不仅释放警报信号——它们还能将肿瘤蛋白分解并在表面展示肽段以警示T细胞,这一过程称为交叉呈递。作者发现,TMEM175缺失的巨噬细胞在溶酶体内对肿瘤物质的降解更慢,因而保留更多完整片段可供呈递。在共培养实验中,这些细胞在驱动肿瘤特异性CD8 T细胞扩增和激活方面表现显著更优,并且在IL‑1β和IL‑18存在时这一效应更强。当将这些被有效“教育”的T细胞转移到缺乏自身CD8细胞的带瘤小鼠体内,它们比由正常巨噬细胞教育的T细胞更能有效减缓肿瘤生长。
增强检查点抑制疗法的效力
由于TMEM175缺失的肿瘤富含活化的T细胞,研究者测试了这种环境对抗‑PD‑1(一种广泛使用的检查点抑制剂)的反应。在对照小鼠中,抗‑PD‑1对黑色素瘤生长几乎无影响,反映出临床中常见的耐药情形。相比之下,在巨噬细胞中缺失TMEM175的小鼠接受相同药物后,肿瘤明显更小、肿瘤细胞死亡更多。其肿瘤内含有更多活化的巨噬细胞、T细胞和NK细胞,表明通过调控TMEM175重塑肿瘤微环境能够提高既有免疫疗法的疗效。
对肿瘤微环境的新操控点
总体而言,该研究揭示了TMEM175作为控制巨噬细胞对死亡肿瘤细胞反应的分子开关。当这一溶酶体离子通道缺失时,肿瘤碎片更易致溶酶体不稳定,细胞外钙水平升高,炎症小体被点燃,释放IL‑1β和IL‑18。与此同时,肿瘤蛋白降解变慢,提升了向CD8 T细胞呈递抗原的能力。上述改变将巨噬细胞从肿瘤的帮凶转变为强有力的盟友,动员T细胞和NK细胞对抗癌症,并使肿瘤对抗‑PD‑1疗法更为敏感。虽然能选择性阻断TMEM175并到达肿瘤相关巨噬细胞的药物仍需开发,但这项工作为联合癌症免疫疗法提供了一个有前景的新方向。
引用: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
关键词: 肿瘤微环境, 巨噬细胞, 炎症小体, 癌症免疫治疗, 抗原交叉呈递