Clear Sky Science · de
Mangel an lysosomalem TMEM175 in myeloiden Makrophagen vermittelt Anti-Tumor-Immunität über Inflammasom- und Kreuzpräsentationswege
Das körpereigene Aufräumkommando zu Krebsbekämpfern machen
Die Krebsbehandlung setzt zunehmend darauf, das Immunsystem zu aktivieren, doch viele Tumoren entgehen weiterhin unseren Abwehrmechanismen. Diese Studie untersucht eine unerwartete Bremse in Immunzellen — einen Ionenkanal namens TMEM175, der auf kleinen Recycling-Kompartimenten, den Lysosomen, sitzt. Durch das Entfernen von TMEM175 speziell in Makrophagen, der zellulären Aufräumtruppe des Körpers, zeigen die Autoren an Mäusen, dass Tumoren schrumpfen, sich weniger ausbreiten und besser auf bestehende Immuntherapien ansprechen. Die Arbeit deutet auf einen neuen Weg hin, die Tumormikroumgebung so umzuprogrammieren, dass das Immunsystem Krebszellen effektiver erkennt und zerstört.
Warum bestimmte Immunzellen Tumoren unterstützen können
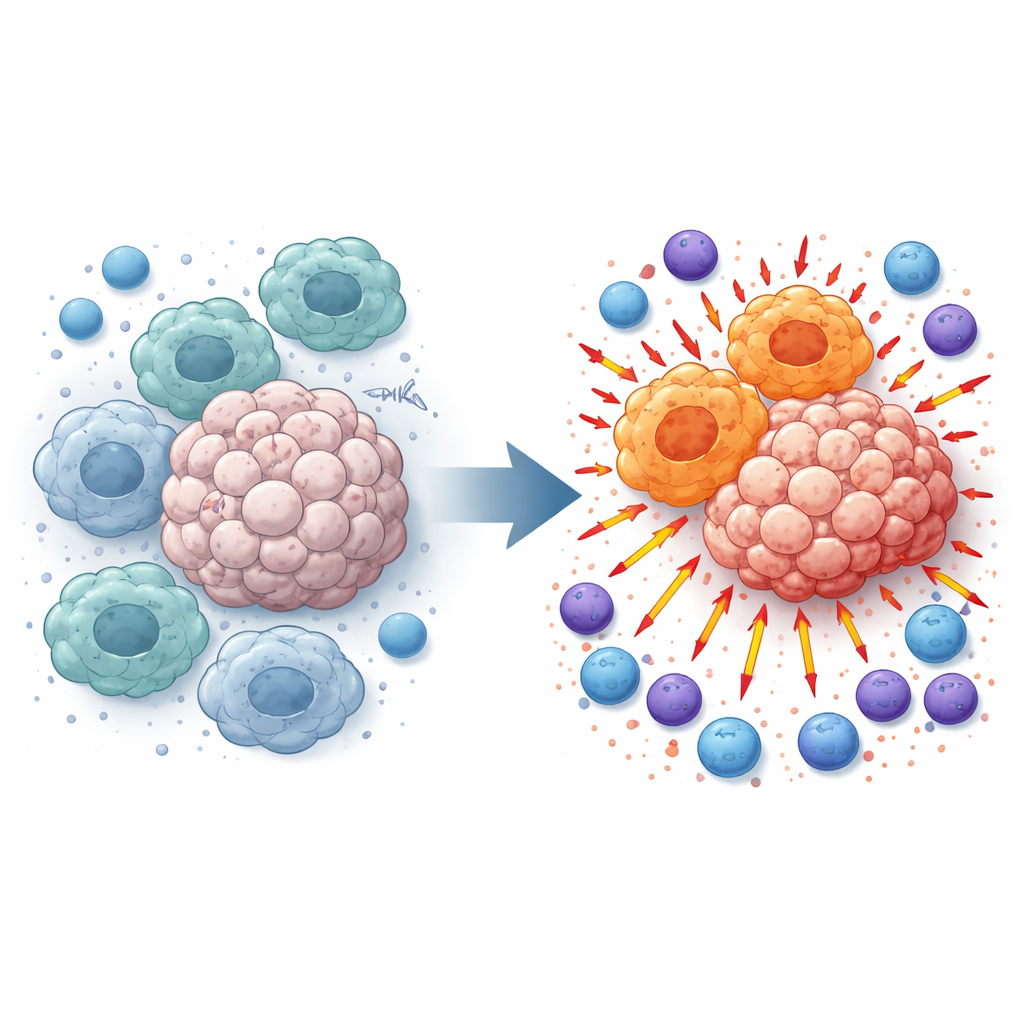
Makrophagen patrouillieren im Gewebe und fressen Zelltrümmer, doch innerhalb von Tumoren werden sie häufig umprogrammiert und nehmen einen nährenden, tumorfreundlichen Zustand ein. Diese „M2‑ähnlichen“ Makrophagen dämpfen Entzündungen und behindern T‑Zellen sowie natürliche Killerzellen (NK), die sonst Krebs angreifen würden. Bei der Untersuchung von Melanomproben von Patientinnen und Patienten sowie tumorbefallenen Mäusen stellten die Forschenden fest, dass die TMEM175‑Spiegel in Tumoren höher waren als im umgebenden Normalgewebe und eng mit diesem suppressiven Makrophagenzustand verknüpft waren. Diese Beobachtung führte zu der Frage: Was passiert, wenn TMEM175 nur in myeloiden Zellen wie Makrophagen ausgeschaltet wird?
Entfernt man einen lysosomalen Türsteher, verschiebt sich das Gleichgewicht
Das Team erzeugte Mäuse, in denen TMEM175 spezifisch in myeloiden Zellen gelöscht ist, und implantierte dann Melanom- oder Lungenkrebszellen unter die Haut oder injizierte sie in die Blutbahn, um Lungenmetastasen zu provozieren. In all diesen Modellen wuchsen Tumoren in TMEM175‑defizienten Mäusen langsamer und bildeten weniger metastatische Herde. Detaillierte Zellanalysen zeigten, dass sich die Makrophagen in diesen Tumoren in Richtung eines „M1‑ähnlichen“ Profils verschoben, das mit starker Immunaktivierung assoziiert ist, während die suppressive M2‑ähnliche Population abnahm. Gleichzeitig rekrutierten sich deutlich mehr CD4‑ und CD8‑T‑Zellen sowie NK‑Zellen in das Tumorgewebe und zeigten molekulare Zeichen von Aktivierung und Bereitschaft zur Eliminierung.
Wie Zelltrümmer ein heftiges Immun-Signal auslösen
Um die zugrundeliegenden Mechanismen aufzudecken, untersuchten die Forschenden aus dem Knochenmark gewonnene Makrophagen im Kulturmodell. Wenn diese Zellen Fragmente toter Tumorzellen aufnahmen, wurden ihre Lysosomen destabilisiert, sodass Enzyme wie Cathepsin B austraten und sich die Calciumspiegel in der Umgebung veränderten. In TMEM175‑defizienten Makrophagen war diese Störung stärker ausgeprägt, was zur robusten Aktivierung eines molekularen Alarmsystems namens NLRP3‑Inflammasom führte. Ist dieses aktiviert, löst der mehrteilige Proteinkomplex die Freisetzung potenter Botenstoffe aus, darunter die Zytokine IL‑1β und IL‑18. Die Blockade der Caspase‑1 oder die Neutralisierung von IL‑1β bzw. IL‑18 mit Antikörpern tilgte weitgehend den Anti-Tumor-Effekt des TMEM175‑Verlusts in Mäusen, was zeigt, dass diese entzündliche Kaskade zentral für die Wirkung ist.
T‑Zellen helfen, Tumoren zu sehen und anzugreifen
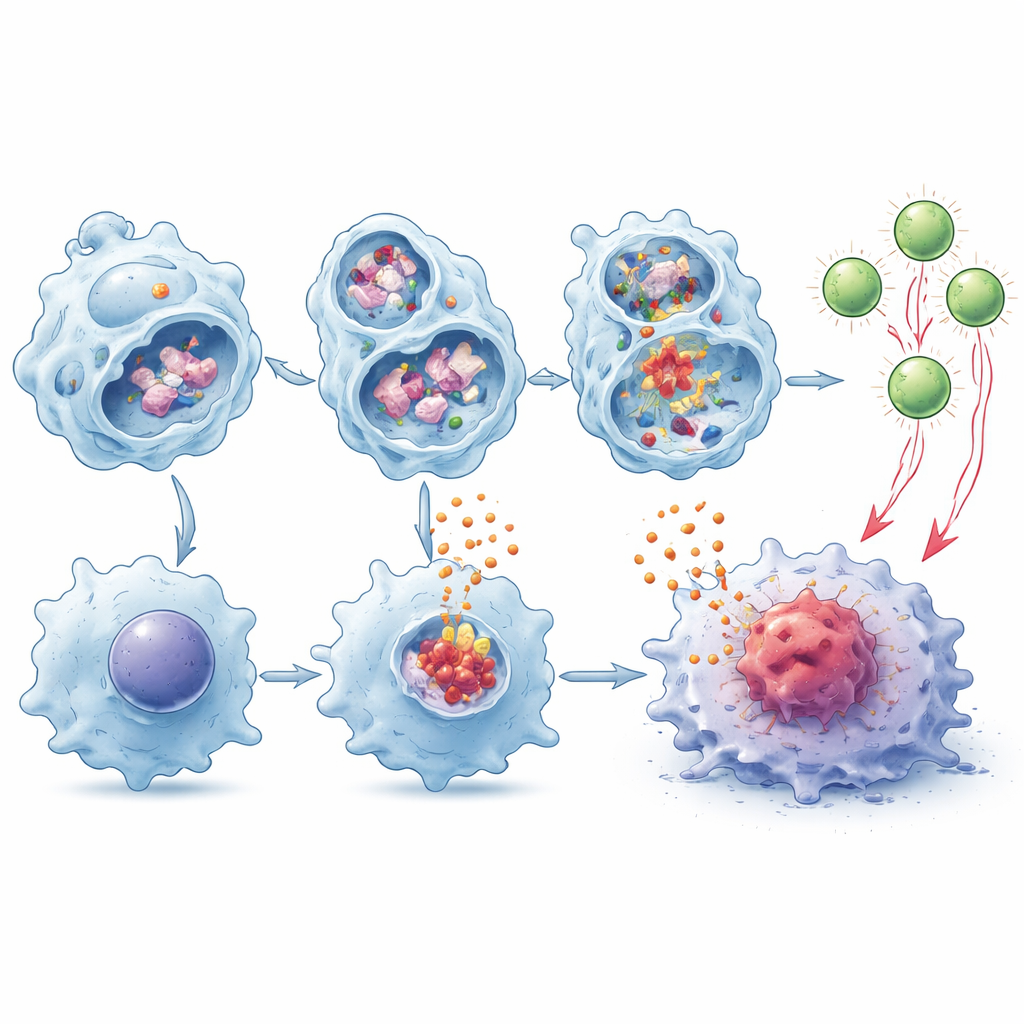
Makrophagen tun mehr, als Alarmzeichen auszusenden — sie können Tumorproteine zerkleinern und Fragmente an ihrer Oberfläche präsentieren, um T‑Zellen zu alarmieren, ein Prozess, der als Kreuzpräsentation bekannt ist. Die Autoren fanden, dass TMEM175‑defiziente Makrophagen Tumormaterial langsamer in den Lysosomen abbauten, sodass mehr intakte Stücke für die Präsentation verfügbar blieben. In Ko-Kultur‑Experimenten waren diese Zellen deutlich besser darin, die Expansion und Aktivierung tumorspezifischer CD8‑T‑Zellen zu fördern, und dieser Effekt verstärkte sich noch in Gegenwart von IL‑1β und IL‑18. Wurden solche primed T‑Zellen in tumorbefallene Mäuse ohne eigene CD8‑Zellen übertragen, verlangsamten sie das Tumorwachstum effektiver als T‑Zellen, die von normalen Makrophagen „gebildet“ worden waren.
Die Wirksamkeit von Checkpoint‑Therapie steigern
Da TMEM175‑defiziente Tumoren reich an aktiven T‑Zellen waren, prüften die Forschenden, ob dieses Umfeld anders auf Anti‑PD‑1 — einen weit verbreiteten Checkpoint‑Inhibitor — reagiert. In normalen Mäusen beeinflusste Anti‑PD‑1 das Melanomwachstum kaum, was die in der Klinik häufig beobachtete Resistenz widerspiegelt. Im Gegensatz dazu zeigten Mäuse ohne TMEM175 in Makrophagen bei gleicher Behandlung deutlich kleinere Tumoren und mehr Tumorzellsterben. Ihre Tumoren enthielten mehr aktivierte Makrophagen, T‑Zellen und NK‑Zellen, was darauf hinweist, dass die Umgestaltung der Tumormikroumgebung über TMEM175 etablierte Immuntherapien wirksamer macht.
Ein neuer Ansatzpunkt für die Tumormikroumgebung
Insgesamt zeigt die Studie TMEM175 als molekularen Schalter, der steuert, wie Makrophagen auf sterbende Tumorzellen reagieren. Fehlt dieser lysosomale Ionenkanal, destabilisieren Tumortrümmer Lysosomen leichter, Calciumspiegel steigen und das Inflammasom feuert, wodurch IL‑1β und IL‑18 freigesetzt werden. Gleichzeitig verbessert die verlangsamte Degradation von Tumorproteinen deren Präsentation an CD8‑T‑Zellen. Zusammengenommen verwandeln diese Änderungen Makrophagen von Tumorkomplizen zu starken Verbündeten, die T‑Zellen und NK‑Zellen gegen Krebs mobilisieren und Tumoren für Anti‑PD‑1‑Therapie sensibilisieren. Obwohl noch Wirkstoffe entwickelt werden müssen, die TMEM175 selektiv hemmen und tumorassoziierte Makrophagen erreichen, weist die Arbeit auf eine vielversprechende neue Richtung für kombinatorische Krebsimmuntherapien hin.
Zitation: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Schlüsselwörter: Tumormikroumgebung, Makrophagen, Inflammasom, Krebsimmuntherapie, Antigen-Kreuzpräsentation