Clear Sky Science · fr
Déficit en TMEM175 lysosomal dans les macrophages myéloïdes exerce une immunité anti‑tumorale via l’inflammasome et la voie de présentation croisée
Transformer l’équipe de nettoyage du corps en combattants du cancer
Le traitement du cancer repose de plus en plus sur le réveil du système immunitaire, pourtant de nombreuses tumeurs échappent encore à nos défenses. Cette étude explore un frein inattendu au sein des cellules immunitaires : un canal ionique nommé TMEM175 situé sur de petits compartiments de recyclage appelés lysosomes. En supprimant TMEM175 spécifiquement dans les macrophages, l’équipe montre chez la souris que les tumeurs rétrécissent, se propagent moins et répondent mieux aux immunothérapies existantes. Ce travail suggère une nouvelle façon de reconfigurer le microenvironnement tumoral pour que le système immunitaire puisse mieux reconnaître et détruire les cellules cancéreuses.
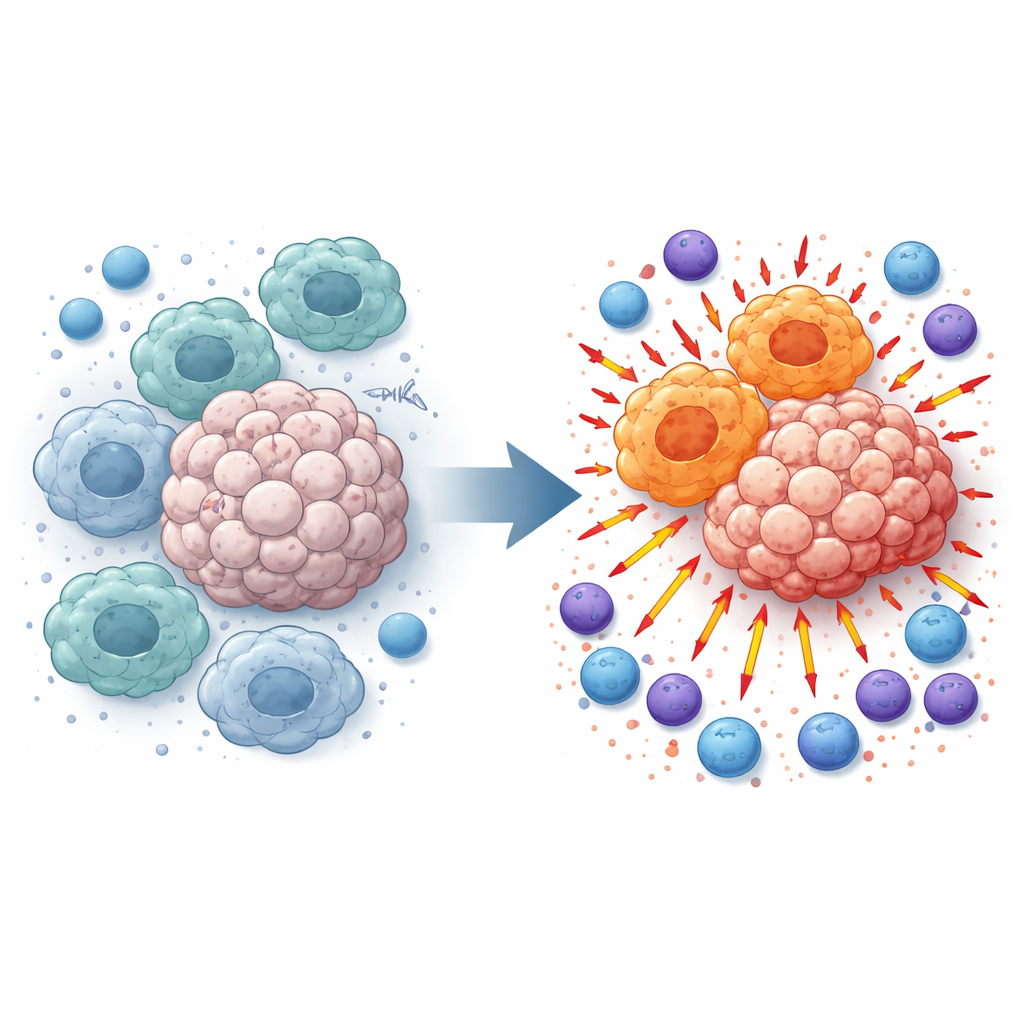
Pourquoi certains effecteurs immunitaires favorisent la croissance tumorale
Les macrophages patrouillent les tissus et engloutissent les débris, mais au sein des tumeurs ils sont souvent reprogrammés dans un état nourricier, favorable à la tumeur. Ces macrophages de type « M2 » atténuent l’inflammation et entravent les cellules T et les cellules NK qui autrement attaqueraient le cancer. En examinant des échantillons de mélanome de patients et de souris porteuses de tumeurs, les chercheurs ont constaté que les niveaux de TMEM175 étaient plus élevés dans les tumeurs que dans le tissu normal adjacent et étaient étroitement liés à cet état macrophagique suppressif. Cette observation les a amenés à se demander : que se passe‑t‑il si TMEM175 est désactivé uniquement dans les cellules myéloïdes telles que les macrophages ?
Supprimer un gardien lysosomal fait pencher la balance
L’équipe a généré des souris chez lesquelles TMEM175 est supprimé spécifiquement dans les cellules myéloïdes, puis a implanté des cellules de mélanome ou de cancer du poumon sous la peau, ou les a injectées dans la circulation pour provoquer des métastases pulmonaires. Dans ces modèles, les tumeurs des souris déficientes en TMEM175 croissaient plus lentement et formaient moins de nodules métastatiques. Des analyses cellulaires détaillées ont montré que les macrophages intratumoraux basculaient vers un profil « M1 » associé à une forte activation immunitaire, tandis que la population suppressive de type M2 diminuait. Parallèlement, beaucoup plus de cellules T CD4 et CD8 ainsi que de cellules NK s’accumulaient dans le tissu tumoral et présentaient des signes moléculaires d’activation prêtes à tuer.
Comment les débris cellulaires déclenchent un signal inflammatoire puissant
Pour comprendre les mécanismes, les chercheurs ont étudié des macrophages dérivés de moelle osseuse en culture. Lorsque ces cellules ingéraient des fragments de cellules tumorales mortes, leurs lysosomes se déstabilisaient, fuyant des enzymes comme la cathépsine B et modifiant les niveaux de calcium dans le milieu environnant. Dans les macrophages déficients en TMEM175, cette perturbation était plus marquée, conduisant à une activation robuste d’un système d’alarme moléculaire appelé l’inflammasome NLRP3. Une fois activé, ce complexe multiprotéique déclenche la libération de messagers puissants, dont les cytokines IL‑1β et IL‑18. Bloquer l’enzyme caspase‑1, ou neutraliser IL‑1β ou IL‑18 par des anticorps, annulait en grande partie le bénéfice anti‑tumoral de la perte de TMEM175 chez la souris, montrant que cette cascade inflammatoire est centrale pour l’effet.
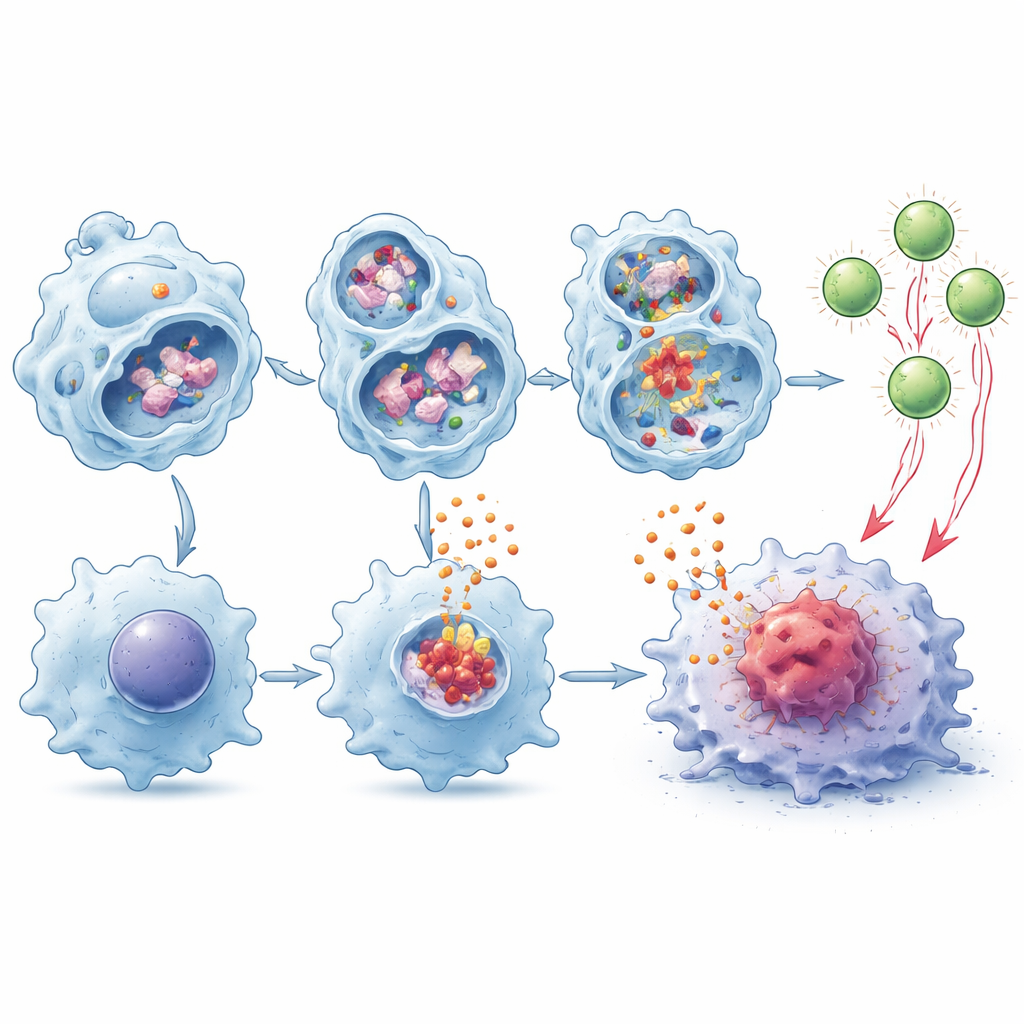
Aider les cellules T à voir et attaquer les tumeurs
Les macrophages font plus que sécréter des signaux d’alerte : ils peuvent aussi découper les protéines tumorales et exposer des fragments à leur surface pour alerter les cellules T, un processus appelé présentation croisée. Les auteurs ont constaté que les macrophages déficients en TMEM175 dégradaient le matériel tumoral plus lentement à l’intérieur des lysosomes, laissant davantage de fragments intacts disponibles pour être présentés. Dans des co‑cultures, ces cellules stimulaient beaucoup mieux l’expansion et l’activation des cellules T CD8 spécifiques de la tumeur, et cet effet était renforcé en présence d’IL‑1β et d’IL‑18. Lorsque des cellules T ainsi primées étaient transférées dans des souris porteuses de tumeurs dépourvues de leurs propres cellules CD8, elles ralentissaient la croissance tumorale plus efficacement que les cellules T éduquées par des macrophages normaux.
Renforcer l’efficacité de la thérapie par inhibiteur de point de contrôle
Comme les tumeurs déficientes en TMEM175 étaient riches en cellules T actives, les chercheurs ont testé si ce contexte répondrait différemment à l’anti‑PD‑1, un inhibiteur de point de contrôle largement utilisé. Chez des souris normales, l’anti‑PD‑1 affectait à peine la croissance du mélanome, reflétant la résistance souvent observée en clinique. En revanche, les souris dépourvues de TMEM175 dans leurs macrophages présentaient des tumeurs nettement plus petites et davantage de mort cellulaire tumorale lors du traitement par le même médicament. Leurs tumeurs contenaient plus de macrophages activés, de cellules T et de cellules NK, indiquant que remodeler le microenvironnement tumoral via TMEM175 rend l’immunothérapie établie plus efficace.
Une nouvelle prise sur le microenvironnement tumoral
Dans l’ensemble, l’étude révèle TMEM175 comme un interrupteur moléculaire qui contrôle la façon dont les macrophages répondent aux cellules tumorales mourantes. En l’absence de ce canal ionique lysosomal, les débris tumoraux déstabilisent plus facilement les lysosomes, les taux de calcium augmentent et l’inflammasome s’enclenche, libérant IL‑1β et IL‑18. Parallèlement, le ralentissement de la dégradation des protéines tumorales améliore leur présentation aux cellules T CD8. Ensemble, ces changements transforment les macrophages d’acolytes de la tumeur en puissants alliés qui mobilisent les cellules T et NK contre le cancer et sensibilisent les tumeurs à l’anti‑PD‑1. Bien que des médicaments bloquant sélectivement TMEM175 et ciblant les macrophages associés aux tumeurs restent à développer, ce travail ouvre une voie prometteuse pour des immunothérapies combinées contre le cancer.
Citation: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Mots-clés: microenvironnement tumoral, macrophages, inflammasome, immunothérapie du cancer, présentation croisée d’antigènes