Clear Sky Science · pl
Niedobór lizosomalnego TMEM175 w makrofagach mieloidalnych wywołuje odporność przeciwnowotworową poprzez inflammasom i ścieżkę prezentacji krzyżowej
Przekształcanie komórkowej brygady sprzątającej w pogromców raka
Leczenie nowotworów coraz częściej polega na pobudzeniu układu odpornościowego, jednak wiele guzów wciąż umyka naszym mechanizmom obronnym. W pracy tej badano nieoczekiwany hamulec wewnątrz komórek odpornościowych — kanał jonowy TMEM175 zlokalizowany w niewielkich kompartmentach recyklingowych, zwanych lizosomami. Usuwając TMEM175 specyficznie z makrofagów, komórek pełniących rolę wewnątrzorganizacyjnej „brygady sprzątającej”, autorzy wykazali na modelu myszy, że guzy ulegają zmniejszeniu, mniej przerzutują i lepiej odpowiadają na istniejącą immunoterapię. Praca sugeruje nowy sposób przesterowania mikrośrodowiska guza, by układ odpornościowy sprawniej rozpoznawał i niszczył komórki nowotworowe.
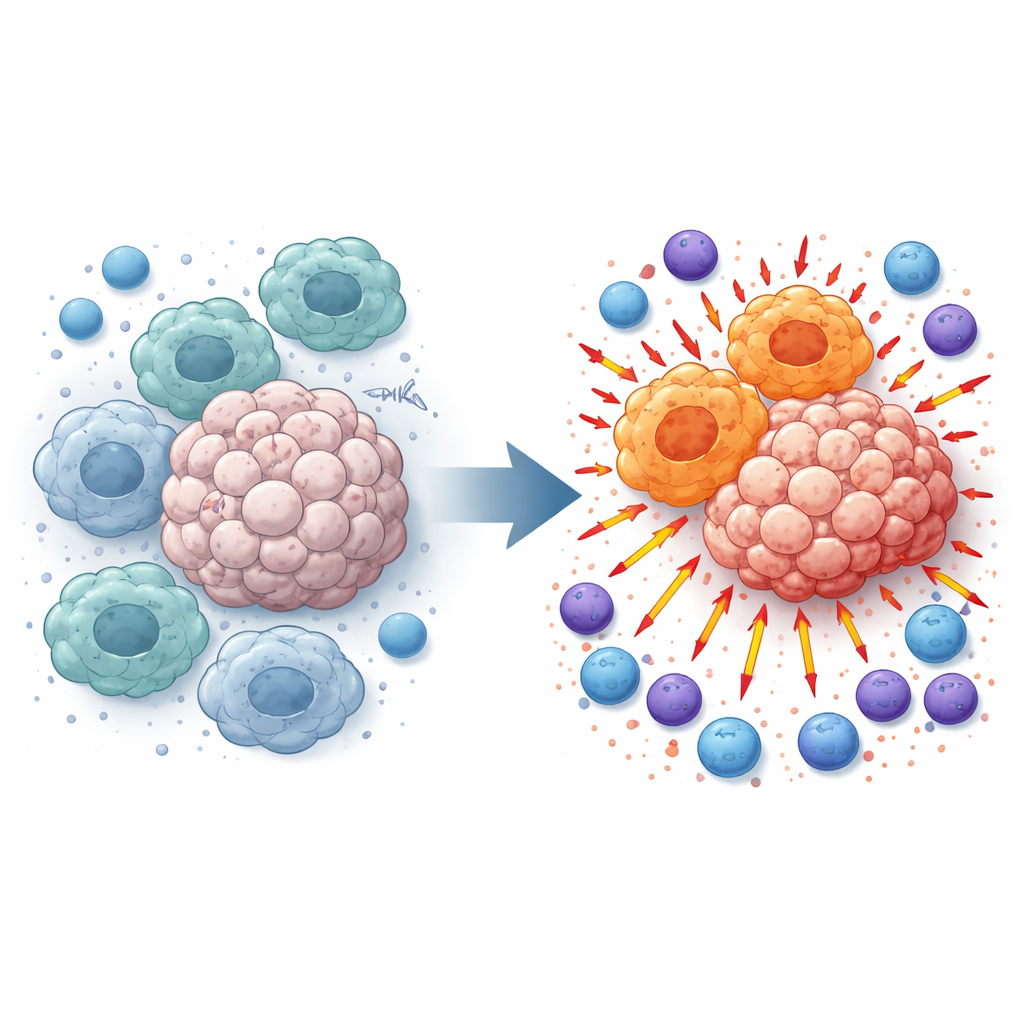
Dlaczego pewne komórki odpornościowe mogą wspierać wzrost guza
Makrofagi patrolują tkanki i pochłaniają zanieczyszczenia, lecz w obrębie guza często zostają przeprogramowane do stanu wspierającego nowotwór. Takie makrofagi o profilu „M2‑podobnym” tłumią zapalenie i hamują komórki T oraz naturalne komórki zabójcze (NK), które mogłyby atakować raka. Analiza próbek czerniaka od pacjentów oraz tkanek od myszy z guzami wykazała, że poziomy TMEM175 były wyższe w guzach niż w sąsiedniej tkance prawidłowej i silnie skorelowane z tym supresyjnym fenotypem makrofagów. To spostrzeżenie skłoniło badaczy do pytania: co się stanie, jeśli TMEM175 zostanie wyłączony tylko w komórkach mieloidalnych, takich jak makrofagi?
Usunięcie lizosomalnego strażnika przechyla szalę
Zespół wygenerował myszy, w których TMEM175 usunięto specyficznie w komórkach mieloidalnych, a następnie wszczepiał komórki czerniaka lub raka płuca pod skórę albo podawał do krwi, by wywołać przerzuty płucne. W tych modelach guzy u myszy pozbawionych TMEM175 rosły wolniej i tworzyły mniej ognisk przerzutowych. Szczegółowe analizy komórkowe wykazały, że makrofagi w obrębie tych guzów przesunęły się ku profilowi „M1‑podobnemu” związanym z silną aktywacją immunologiczną, podczas gdy populacja supresyjnych makrofagów M2 zmalała. Równocześnie w tkance guza gromadziło się znacznie więcej komórek CD4 i CD8 oraz komórek NK, które wykazywały molekularne cechy aktywacji i gotowości do zabijania.
Jak szczątki komórkowe wzniecają zapalny sygnał
Aby odkryć mechanizmy, badacze przeanalizowali makrofagi pochodzące z szpiku w hodowlach. Gdy te komórki połykały fragmenty martwych komórek nowotworowych, ich lizosomy ulegały destabilizacji, co prowadziło do wycieku enzymów, takich jak katepsyna B, oraz zmian stężenia wapnia w otaczającym środowisku. W makrofagach pozbawionych TMEM175 ten zaburzenia były silniejsze, co skutkowało silną aktywacją molekularnego systemu alarmowego zwanego inflammasomem NLRP3. Po uruchomieniu ten kompleks wielobiałkowy wyzwala uwalnianie silnych mediatorów, w tym cytokin IL‑1β i IL‑18. Zablokowanie enzymu kaspazy‑1 lub unieczynnienie IL‑1β albo IL‑18 za pomocą przeciwciał w dużej mierze znosiło przeciwnowotworową korzyść wynikającą z utraty TMEM175 u myszy, pokazując że ten kaskadowy proces zapalny jest kluczowy dla efektu.
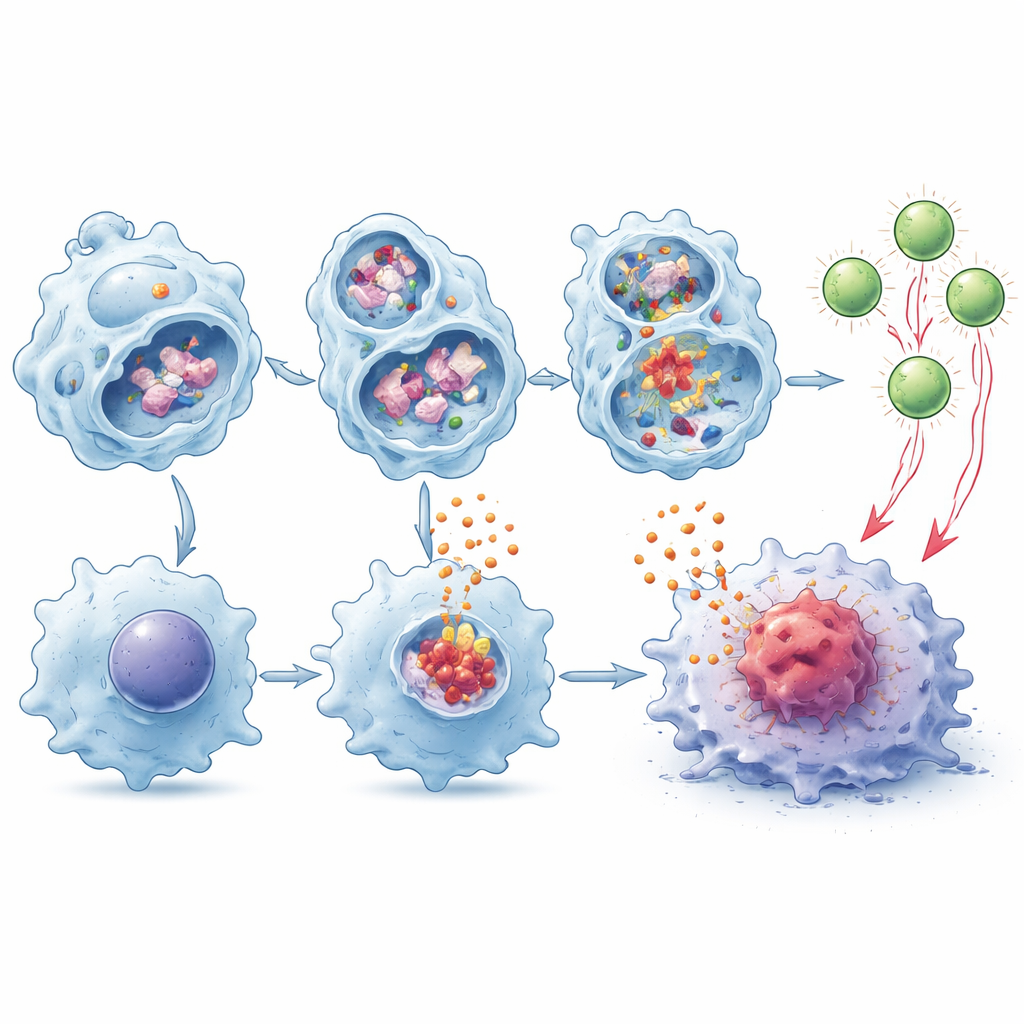
Pomaganie komórkom T widzieć i atakować guzy
Makrofagi robią więcej niż wydzielają sygnały alarmowe — potrafią także rozkładać białka nowotworowe i eksponować fragmenty na swojej powierzchni, by uczulić komórki T, proces znany jako prezentacja krzyżowa. Autorzy odkryli, że makrofagi pozbawione TMEM175 rozkładały materiał nowotworowy wolniej w lizosomach, pozostawiając więcej nienaruszonych fragmentów dostępnych do prezentacji. W eksperymentach współhodowli te komórki znacznie lepiej napędzały ekspansję i aktywację swoistych dla guza komórek CD8, a efekt ten nasilał się w obecności IL‑1β i IL‑18. Gdy takie „wyszkolone” komórki T przeszczepiono do myszy z guzami, które same nie miały komórek CD8, hamowały wzrost guza skuteczniej niż komórki T wyedukowane przez normalne makrofagi.
Wzmacnianie skuteczności terapii hamujących punkty kontrolne
Ponieważ guzy pozbawione TMEM175 obfitowały w aktywne komórki T, badacze sprawdzili, czy taki stan wpłynie na odpowiedź na anty‑PD‑1, powszechnie stosowany inhibitor punktu kontrolnego. U standardowych myszy anty‑PD‑1 prawie nie wpływał na wzrost czerniaka, co odzwierciedla oporność często obserwowaną w klinice. Natomiast myszy z brakiem TMEM175 w makrofagach wykazywały wyraźnie mniejsze guzy i więcej obumarłych komórek nowotworowych po podaniu tego samego leku. Ich guzy zawierały więcej aktywowanych makrofagów, komórek T i komórek NK, co wskazuje, że przekształcenie mikrośrodowiska guza przez TMEM175 poprawia skuteczność istniejącej immunoterapii.
Nowa dźwignia na mikrośrodowisko guza
Podsumowując, badanie ujawnia TMEM175 jako molekularny przełącznik sterujący reakcją makrofagów na obumierające komórki nowotworowe. Gdy ten lizosomalny kanał jonowy jest nieobecny, szczątki guza łatwiej destabilizują lizosomy, wzrasta stężenie wapnia, a inflammasom zostaje uruchomiony, uwalniając IL‑1β i IL‑18. Równocześnie wolniejsze trawienie białek nowotworowych poprawia ich prezentację komórkom CD8. Wspólnie te zmiany przekształcają makrofagi z pomocników guza w silnych sprzymierzeńców, którzy mobilizują komórki T i NK przeciw rakowi oraz uczulają guzy na terapię anty‑PD‑1. Choć leki selektywnie blokujące TMEM175 i trafiające do makrofagów związanych z guzem wciąż wymagają opracowania, praca wskazuje obiecujący kierunek dla terapii skojarzonej w immunoterapii nowotworów.
Cytowanie: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Słowa kluczowe: mikrośrodowisko guza, makrofagi, inflammasom, immunoterapia nowotworów, prezentacja antygenu krzyżowa