Clear Sky Science · tr
Myeloid makrofajlarda lizozomal TMEM175 eksikliği, inflammasom ve çapraz sunum yoluyla anti-tümör bağışıklığı sağlar
Vücudun Temizlik Ekibini Kanser Savaşçılarına Dönüştürmek
Kanser tedavisi giderek bağışıklık sistemini uyandırmaya dayanıyor, ancak birçok tümör hâlâ savunmamızdan sıyrılıyor. Bu çalışma, lizozom adı verilen küçük geri dönüşüm bölmelerinde yer alan bir iyon kanalı olan TMEM175 adlı immün hücre içi beklenmedik bir fren mekanizmasını araştırıyor. TMEM175’i özellikle makrofajlardan kaldırarak —vücudun hücresel temizlik ekibi— yazarlar fare modellerinde tümörlerin küçüldüğünü, daha az yayıldığını ve mevcut immünoterapiye daha iyi yanıt verdiğini gösteriyor. Bu çalışma, tümör mikroçevresini yeniden kablolamanın ve böylece bağışıklık sisteminin kanser hücrelerini daha etkili tanıyıp yok etmesinin yeni bir yolunu öneriyor.
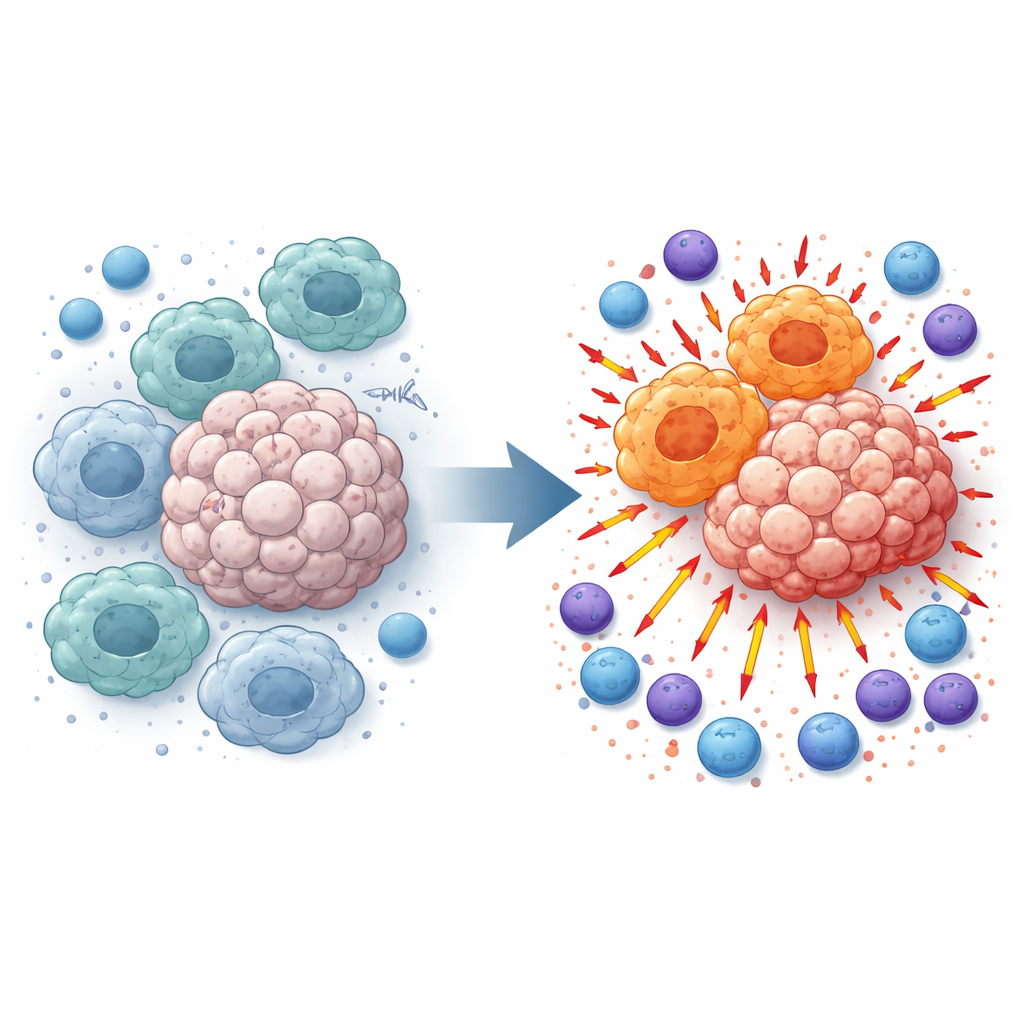
Neden Bazı İmmün Hücreler Tümörlere Yardım Eder?
Makrofajlar dokularda devriye gezer ve artık maddeleri yutar, ancak tümör içinde genellikle besleyici, tümör-dostu bir duruma yeniden programlanırlar. Bu “M2-benzeri” makrofajlar inflamasyonu baskılar ve aksi halde kanseri hedef alacak T hücreleri ile doğal öldürücü (NK) hücrelerin etkinliğini engeller. Hastalardan ve tümör taşıyan farelerden alınan melanom örneklerini inceleyen araştırmacılar, TMEM175 düzeylerinin çevre normal dokuya göre tümörlerde daha yüksek olduğunu ve bu baskılayıcı makrofaj durumuyla yakından ilişkili olduğunu buldular. Bu gözlem onları şu soruyu sormaya yöneltti: TMEM175 yalnızca makrofaj gibi myeloid hücrelerde kapatılırsa ne olur?
Bir Lizozomal Kapı Bekçisini Kaldırmak Dengeyi Değiştirir
Araştırma grubu, TMEM175’in özellikle myeloid hücrelerde silindiği fareler geliştirdi ve ardından cilt altına melanom veya akciğer kanseri hücreleri yerleştirerek veya akciğerde metastazı tetiklemek için kan dolaşımına vererek modeller oluşturdu. Bu modellerin tamamında, TMEM175 eksik farelerde tümörler daha yavaş büyüdü ve daha az metastatik nodül oluştu. Ayrıntılı hücre analizi, tümör içindeki makrofajların güçlü bağışıklık aktivasyonu ile ilişkili “M1-benzeri” profile kaydığını, aynı zamanda baskılayıcı M2-benzeri popülasyonun azaldığını gösterdi. Aynı zamanda, tümör dokusunda çok daha fazla CD4 ve CD8 T hücresi ile NK hücresi birikti ve bunlar moleküler olarak aktifleşmiş ve öldürmeye hazır olduklarına dair işaretler gösterdi.
Hücre Artıkları Nasıl Ateşli Bir Bağışıklık Sinyali Tetikler?
İç mekanizmayı açığa çıkarmak için araştırmacılar kültürde kemik iliği kaynaklı makrofajları inceledi. Bu hücreler ölü tümör hücre parçalarını yuttuğunda lizozomları destabilize oldu, kathepsin B gibi enzimler sızıntı yaptı ve çevre sıvıdaki kalsiyum düzeyleri değişti. TMEM175 eksik makrofajlarda bu bozulma daha güçlüydü ve NLRP3 inflammasom adı verilen moleküler alarm sisteminin güçlü bir şekilde aktivasyonuna yol açtı. Bir kez aktif hale geldiğinde, bu çok proteinli kompleks IL‑1β ve IL‑18 gibi güçlü haberci moleküllerin salınmasını tetikliyor. Kaspaz‑1 enzimini bloke etmek veya IL‑1β ya da IL‑18’i antikorlarla nötralize etmek, farelerde TMEM175 kaybının anti‑tümör faydasını büyük ölçüde ortadan kaldırdı; bu da bu inflamatuvar kaskadın etkinin merkezinde olduğunu gösteriyor.
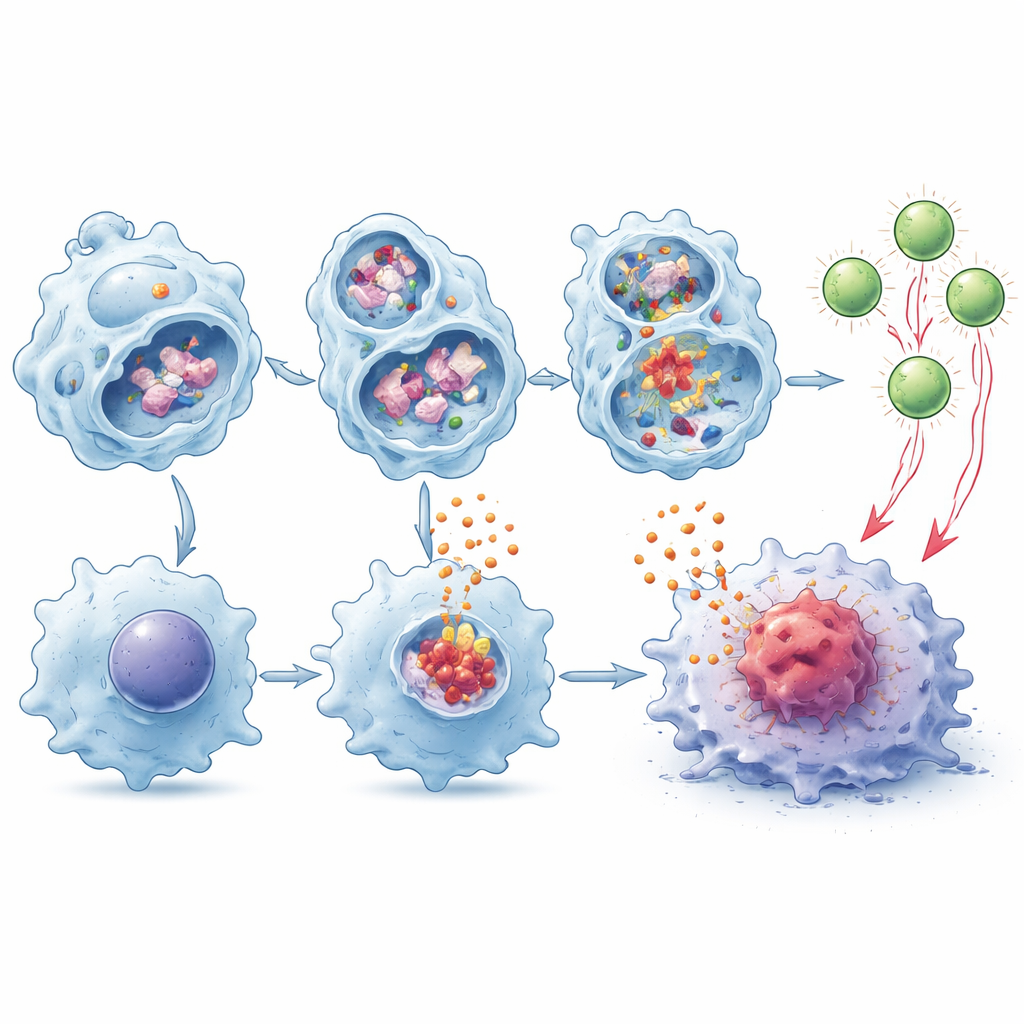
T Hücrelerinin Tümörleri Görüp Saldırmasına Yardım Etmek
Makrofajlar sadece alarm sinyalleri salgılamaz—aynı zamanda tümör proteinlerini parçalayıp parçacıkları yüzeylerinde sergileyerek T hücrelerini uyaran çapraz‑sunum sürecini de yürütürler. Yazarlar, TMEM175 eksik makrofajların lizozom içinde tümör materyalini daha yavaş parçaladığını ve böylece sunum için daha fazla sağlam parça kaldığını buldular. Ortak kültür deneylerinde, bu hücreler tümör‑spesifik CD8 T hücrelerinin genişlemesini ve aktivasyonunu çok daha iyi tetikledi ve bu etki IL‑1β ve IL‑18 varlığında daha da güçlendi. Bu şekilde eğitilmiş T hücreleri, kendi CD8 hücreleri olmayan tümör taşıyan farelere aktarıldığında, normal makrofajlar tarafından eğitilen T hücrelere kıyasla tümör büyümesini daha etkili biçimde yavaşlattı.
Kontrol Noktası Terapisinin Gücünü Artırmak
TMEM175 eksik tümörlerde aktif T hücreleri zengin olduğundan, araştırmacılar bu ortamın yaygın kullanılan bir kontrol noktası inhibitörü olan anti‑PD‑1’e farklı yanıt verip vermeyeceğini test ettiler. Standart farelerde anti‑PD‑1 melanom büyümesini neredeyse etkilemedi; bu, klinikte sık görülen direnci yansıtıyor. Buna karşılık, makrofajlarda TMEM175 olmayan farelerde aynı ilaç verildiğinde tümörler belirgin şekilde daha küçük oldu ve daha fazla tümör hücresi ölümü görüldü. Bu hayvanların tümörlerinde daha fazla aktif makrofaj, T hücresi ve NK hücresi vardı; bu da TMEM175 aracılığıyla tümör ortamının yeniden şekillendirilmesinin mevcut immünoterapinin etkinliğini artırdığını gösteriyor.
Tümör Mikroçevresine Yeni Bir Müdahale Noktası
Genel olarak çalışma, TMEM175’i makrofajların ölen tümör hücrelerine nasıl yanıt vereceğini kontrol eden moleküler bir anahtar olarak ortaya koyuyor. Bu lizozomal iyon kanalı yok olduğunda, tümör kalıntıları lizozomları daha kolay destabilize ediyor, kalsiyum seviyeleri yükseliyor ve inflammasom ateşlenerek IL‑1β ve IL‑18’in salınmasını serbest bırakıyor. Aynı zamanda tümör proteinlerinin daha yavaş parçalanması, bunların CD8 T hücrelerine sunumunu iyileştiriyor. Bu değişiklikler birlikte makrofajları tümörün suç ortaklarından güçlü müttefiklere dönüştürüyor; T hücreleri ve NK hücrelerini kanserle savaşmaya çağırıyor ve tümörleri anti‑PD‑1 tedavisine duyarlı hale getiriyor. Seçici olarak TMEM175’i bloke eden ve tümör ilişkili makrofajlara ulaşabilen ilaçların geliştirilmesi hâlâ gerekse de, bu çalışma kombinasyon kanser immünoterapisi için umut verici yeni bir yol işaret ediyor.
Atıf: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Anahtar kelimeler: tümör mikroçevresi, makrofajlar, inflammasom, kanser immünoterapisi, antijen çapraz-sunumu