Clear Sky Science · nl
Gebrek aan lysosomaal TMEM175 in myeloïde macrofagen wekt antitumorimmuniteit op via inflammasoom- en kruispresentatie-route
De schoonmaakploeg van het lichaam omzetten in kankebestrijders
Behandeling van kanker steunt steeds vaker op het wakker maken van het immuunsysteem, maar veel tumoren weten toch aan onze afweer te ontsnappen. Deze studie onderzoekt een onverwachte rem in immuuncellen — een ionkanaal genaamd TMEM175 dat zich bevindt op kleine recyclende compartimenten, de lysosomen. Door TMEM175 specifiek uit macrofagen te verwijderen, de cellulaire schoonmaakploeg van het lichaam, tonen de auteurs in muizen aan dat tumoren krimpen, minder uitzaaien en beter reageren op bestaande immunotherapie. Het werk suggereert een nieuwe manier om de tumormicro-omgeving te herbedraden zodat het immuunsysteem kankercellen effectiever kan herkennen en vernietigen.
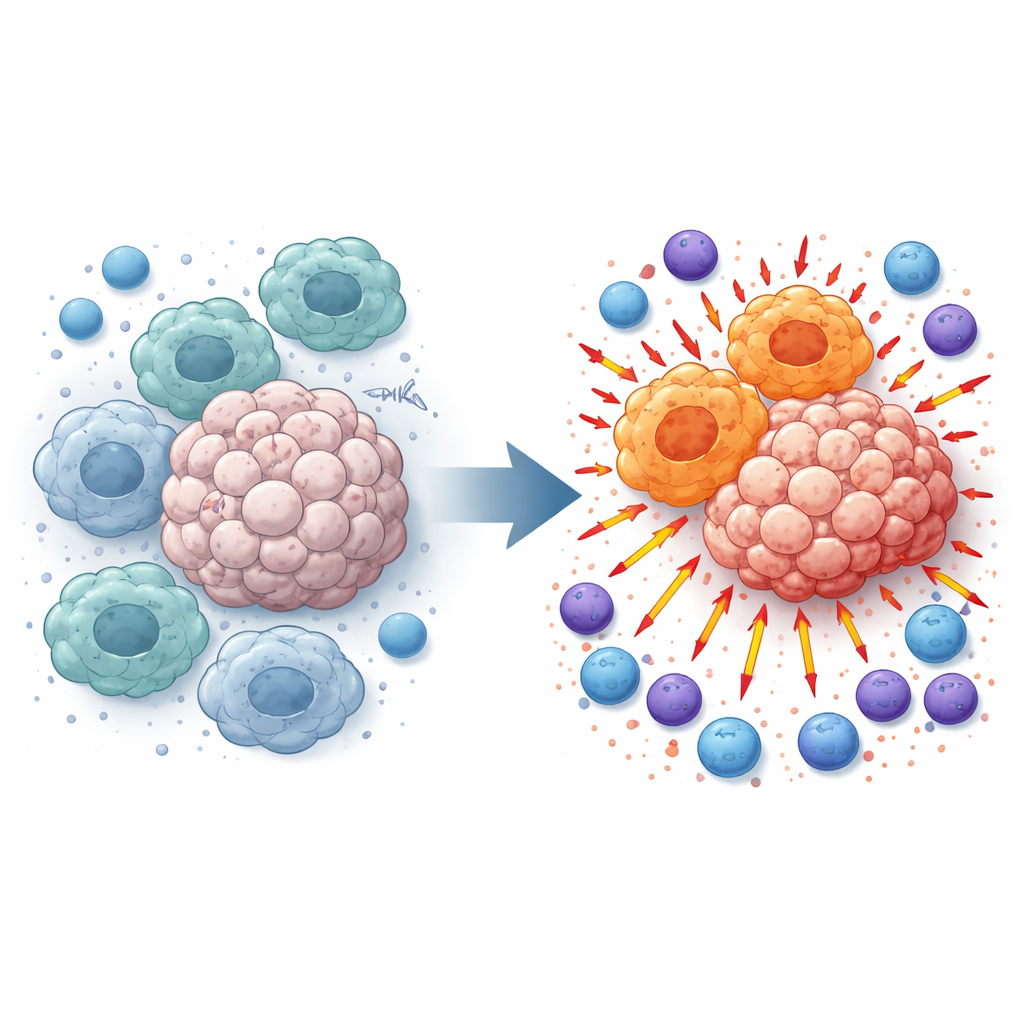
Waarom bepaalde immuuncellen tumorgroei kunnen bevorderen
Macrofagen patrouilleren door weefsels en ruimen afval op, maar binnen tumoren worden ze vaak omgeprogrammeerd naar een verzorgende, tumorrelevante staat. Deze “M2‑achtige” macrofagen dempen ontsteking en belemmeren T‑cellen en natural killer (NK)‑cellen die anders kanker zouden aanvallen. Bij onderzoek van melanoommonsters van patiënten en tumoren bij muizen vonden de onderzoekers dat TMEM175-niveaus hoger waren in tumoren dan in nabijgelegen normaal weefsel en sterk gekoppeld waren aan deze onderdrukkende macrofaagtoestand. Die observatie riep de vraag op: wat gebeurt er als TMEM175 alleen in myeloïde cellen zoals macrofagen wordt uitgeschakeld?
Het verwijderen van een lysosomaal poortwachter kantelt het evenwicht
Het team maakte muizen waarbij TMEM175 specifiek in myeloïde cellen werd verwijderd en plaatste vervolgens melanoom- of longkankercellen onder de huid of in de bloedbaan om longmetastasen uit te lokken. In al deze modellen groeiden tumoren bij TMEM175‑deficiënte muizen langzamer en vormden ze minder metastatische knobbeltjes. Gedetailleerde celanalyses toonden dat macrofagen binnen deze tumoren verschoven naar een “M1‑achtige” profiel dat geassocieerd is met sterke immuunactivatie, terwijl de onderdrukkende M2‑achtige populatie afnam. Tegelijkertijd stapelden veel meer CD4‑ en CD8‑T‑cellen en NK‑cellen zich op in het tumorgebied en vertoonden moleculaire tekenen van activering en paraatheid om te doden.
Hoe celdébris een vurig immuunsignaal ontsteekt
Om de interne mechanismen te ontrafelen bestudeerden de onderzoekers in kweek met beenmergafgeleide macrofagen. Wanneer deze cellen fragmente van dode tumorcellen opnamen, raakten hun lysosomen destabiliseerd, lekten enzymen zoals cathepsine B en veranderden de calciumconcentraties in de omgevende vloeistof. Bij TMEM175‑deficiënte macrofagen was deze verstoring sterker, wat leidde tot robuuste activatie van een moleculair alarmsysteem, het NLRP3‑inflammasoom. Eenmaal actief zet dit meereiwitcomplex de vrijgave in gang van krachtige boodschappers, waaronder de cytokinen IL‑1β en IL‑18. Het blokkeren van het enzym caspase‑1, of het neutraliseren van IL‑1β of IL‑18 met antilichamen, maakte het antitumoreffect van het ontbreken van TMEM175 bij muizen grotendeels ongedaan, wat aantoont dat deze ontstekingscascade centraal staat in het effect.
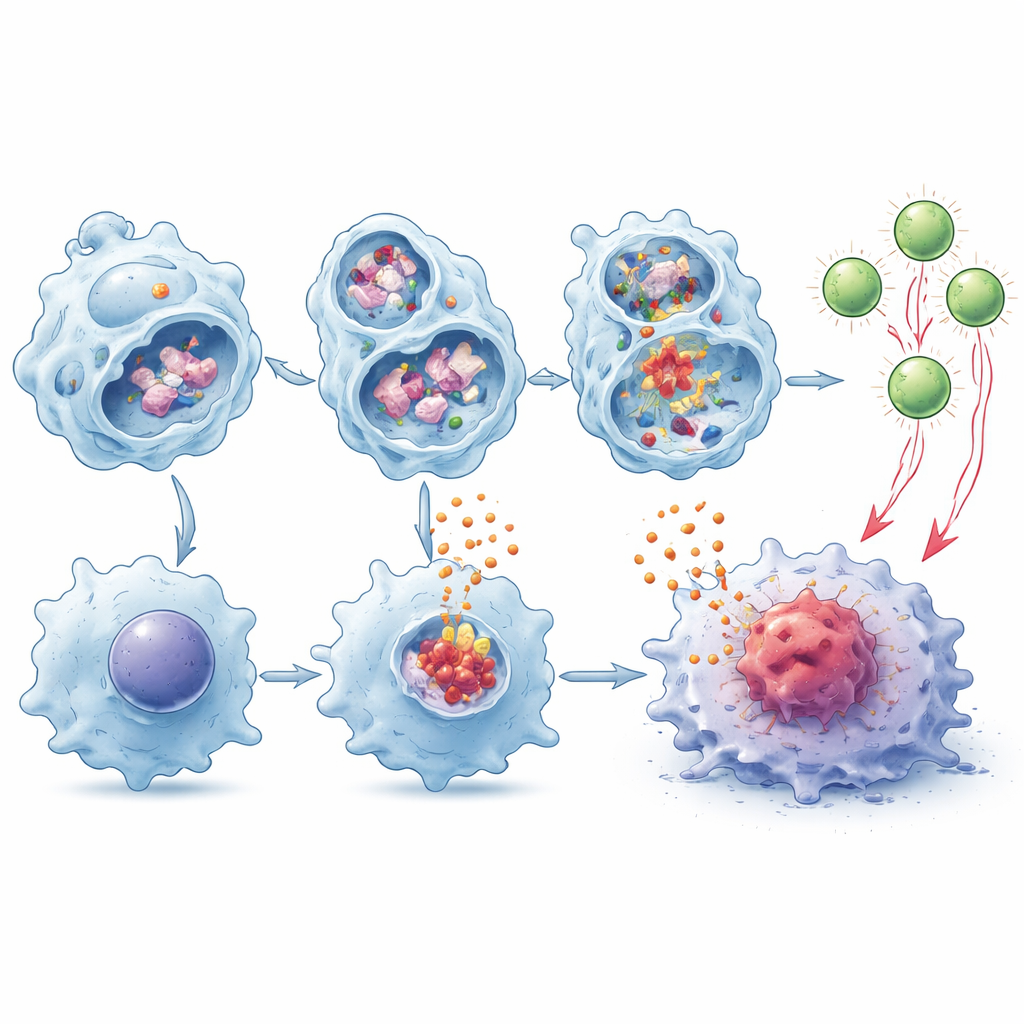
Helpen dat T‑cellen tumoren zien en aanvallen
Macrofagen doen meer dan alarmmoleculen uitscheiden — ze kunnen ook tumorantigenen afbreken en fragmenten op hun oppervlak presenteren om T‑cellen te waarschuwen, een proces dat kruispresentatie wordt genoemd. De auteurs vonden dat TMEM175‑deficiënte macrofagen tumormateriaal langzamer afbraakten in lysosomen, waardoor meer intacte stukken beschikbaar bleven voor presentatie. In co‑kweekexperimenten waren deze cellen veel beter in het stimuleren van expansie en activatie van tumorspecifieke CD8‑T‑cellen, en dit effect werd nog sterker in aanwezigheid van IL‑1β en IL‑18. Wanneer dergelijke geprimede T‑cellen werden overgedragen naar tumor‑dragende muizen die hun eigen CD8‑cellen misten, vertraagden ze de tumorgroei effectiever dan T‑cellen opgevoed door normale macrofagen.
De kracht van checkpointtherapie versterken
Aangezien TMEM175‑deficiënte tumoren rijk waren aan actieve T‑cellen, testten de onderzoekers of deze situatie anders zou reageren op anti‑PD‑1, een veelgebruikte checkpointremmer. Bij gewone muizen had anti‑PD‑1 nauwelijks effect op melanoomgroei, overeenkomend met de resistentie die vaak in de kliniek wordt gezien. In contrast daarmee hadden muizen zonder TMEM175 in macrofagen duidelijk kleinere tumoren en meer celdood na dezelfde behandeling. Hun tumoren bevatten meer geactiveerde macrofagen, T‑cellen en NK‑cellen, wat aangeeft dat het herinrichten van de tumoromgeving via TMEM175 bestaande immunotherapie effectiever maakt.
Een nieuw handvat voor de tumormicro-omgeving
Samengevat onthult de studie TMEM175 als een moleculaire schakelaar die bepaalt hoe macrofagen reageren op stervende tumorcellen. Als dit lysosomale ionkanaal afwezig is, destabiliseert tumordébris lysosomen gemakkelijker, stijgt het calciumgehalte en vuurt het inflammasoom af, met de vrijgave van IL‑1β en IL‑18 tot gevolg. Tegelijkertijd verbetert de vertraagde afbraak van tumorproteïnen hun presentatie aan CD8‑T‑cellen. Gezamenlijk transformeren deze veranderingen macrofagen van tumormedeplichtigen tot krachtige bondgenoten die T‑cellen en NK‑cellen mobiliseren tegen kanker en tumoren gevoeliger maken voor anti‑PD‑1‑therapie. Hoewel medicijnen die TMEM175 selectief blokkeren en tumorgeassocieerde macrofagen bereiken nog ontwikkeld moeten worden, wijst het werk op een veelbelovende nieuwe route voor combinatoire kankerimmunotherapie.
Bronvermelding: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Trefwoorden: tumormicro-omgeving, macrofagen, inflammasoom, kankerimmunotherapie, antigeenkruispresentatie