Clear Sky Science · ar
نقص قناة الأيونات الليزوزومية TMEM175 في البلاعم النخاعية يحفز المناعة المضادة للأورام عبر المسار الالتهابي وعبر العرض المتبادل للمستضدات
تحويل طاقم التنظيف في الجسم إلى مقاتلين ضد السرطان
تعتمد علاجات السرطان بشكل متزايد على تنشيط الجهاز المناعي، ومع ذلك لا تزال العديد من الأورام تفلت من دفاعاتنا. تستكشف هذه الدراسة فرملة غير متوقعة داخل الخلايا المناعية—قناة أيونات تُدعى TMEM175 توجد على الحويصلات الصغيرة المعاد تدويرها المعروفة بالليزوزومات. من خلال إزالة TMEM175 بشكل محدد من البلاعم، طاقم تنظيف الخلايا في الجسم، يظهر الباحثون في الفئران أن الأورام تتقلص، وتنتشر أقل، وتستجيب بشكل أفضل للعلاج المناعي الحالي. وتشير العمل إلى طريقة جديدة لإعادة برمجة البيئة الدقيقة للورم بحيث يستطيع الجهاز المناعي تمييز الخلايا السرطانية وتدميرها بفعالية أكبر.
لماذا تساعد بعض الخلايا المناعية الأورام على النمو
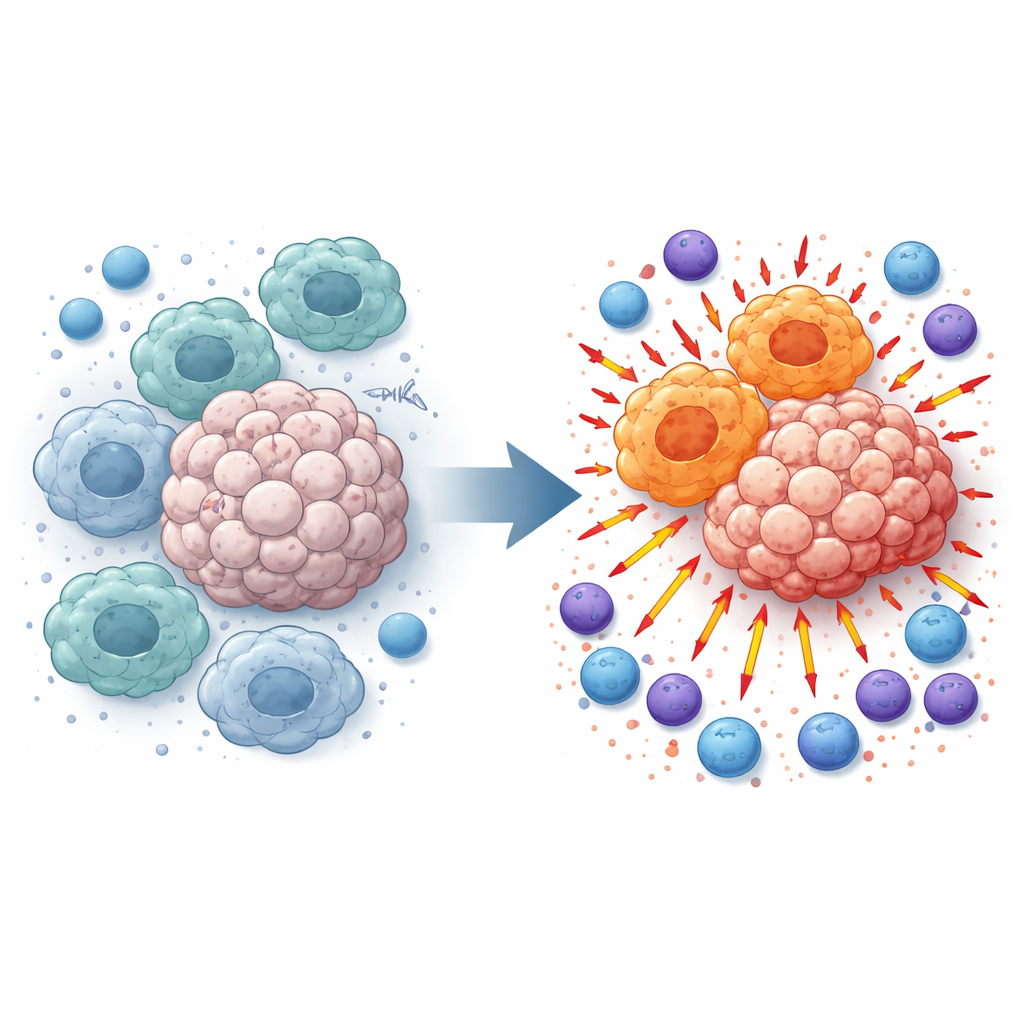
تقوم البلاعم بدور دوريات الأنسجة وابتلاع الحطام، لكن داخل الأورام كثيراً ما تُعاد برمجتها إلى حالة داعمة ومغذّية للورم. هذه البلاعم من الطراز «M2‑شبيه» تخفف الالتهاب وتعيق الخلايا التائية والخلايا القاتلة الطبيعية (NK) التي كانت ستهاجم السرطان. عند فحص عينات ميلانوما من مرضى وفئران حاملة للأورام، وجد الباحثون أن مستويات TMEM175 كانت أعلى في الأورام مقارنة بالنسيج الطبيعي المجاور وكانت مرتبطة ارتباطاً وثيقاً بهذه الحالة المثبطة للبلاعم. قادهم هذا الملاحظة لسؤال: ماذا يحدث إذا أُطفئت TMEM175 فقط في الخلايا النخاعية مثل البلاعم؟
إزالة بوّاب ليزوزومي تغير كفة التوازن
صمّم الفريق فئراناً محرّفة بحيث تُحذف TMEM175 بشكل محدد في الخلايا النخاعية ثم زرعوا خلايا ميلانوما أو سرطان الرئة تحت الجلد، أو في مجرى الدم لإحداث النقائل الرئوية. عبر هذه النماذج، نمت الأورام في الفئران التي تفتقر إلى TMEM175 بوتيرة أبطأ وكونت عُقيدات نقيلية أقل. أظهر التحليل الخلوي المفصّل أن البلاعم داخل هذه الأورام تحولت نحو ملف «M1‑شبيه» المرتبط بالتنشيط المناعي القوي، بينما انخفضت الفئة المثبطة الشبيهة بـM2. في الوقت نفسه، تراكم عدد أكبر بكثير من الخلايا التائية CD4 وCD8 والخلايا القاتلة الطبيعية داخل نسيج الورم وأظهرت دلائل جزيئية على أنها مفعّلة ومستعدة للقتل.
كيف يثير حطام الخلايا إشارة مناعية نارية
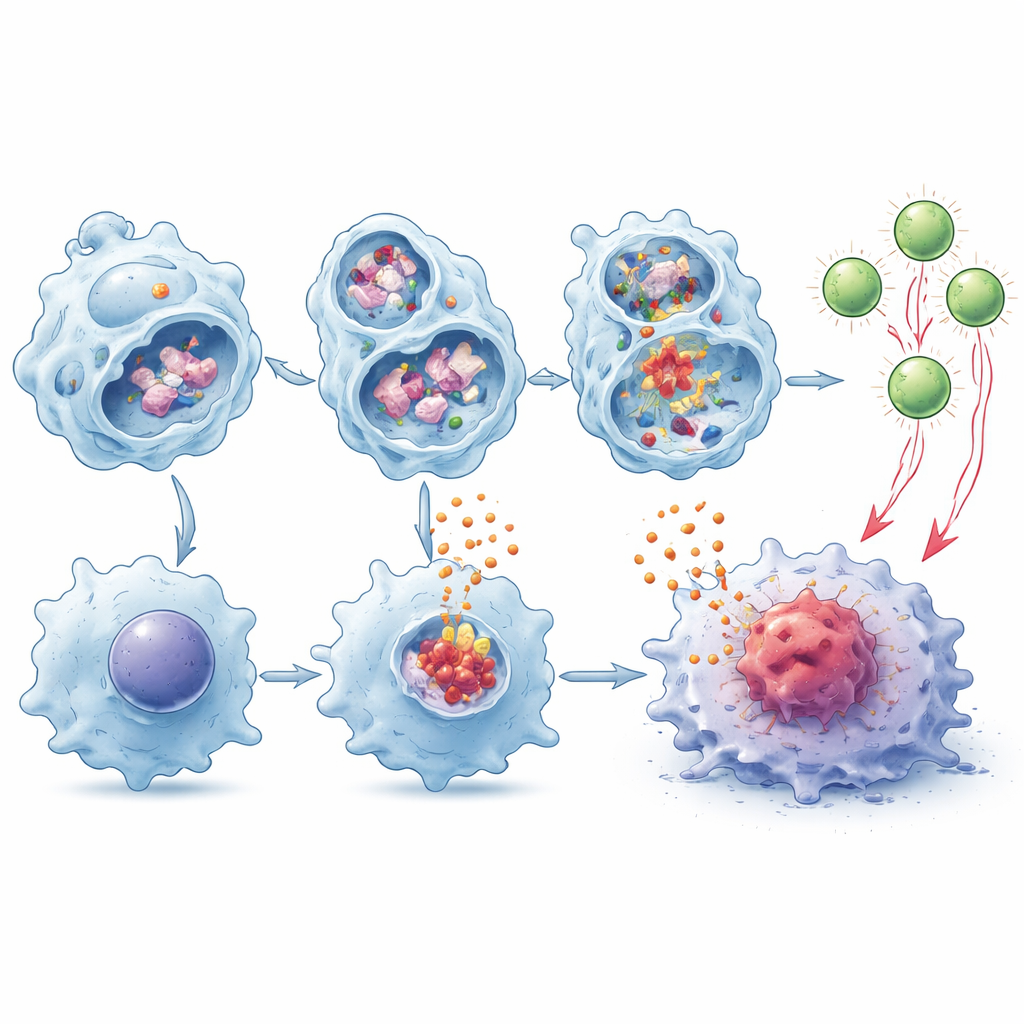
لكشف الآليات الداخلية، درس الباحثون بلاعم مشتقة من نخاع العظم في مزرعة خلوية. عندما ابتلعت هذه الخلايا شظايا من خلايا الورم الميتة، أصبحت الليزوزومات غير مستقرة، متسربةً إنزيمات مثل كاتيبسين B ومغيرة مستويات الكالسيوم في الوسط المحيط. في البلاعم التي تفتقر إلى TMEM175 كان هذا الاضطراب أقوى، مما أدى إلى تنشيط قوي لنظام إنذار جزيئي يسمى إنفلاماسوم NLRP3. وبمجرد نشاطه، يطلق هذا المركب متعدد البروتينات جزيئات مرسال قوية، بما في ذلك السيتوكينات IL‑1β وIL‑18. أدى حجب الإنزيم كاسبيز‑1، أو تحييد IL‑1β أو IL‑18 بأجسام مضادة، إلى محو الفائدة المضادة للأورام المترتبة على فقدان TMEM175 لدى الفئران إلى حد كبير، مما يبيّن أن هذا المسار الالتهابي مركزي للتأثير.
مساعدة الخلايا التائية على رؤية ومهاجمة الأورام
تفعل البلاعم أكثر من إطلاق إشارات الإنذار—فهي أيضاً تقطع بروتينات الورم وتعرض شظايا على سطحها لتنبيه الخلايا التائية، وهي عملية تُعرف بالعرض المتبادل للمستضدات. وجد المؤلفون أن البلاعم الخالية من TMEM175 تكسّر مادّة الورم ببطء أكبر داخل الليزوزومات، مما يترك قطعاً أكثر سليمة متاحة للعرض. في تجارب زرع مشترك أظهرت هذه الخلايا قدرة أفضل بكثير على دفع توسع وتنشيط الخلايا التائية CD8 المحددة للورم، وزاد هذا التأثير قوةً بوجود IL‑1β وIL‑18. وعندما نُقلت مثل هذه الخلايا التائية المُحضّرة إلى فئران حاملة للأورام وحيدة القنوات خالية من خلايا CD8 الخاصة بها، أبطأت نمو الورم بفعالية أكبر من الخلايا التائية المتعلمة على يد البلاعم الطبيعية.
تعزيز فعالية علاج نقاط التفتيش المناعية
لأن الأورام الخالية من TMEM175 كانت غنية بالخلايا التائية النشطة، اختبر الباحثون ما إذا كانت هذه البيئة ستستجيب بشكل مختلف لمضاد PD‑1، وهو مثبط نقاط تفتيش مستخدم على نطاق واسع. في الفئران العادية، أثّر مضاد PD‑1 بالكاد على نمو الميلانوما، مما يعكس المقاومة التي تُرى غالباً في العيادة. بالمقابل، أظهرت الفئران التي تفتقر إلى TMEM175 في البلاعم أوراماً أصغر بكثير ومعدلات موت خلوي ورمي أعلى عند إعطاء نفس الدواء. احتوت أورامها على بلاعم وخلايا تائية وخلايا NK أكثر تفعيلًا، مما يدل على أن إعادة تشكيل بيئة الورم عبر TMEM175 يجعل العلاج المناعي القائم يعمل بشكل أفضل.
مقبض جديد على البيئة الدقيقة للورم
بشكل عام تكشف الدراسة أن TMEM175 هو مفتاح جزيئي يتحكم في كيفية استجابة البلاعم لخلايا الورم الميتة. عندما تغيب هذه القناة الأيونية الليزوزومية، يصبح حطام الورم أكثر قدرة على زعزعة استقرار الليزوزومات، ترتفع مستويات الكالسيوم، وينطلق الإنفلاماسوم مطلقًا IL‑1β وIL‑18. في الوقت نفسه، يؤدي تباطؤ تَحلّل بروتينات الورم إلى تحسين عرضها على خلايا CD8 التائية. معاً، تحول هذه التغيرات البلاعم من متواطئة مع الورم إلى حلفاء أقوياء يجمعون الخلايا التائية وNK لمهاجمة السرطان ويجعلون الأورام أكثر حساسية لمضاد PD‑1. وبينما لا تزال هناك حاجة لتطوير أدوية تحجب TMEM175 بشكل انتقائي وتصل إلى البلاعم المرتبطة بالأورام، يشير العمل إلى مسار واعد جديد للعلاج المناعي التكاملي للسرطان.
الاستشهاد: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
الكلمات المفتاحية: البيئة الدقيقة للورم, البلاعم, الجسم الالتهابي (إنفلاماسوم), المناعة المناعية للسرطان, العرض المتبادل للمستضدات