Clear Sky Science · pt
Deficiência da TMEM175 lisossomal em macrófagos mieloides exerce imunidade antitumoral via inflamasoma e via de apresentação cruzada
Transformando a Equipe de Limpeza do Corpo em Combatentes do Câncer
O tratamento do câncer depende cada vez mais de despertar o sistema imunológico, mas muitos tumores ainda escapam às nossas defesas. Este estudo explora um freio inesperado dentro das células imunes — um canal iônico chamado TMEM175 que fica em pequenos compartimentos de reciclagem conhecidos como lisossomos. Ao remover o TMEM175 especificamente de macrófagos, a equipe de limpeza celular do corpo, os autores mostram em camundongos que os tumores encolhem, espalham‑se menos e respondem melhor à imunoterapia existente. O trabalho sugere uma nova forma de reconfigurar o microambiente tumoral para que o sistema imune reconheça e destrua as células cancerosas com mais eficácia.
Por que Certas Células Imunes Podem Ajudar o Tumor a Crescer
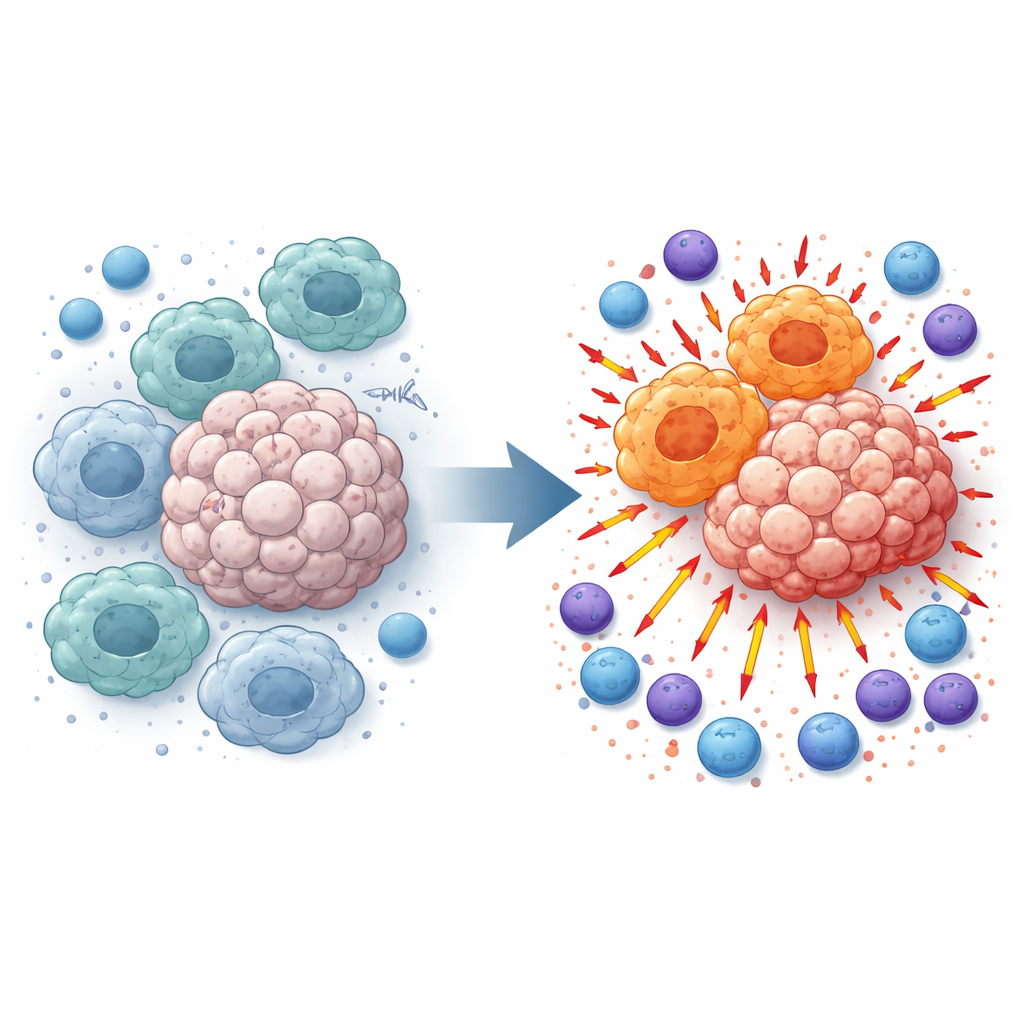
Os macrófagos patrulham os tecidos e engolem detritos, mas dentro dos tumores frequentemente são reprogramados para um estado que nutre e favorece o tumor. Esses macrófagos “semelhantes a M2” reduzem a inflamação e atrapalham células T e células NK que, de outra forma, atacariam o câncer. Ao examinar amostras de melanoma de pacientes e de camundongos com tumores, os pesquisadores encontraram níveis mais altos de TMEM175 nos tumores do que no tecido normal adjacente, e isso se relacionou de perto com esse estado supressor dos macrófagos. Essa observação levou à pergunta: o que acontece se o TMEM175 for desligado apenas em células mieloides, como os macrófagos?
Remover um Guardião Lisossomal Inclina a Balança
A equipe desenvolveu camundongos nos quais o TMEM175 é deletado especificamente em células mieloides e então implantou células de melanoma ou câncer de pulmão sob a pele, ou na corrente sanguínea para provocar metástases pulmonares. Em todos esses modelos, os tumores em camundongos deficientes em TMEM175 cresceram mais devagar e formaram menos nódulos metastáticos. Análises celulares detalhadas mostraram que os macrófagos dentro desses tumores mudaram para um perfil “semelhante a M1” associado à forte ativação imune, enquanto a população supressora semelhante a M2 diminuiu. Ao mesmo tempo, muito mais células T CD4 e CD8 e células NK acumularam‑se no tecido tumoral e apresentaram sinais moleculares de ativação e prontidão para matar.
Como Detritos Celulares Disparam um Sinal Imune Inflamatório
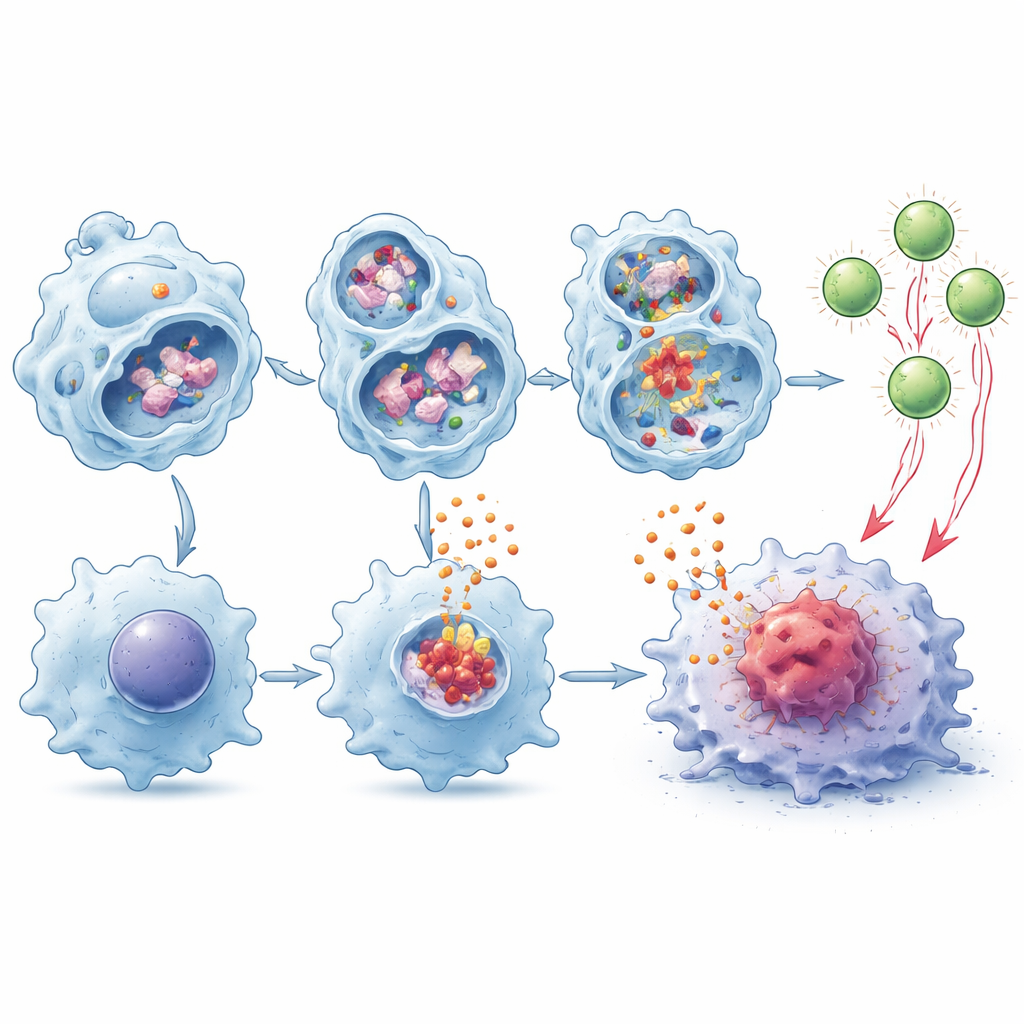
Para desvendar os mecanismos, os pesquisadores estudaram macrófagos derivados da medula óssea em cultura. Quando essas células engolfavam fragmentos de células tumorais mortas, seus lisossomos se tornavam desestabilizados, vazando enzimas como a catepsina B e alterando os níveis de cálcio no fluido ao redor. Em macrófagos deficientes em TMEM175 essa perturbação foi mais intensa, levando à ativação robusta de um sistema de alarme molecular chamado inflamasoma NLRP3. Uma vez ativo, esse complexo multiproteico desencadeia a liberação de mensageiros potentes, incluindo as citocinas IL‑1β e IL‑18. Bloquear a enzima caspase‑1, ou neutralizar IL‑1β ou IL‑18 com anticorpos, apagou em grande parte o benefício antitumoral da perda de TMEM175 em camundongos, mostrando que essa cascata inflamatória é central para o efeito.
Auxiliando as Células T a Ver e Atacar os Tumores
Os macrófagos fazem mais do que secretar sinais de alarme — eles também podem fragmentar proteínas tumorais e exibir pedaços na superfície para alertar as células T, um processo conhecido como apresentação cruzada. Os autores descobriram que macrófagos deficientes em TMEM175 degradavam o material tumoral mais lentamente dentro dos lisossomos, deixando mais fragmentos intactos disponíveis para apresentação. Em experimentos de co‑cadeia, essas células foram muito melhores em impulsionar a expansão e ativação de células T CD8 específicas do tumor, e esse efeito aumentou ainda mais na presença de IL‑1β e IL‑18. Quando tais células T ativadas foram transferidas para camundongos portadores de tumor que não tinham suas próprias células CD8, retardaram o crescimento tumoral de forma mais eficaz do que células T educadas por macrófagos normais.
Potencializando o Efeito da Terapia com Inibidor de Checkpoint
Como os tumores deficientes em TMEM175 estavam ricos em células T ativas, os pesquisadores testaram se esse contexto responderia de forma diferente ao anti‑PD‑1, um inibidor de checkpoint amplamente usado. Em camundongos padrão, o anti‑PD‑1 mal afetou o crescimento do melanoma, refletindo a resistência frequentemente vista na clínica. Em contraste, camundongos sem TMEM175 em macrófagos mostraram tumores marcadamente menores e mais morte de células tumorais quando receberam o mesmo medicamento. Seus tumores continham mais macrófagos ativados, células T e células NK, indicando que remodelar o ambiente tumoral via TMEM175 torna a imunoterapia estabelecida mais eficaz.
Uma Nova Alavanca sobre o Microambiente Tumoral
Em suma, o estudo revela TMEM175 como um interruptor molecular que controla como os macrófagos respondem às células tumorais em morte. Quando esse canal iônico lisossomal está ausente, os detritos tumorais desestabilizam os lisossomos com mais facilidade, os níveis de cálcio aumentam e o inflamasoma dispara, liberando IL‑1β e IL‑18. Ao mesmo tempo, a degradação mais lenta das proteínas tumorais melhora sua apresentação às células T CD8. Juntas, essas mudanças transformam macrófagos de cúmplices do tumor em aliados poderosos que mobilizam células T e NK contra o câncer e tornam os tumores mais sensíveis à terapia anti‑PD‑1. Embora ainda seja necessário desenvolver fármacos que bloqueiem seletivamente o TMEM175 e atinjam macrófagos associados a tumores, o trabalho aponta para uma nova e promissora avenida para a imunoterapia combinada contra o câncer.
Citação: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Palavras-chave: microambiente tumoral, macrófagos, inflamasoma, imunoterapia contra o câncer, apresentação cruzada de antígenos