Clear Sky Science · es
Deficiencia de TMEM175 lisosomal en macrófagos mieloides ejerce inmunidad antitumoral mediante la vía del inflamasoma y la presentación cruzada
Convertir al equipo de limpieza del cuerpo en luchadores contra el cáncer
El tratamiento del cáncer depende cada vez más de despertar al sistema inmunitario, pero muchos tumores siguen eludiendo nuestras defensas. Este estudio explora un freno inesperado dentro de las células inmunitarias: un canal iónico llamado TMEM175 que se localiza en pequeños compartimentos de reciclaje conocidos como lisosomas. Al eliminar TMEM175 específicamente en macrófagos, el equipo de limpieza celular del organismo, los autores muestran en ratones que los tumores se reducen, hacen menos metástasis y responden mejor a la inmunoterapia existente. El trabajo sugiere una nueva forma de reconfigurar el microambiente tumoral para que el sistema inmunitario reconozca y destruya las células cancerosas con mayor eficacia.
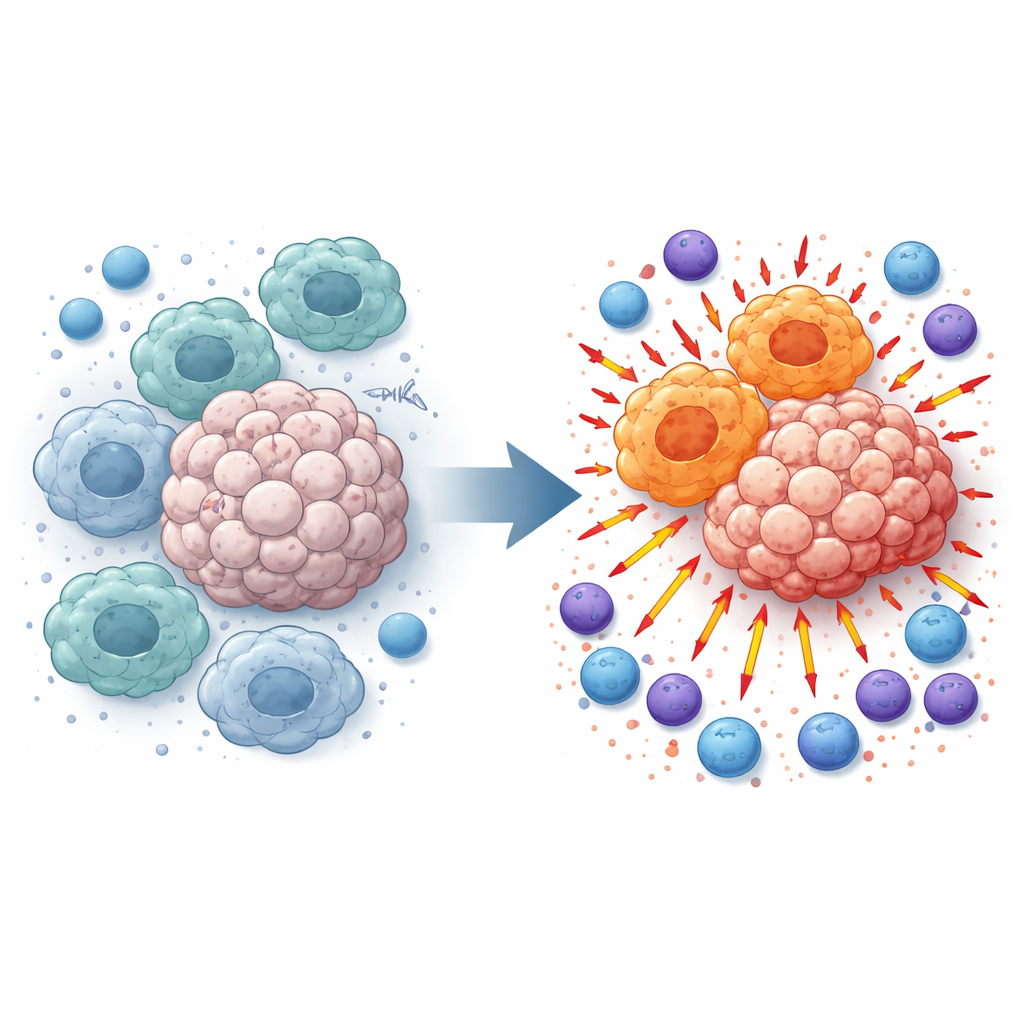
Por qué ciertos células inmunitarias pueden ayudar al crecimiento tumoral
Los macrófagos patrullan los tejidos y fagocitan desechos, pero dentro de los tumores con frecuencia se reprograman hacia un estado que los nutre y favorece al tumor. Estos macrófagos de tipo “M2” atenúan la inflamación y entorpecen a las células T y a las células NK que de otro modo atacarían el cáncer. Al examinar muestras de melanoma de pacientes y de ratones con tumores, los investigadores encontraron que los niveles de TMEM175 eran más altos en los tumores que en el tejido sano cercano y se asociaban estrechamente con este estado supresor de los macrófagos. Esa observación les planteó la pregunta: ¿qué ocurre si TMEM175 se apaga solo en las células mieloides, como los macrófagos?
Quitar a un portero lisosomal inclina la balanza
El equipo diseñó ratones en los que TMEM175 se elimina específicamente en células mieloides y luego implantó células de melanoma o de cáncer de pulmón bajo la piel, o las introdujo en el torrente sanguíneo para provocar metástasis pulmonares. En todos estos modelos, los tumores en ratones sin TMEM175 crecieron más despacio y formaron menos nódulos metastásicos. El análisis celular detallado mostró que los macrófagos dentro de esos tumores cambiaron hacia un perfil “M1”, asociado con fuerte activación inmune, mientras que la población supresora de tipo M2 disminuyó. Al mismo tiempo, muchos más linfocitos T CD4 y CD8 y células NK se acumularon en el tejido tumoral y mostraron signos moleculares de activación y disposición para matar.
Cómo los desechos celulares desencadenan una señal inmune intensa
Para desentrañar los mecanismos, los investigadores estudiaron macrófagos derivados de médula ósea en cultivo. Cuando estas células fagocitaban fragmentos de células tumorales muertas, sus lisosomas se desestabilizaban, filtrando enzimas como la catepsina B y alterando los niveles de calcio en el fluido circundante. En macrófagos deficientes en TMEM175 esta perturbación fue más intensa, lo que condujo a una activación robusta de un sistema de alarma molecular llamado inflamasoma NLRP3. Una vez activo, este complejo multiproteico provoca la liberación de mensajeros potentes, incluidas las citocinas IL‑1β e IL‑18. Bloquear la enzima caspasa‑1, o neutralizar IL‑1β o IL‑18 con anticuerpos, borró en gran medida el beneficio antitumoral de la pérdida de TMEM175 en ratones, demostrando que esta cascada inflamatoria es central para el efecto.
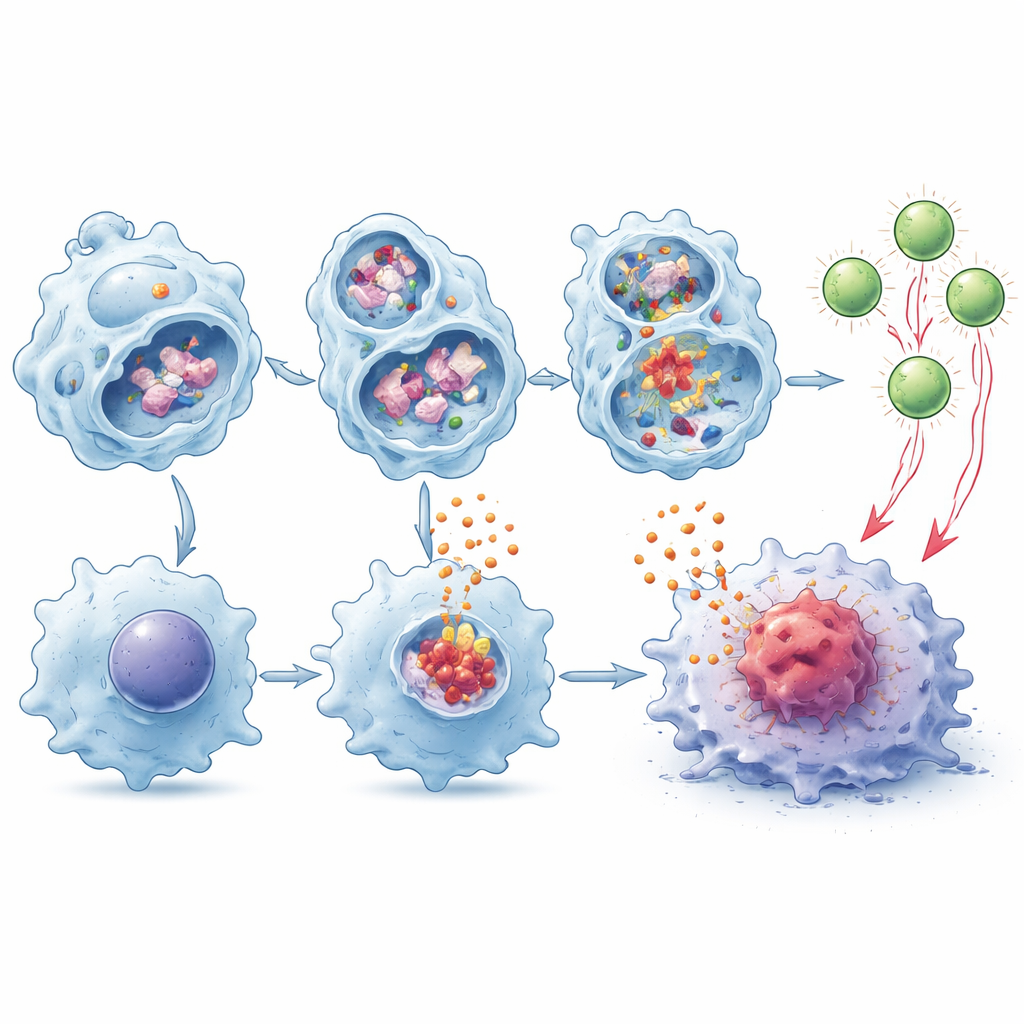
Ayudar a las células T a ver y atacar los tumores
Los macrófagos hacen más que secretar señales de alarma: también pueden degradar proteínas tumorales y mostrar fragmentos en su superficie para alertar a las células T, un proceso conocido como presentación cruzada. Los autores hallaron que los macrófagos deficientes en TMEM175 degradaban el material tumoral más lentamente dentro de los lisosomas, dejando más fragmentos intactos disponibles para su presentación. En experimentos de co‑cultivo, estas células fueron mucho mejores para impulsar la expansión y activación de linfocitos T CD8 específicos del tumor, y este efecto se intensificó en presencia de IL‑1β e IL‑18. Cuando dichos linfocitos T estimulados se transfirieron a ratones portadores de tumor que carecían de sus propias células CD8, frenaron el crecimiento tumoral con mayor eficacia que los linfocitos educados por macrófagos normales.
Potenciar el efecto de la terapia con inhibidores de puntos de control
Dado que los tumores sin TMEM175 estaban llenos de células T activas, los investigadores probaron si ese contexto respondería de forma distinta al anti‑PD‑1, un inhibidor de punto de control de uso generalizado. En ratones convencionales, el anti‑PD‑1 apenas afectó al crecimiento del melanoma, reflejando la resistencia que a menudo se observa en clínica. En contraste, los ratones que carecían de TMEM175 en los macrófagos mostraron tumores notablemente más pequeños y más muerte de células tumorales al recibir el mismo fármaco. Sus tumores contenían más macrófagos activados, más linfocitos T y más células NK activas, lo que indica que remodelar el microambiente tumoral a través de TMEM175 mejora la eficacia de inmunoterapias establecidas.
Una nueva palanca sobre el microambiente tumoral
En conjunto, el estudio revela a TMEM175 como un interruptor molecular que controla cómo responden los macrófagos a las células tumorales moribundas. Cuando este canal iónico lisosomal está ausente, los desechos tumorales desestabilizan más fácilmente los lisosomas, suben los niveles de calcio y se activa el inflamasoma, liberando IL‑1β e IL‑18. A la vez, la degradación más lenta de proteínas tumorales mejora su presentación a las células T CD8. Estos cambios convierten a los macrófagos de cómplices del tumor en aliados poderosos que movilizan a las células T y NK contra el cáncer y hacen que los tumores sean más sensibles a la terapia anti‑PD‑1. Aunque aún es necesario desarrollar fármacos que bloqueen selectivamente TMEM175 y alcancen a los macrófagos asociados a tumores, el trabajo apunta a una vía prometedora para la inmunoterapia combinada del cáncer.
Cita: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Palabras clave: microambiente tumoral, macrófagos, inflamasoma, inmunoterapia contra el cáncer, presentación cruzada de antígenos