Clear Sky Science · it
La carenza del TMEM175 lisosomiale nei macrofagi mieloidi esercita immunità antitumorale tramite l’inflammasoma e la via della cross‑presentazione
Trasformare la squadra di pulizia del corpo in combattenti contro il cancro
Il trattamento del cancro fa sempre più leva sul risveglio del sistema immunitario, eppure molti tumori riescono ancora a eludere le nostre difese. Questo studio esplora un freno inatteso all’interno delle cellule immunitarie: un canale ionico chiamato TMEM175 che si trova su piccoli compartimenti di riciclo noti come lisosomi. Rimuovendo TMEM175 specificamente nei macrofagi, la “squadra di pulizia” cellulare del corpo, gli autori mostrano nei topi che i tumori si riducono, si diffondono meno e rispondono meglio alle immunoterapie esistenti. Il lavoro suggerisce un nuovo modo di riconfigurare il microambiente tumorale affinché il sistema immunitario riconosca e distrugga più efficacemente le cellule tumorali.
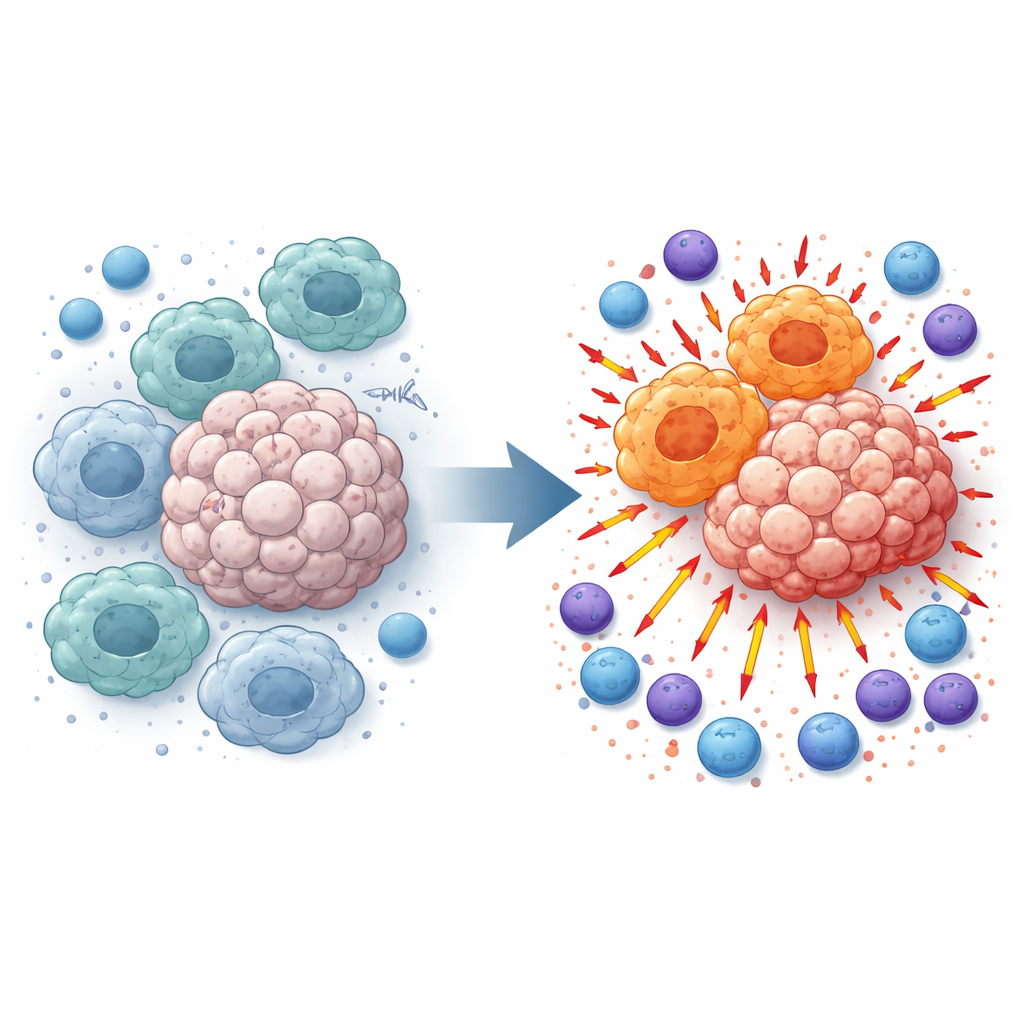
Perché certe cellule immunitarie possono favorire la crescita tumorale
I macrofagi pattugliano i tessuti e fagocitano detriti, ma all’interno dei tumori vengono spesso riprogrammati in uno stato nutritivo che favorisce la crescita tumorale. Questi macrofagi di tipo “M2‑like” attenuano l’infiammazione e ostacolano le cellule T e le cellule natural killer (NK) che altrimenti attaccherebbero il cancro. Analizzando campioni di melanoma di pazienti e topi portatori di tumore, i ricercatori hanno riscontrato che i livelli di TMEM175 erano più alti nei tumori rispetto ai tessuti normali circostanti e correlavano strettamente con questo stato soppressivo dei macrofagi. Questa osservazione li ha spinti a chiedersi: cosa succede se TMEM175 viene spento solo nelle cellule mieloidi come i macrofagi?
Rimuovere un guardiano lisosomiale inclina l’equilibrio
Il gruppo ha ingegnerizzato topi in cui TMEM175 è eliminato specificamente nelle cellule mieloidi e poi ha impiantato cellule di melanoma o di tumore polmonare sotto la pelle, o le ha iniettate nel circolo per indurre metastasi polmonari. In tutti questi modelli, i tumori nei topi privi di TMEM175 crescevano più lentamente e formavano meno noduli metastatici. Analisi cellulari dettagliate hanno mostrato che i macrofagi all’interno di questi tumori si sono spostati verso un profilo “M1‑like” associato a forte attivazione immunitaria, mentre la popolazione soppressiva M2‑like diminuiva. Allo stesso tempo, molte più cellule T CD4 e CD8 e cellule NK si accumulavano nel tessuto tumorale e presentavano segni molecolari di attivazione e prontezza a uccidere.
Come i detriti cellulari scatenano un segnale immunitario infiammatorio
Per svelare i meccanismi interni, i ricercatori hanno studiato macrofagi derivati dal midollo osseo in coltura. Quando queste cellule ingerivano frammenti di cellule tumorali morte, i loro lisosomi si destabilizzavano, rilasciando enzimi come la catepsina B e alterando i livelli di calcio nel fluido circostante. Nei macrofagi privi di TMEM175 questa perturbazione era più intensa, portando a una robusta attivazione di un sistema di allarme molecolare chiamato inflammasoma NLRP3. Una volta attivato, questo complesso multiproteico innesca il rilascio di potenti messaggeri, incluse le citochine IL‑1β e IL‑18. Il blocco della caspasi‑1, o la neutralizzazione di IL‑1β o IL‑18 con anticorpi, ha in gran parte annullato il beneficio antitumorale della perdita di TMEM175 nei topi, dimostrando che questa cascata infiammatoria è centrale per l’effetto.
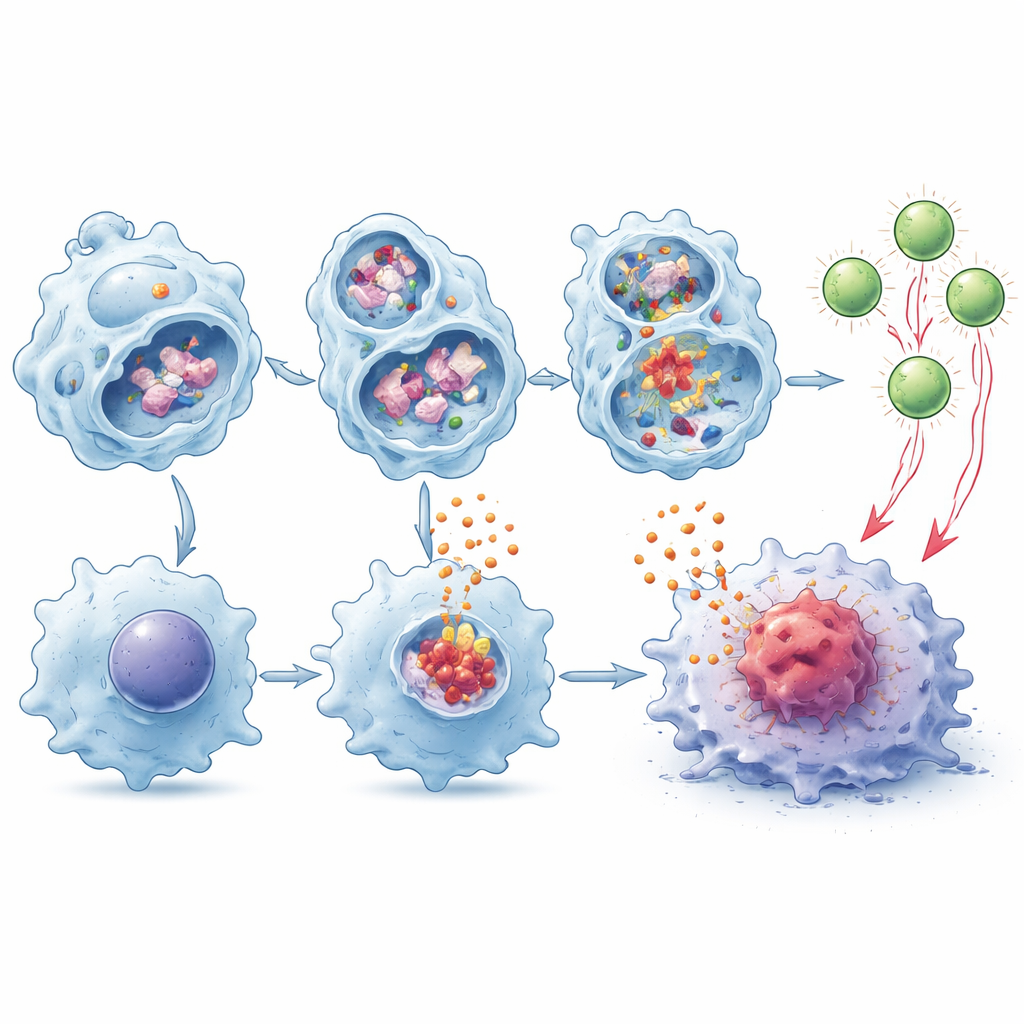
Aiutare le cellule T a vedere e attaccare i tumori
I macrofagi fanno più che secernere segnali di allarme: possono anche scomporre le proteine tumorali e esporre frammenti sulla loro superficie per avvisare le cellule T, un processo noto come cross‑presentazione. Gli autori hanno osservato che i macrofagi privi di TMEM175 degradavano il materiale tumorale più lentamente nei lisosomi, lasciando più pezzi integri disponibili per l’esposizione. In esperimenti di co‑coltura, queste cellule erano molto più efficaci nel promuovere l’espansione e l’attivazione di cellule T CD8 specifiche per il tumore, e questo effetto aumentava ulteriormente in presenza di IL‑1β e IL‑18. Quando tali cellule T primed sono state trasferite in topi portatori di tumore privi delle loro cellule CD8, hanno rallentato la crescita tumorale più efficacemente rispetto alle cellule T educate da macrofagi normali.
Potenziare l’efficacia della terapia con checkpoint
Poiché i tumori privi di TMEM175 risultavano ricchi di cellule T attivate, i ricercatori hanno testato se questo contesto rispondesse diversamente all’anti‑PD‑1, un inibitore di checkpoint ampiamente usato. Nei topi standard, l’anti‑PD‑1 ha avuto scarso effetto sulla crescita del melanoma, rispecchiando la resistenza spesso osservata in clinica. Al contrario, i topi privi di TMEM175 nei macrofagi hanno mostrato tumori marcatamente più piccoli e maggiore morte delle cellule tumorali quando trattati con lo stesso farmaco. I loro tumori contenevano più macrofagi attivati, cellule T e cellule NK, indicando che rimodellare l’ambiente tumorale tramite TMEM175 rende l’immunoterapia già esistente più efficace.
Una nuova leva sul microambiente tumorale
Nel complesso, lo studio rivela TMEM175 come un interruttore molecolare che controlla la risposta dei macrofagi alle cellule tumorali in morte. Quando questo canale ionico lisosomiale è assente, i detriti tumorali destabilizzano più facilmente i lisosomi, i livelli di calcio aumentano e l’inflammasoma si attiva, liberando IL‑1β e IL‑18. Allo stesso tempo, la degradazione rallentata delle proteine tumorali migliora la loro presentazione alle cellule T CD8. Questi cambiamenti trasformano i macrofagi da complici del tumore in potenti alleati che radunano cellule T e NK contro il cancro e rendono i tumori più sensibili all’anti‑PD‑1. Sebbene resti da sviluppare farmaci che blocchino selettivamente TMEM175 e raggiungano i macrofagi associati al tumore, il lavoro indica una promettente nuova strada per combinare l’immunoterapia del cancro.
Citazione: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Parole chiave: microambiente tumorale, macrofagi, inflammasoma, immunoterapia del cancro, cross‑presentazione degli antigeni