Clear Sky Science · he
חוסר בחלבון הטרנסממברנלי TMEM175 של הליזוזום במקרופאגים מיואידיים מפעיל חיסון אנטי‑גידולי דרך אינפלממסום ונתיב הצג־חוצה אנטיגן
להפוך את צוות הניקיון של הגוף ללוחמי סרטן
הטיפול בסרטן נשען יותר ויותר על עוררות המערכת החיסונית, אך גידולים רבים עדיין מצליחים להתחמק מגלאיה. מחקר זה בוחן מעצור בלתי צפוי בתאי החיסון — תעלת יונים בשם TMEM175 שנמצאת במכלי המיחזור הקטנים הנקראים ליזוזומים. על ידי הסרת TMEM175 באופן ספציפי ממקרופאגים, צוות הניקיון התאי של הגוף, מראים המחברים בעכברים שהגידולים מתכווצים, מתפשטים פחות ומגיבים טוב יותר לאימונו‑תרפיה קיימת. הממצא מציע דרך חדשה לכוונן את מיקרו‑סביבת הגידול כך שהמערכת החיסונית תוכל לזהות ולהשמיד תאים סרטניים ביעילות רבה יותר.
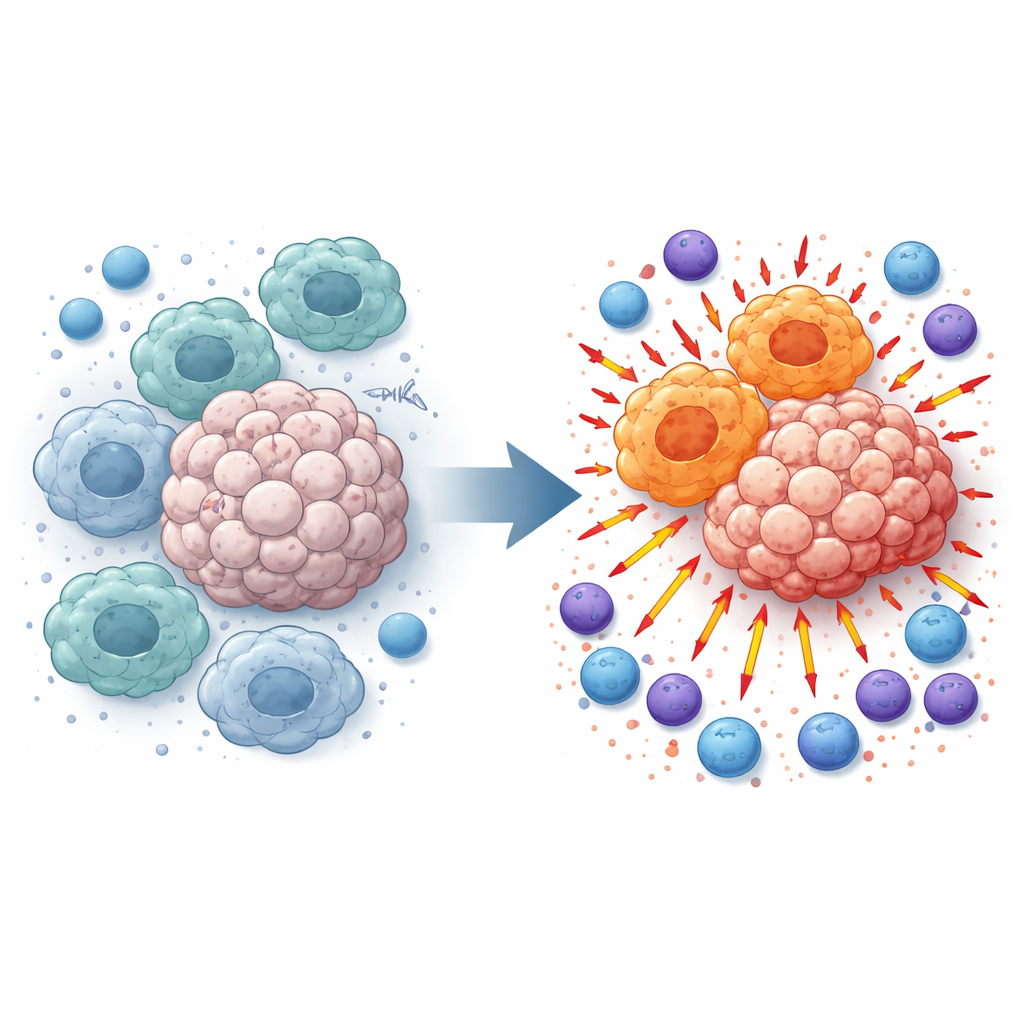
מדוע תאי חיסון מסוימים מסייעים לצמיחת גידולים
מקרופאגים סורקים רקמות ובליעים שברי רקמה, אך בתוך גידולים הם לעיתים מתכנתים למחוזקת תומכת גידול. מקרופאגים אלה הדומים ל‑M2 מרפים דלקת ומעכבים תאי T ותאי NK שבדרך כלל היו תוקפים את הסרטן. בבחינת דגימות מלנומה של חולים ועכברים נשאי גידול, החוקרים מצאו שרמות TMEM175 היו גבוהות יותר בגידולים מאשר ברקמה הקרובה התקינה והיו קשורות במידה רבה למצב המקרופאגים המדכא. תצפית זו הובילה אותם לשאלה: מה קורה אם מכבים את TMEM175 רק בתאים מיואידיים כגון מקרופאגים?
הסרת שומר השער הליזוזומלי מזיזה את המאזן
הצוות הנדס עכברים שבהם TMEM175 נמחק במיוחד בתאים מיואידיים ואז השתילו תאי מלנומה או סרטן ריאה מתחת לעור, או לזרם הדם כדי לעורר גרורות בריאות. במודלים אלה, בגידולים של עכברים חסרי TMEM175 הצמיחה הייתה איטית יותר ויצרו פחות נודולות גרורתיות. ניתוח תאי מפורט הראה שמקרופאגים בתוך אותם גידולים נטו לפרופיל דמוי‑M1 המשויך להפעלת חיסון חזקה, בעוד שאוכלוסיית ה‑M2 המדכאת פחתה. במקביל, הצטברו ברקמת הגידול הרבה יותר תאי CD4 ו‑CD8 ותאי NK והראו סימנים מולקולריים של הפעלה שמוכנים להרוג.
כיצד שברי תאים מציתים אות חיסוני לוהט
כדי לפענח את המנגנונים הפנימיים, החוקרים חקרו מקרופאגים שמקורם במח העצם בתרבית. כאשר תאים אלה בלעו חלקיקי תאים סרטניים מתים, הליזוזומים שלהם התערערו, דולפו אנזימים כגון קטפסין B ושיעור הסידן בנוזל הסמוך השתנה. במקרופאגים חסרי TMEM175 ההפרעה הזו הייתה חזקה יותר, והובילה להפעלה משמעותית של מערכת האזעקה המולקולרית הנקראת אינפלממסום NLRP3. לאחר הפעלה, קומפלקס חלבוני זה מפעיל שחרור מולקולות שליח חזקות, כולל הציטוקינים IL‑1β ו‑IL‑18. חסימת האנזים קספאז‑1, או נטרול IL‑1β או IL‑18 בעזרת נוגדנים, מעקרה במידה רבה את התועלת האנטי‑גידולית של חוסר TMEM175 בעכברים, מה שמראה כי קסקדת הדלקת הזו היא מרכזית להשפעה.
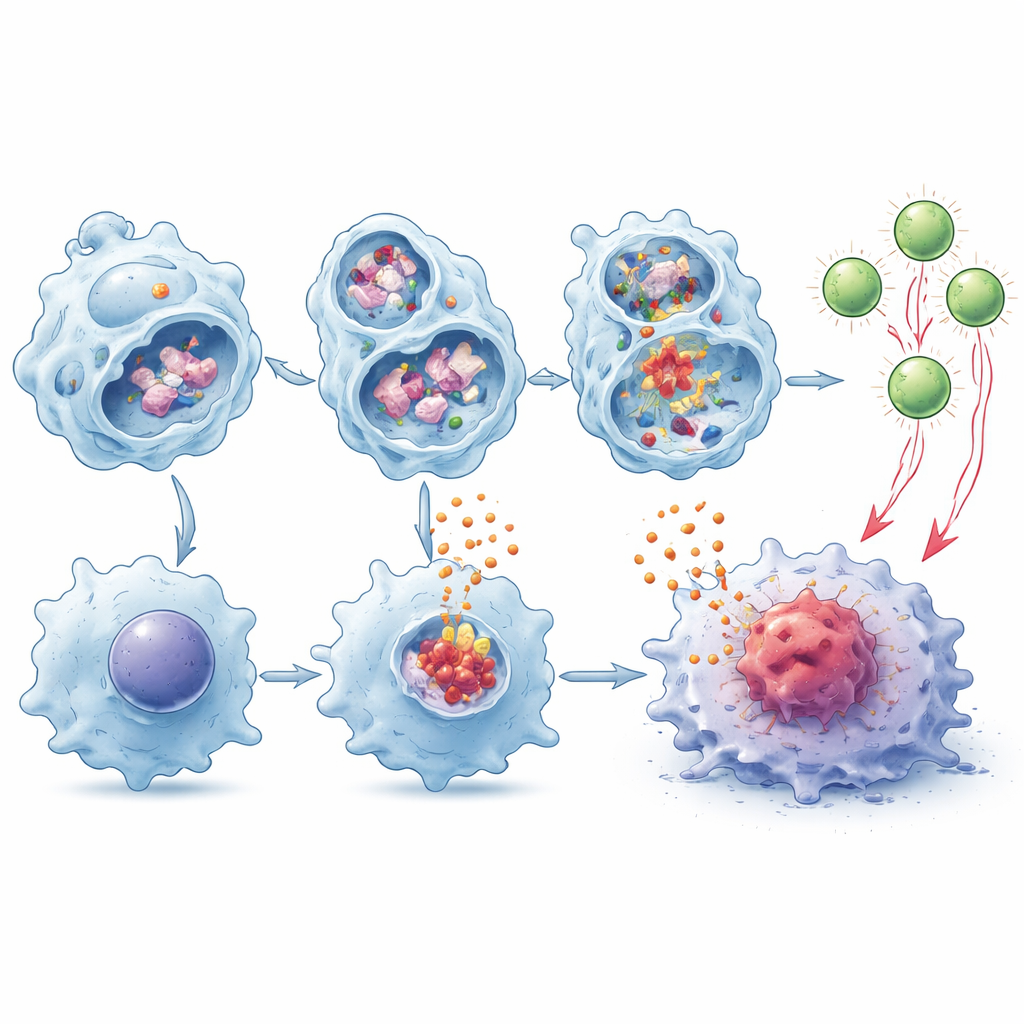
לעזור לתאי T לראות ולתקוף גידולים
מקרופאגים עושים יותר מאשר לשחרר אותות אזעקה — הם גם יכולים לפרק חלבוני גידול ולהציג חלקיקים על הממברנה כדי להתריע בפני תאי T, תהליך הידוע כהצגה חוצת‑תאים (cross‑presentation). המחברים מצאו שמקרופאגים חסרי TMEM175 פירקו את חומר הגידול לאט יותר בתוך הליזוזומים, והשאירו יותר חתיכות שלמות להצגה. בניסויי תרבית משותפת, תאים אלה היו טובים בהרבה בקידום ההתרחבות וההפעלה של תאי CD8 ספציפיים לגידול, והאפקט התגבר עוד יותר בנוכחות IL‑1β ו‑IL‑18. כאשר העבירו תאים T מחוסנים אלה לעכברים נשאי גידול החסרים את תאי ה‑CD8 שלהם, הם האטו את צמיחת הגידול ביעילות גבוהה יותר מתאי T שחונכו על ידי מקרופאגים רגילים.
הגברת העוצמה של תרפיית צמתים (checkpoint)
מכיוון שגידולים חסרי TMEM175 היו עשירים בתאי T פעילים, החוקרים בדקו האם סביבה זו תגיב אחרת ל‑anti‑PD‑1, מעכב צמתי שימושי נרחב. בעכברים סטנדרטיים, anti‑PD‑1 השפיע בקושי על צמיחת המלנומה, מה שמשקף עמידות שנראית לעתים בקליניקה. לעומת זאת, בעכברים החסרים TMEM175 במקרופאגים נצפו גידולים קטנים משמעותית ויותר מוות תאי גידול בעת מתן אותה התרופה. בגידולים שלהם היו יותר מקרופאגים, תאי T ותאי NK פעילים, מה שמעיד כי עיצוב מחודש של מיקרו‑הסביבה דרך TMEM175 משפר את יעילות האימונו‑תרפיה המתקיימת.
ידית חדשה על מיקרו‑סביבת הגידול
בסך הכל, המחקר חושף את TMEM175 כמתג מולקולרי ששולט באופן שבו מקרופאגים מגיבים לתאי גידול מתים. כאשר תעלת יונים ליזוזומלית זו חסרה, שברי הגידול מייצרים חוסר יציבות בליזוזומים ביתר קלות, רמות הסידן עולות והאינפלממסום נורה, משחרר IL‑1β ו‑IL‑18. במקביל, הפרעה בהידור של חלבוני הגידול משפרת את הצגתם לתאי CD8. יחד, השינויים הללו הופכים מקרופאגים משותפים לגידול לבעלי ברית רבי‑עוצמה שמגייסים תאי T ותאי NK נגד הסרטן ומרגישים את הגידולים לרגישות גבוהה יותר ל‑anti‑PD‑1. בעוד שעדיין יש לפתח תרופות שסלקטיבית יחסמו TMEM175 וישיגו את מקרופאגי הגידול, העבודה מצביעה על כיוון מבטיח לשילובי אימונו‑תרפיה בסרטן.
ציטוט: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
מילות מפתח: מיקרו‑סביבת הגידול, מקרופאגים, אינפלממסום, אימונו‑תרפיה בסרטן, הצגת אנטיגן חוצת‑תאים (cross‑presentation)