Clear Sky Science · ru
Дефицит лизосомального TMEM175 в миелоидных макрофагах вызывает противоопухолевый иммунитет через инфламмасому и путь кросс-презентации
Преобразование «службы уборки» организма в бойцов против рака
Лечение рака всё чаще опирается на активацию иммунной системы, но многие опухоли по‑прежнему ускользают от защиты организма. В этом исследовании изучается неожиданный «тормоз» внутри иммунных клеток — ионный канал TMEM175, расположенный на мелких перерабатывающих отделениях клетки, лизосомах. Удаляя TMEM175 выборочно в макрофагах, клеточной «службе уборки», авторы показывают на мышах, что опухоли уменьшаются, реже дают метастазы и лучше отвечают на существующую иммунотерапию. Работа указывает на новый способ перенастроить опухолевую микросреду, чтобы иммунная система эффективнее распознавала и уничтожала раковые клетки.
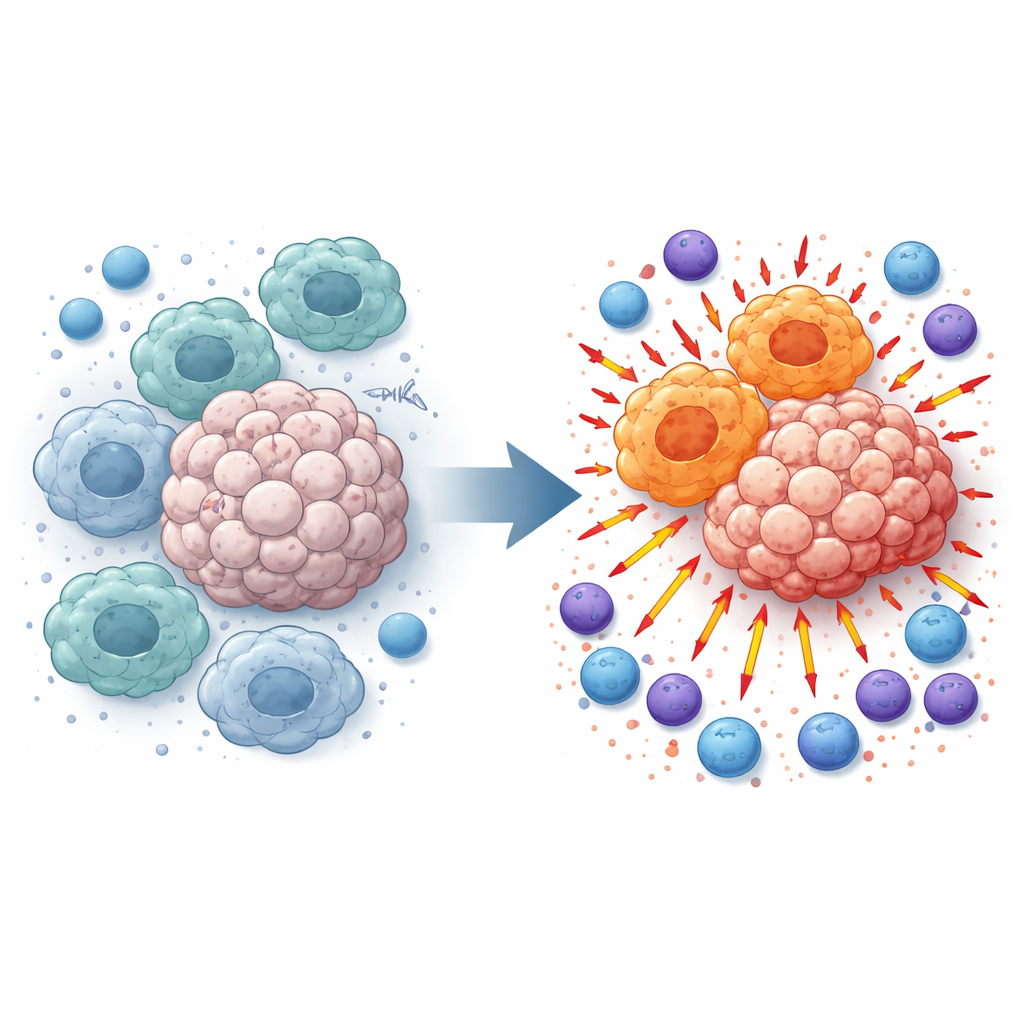
Почему одни иммунные клетки помогают опухолям расти
Макрофаги патрулируют ткани и поедают мусор, но в опухолях их часто перепрограммируют в питательное, дружественное опухоли состояние. Эти «M2‑подобные» макрофаги подавляют воспаление и мешают Т‑ и естественным киллерам (NK), которые в иных условиях атаковали бы рак. При обследовании образцов меланомы от пациентов и опухлевых моделей у мышей исследователи обнаружили, что уровни TMEM175 в опухолях выше, чем в прилежащих нормальных тканях, и тесно связаны с этим подавляющим фенотипом макрофагов. Это наблюдение навело их на вопрос: что произойдет, если выключить TMEM175 только в миелоидных клетках, таких как макрофаги?
Удаление лизосомального «привратника» меняет равновесие
Команда создала мышей, у которых TMEM175 удалён выборочно в миелоидных клетках, и затем имплантировала клетки меланомы или рака лёгкого подкожно или вводила их в кровоток, чтобы спровоцировать метастазы в лёгких. Во всех моделях опухоли у мышей с дефицитом TMEM175 росли медленнее и образовывали меньше метастатических узлов. Детальный анализ клеток показал, что макрофаги в этих опухолях смещались в сторону «M1‑подобного» профиля, связанного с сильной иммунной активацией, тогда как подавляющая M2‑подобная популяция уменьшилась. Одновременно в опухолевой ткани накапливалось намного больше CD4‑ и CD8‑Т‑клеток и NK‑клеток, которые показывали молекулярные признаки включения и готовности к цитотоксическому действию.
Как клеточный мусор зажигает воспалительный сигнал
Чтобы выяснить механизмы, исследователи изучали макрофаги, полученные из костного мозга, в культуре. Когда эти клетки поглощали фрагменты погибших опухолевых клеток, их лизосомы destabilизировались, из них просачивались ферменты, такие как катепсин B, и менялись уровни кальция в окружающей среде. В макрофагах с дефицитом TMEM175 это нарушение было сильнее, что приводило к мощной активации молекулярной сигнализации под названием NLRP3‑инфламмасома. После активации этот многобелковый комплекс вызывает выброс мощных медиаторов, включая цитокины IL‑1β и IL‑18. Блокирование каспазы‑1 или нейтрализация IL‑1β или IL‑18 антителами в значительной степени стирало противоопухолевое преимущество потери TMEM175 у мышей, что показывает центральную роль этой воспалительной каскады в эффекте.
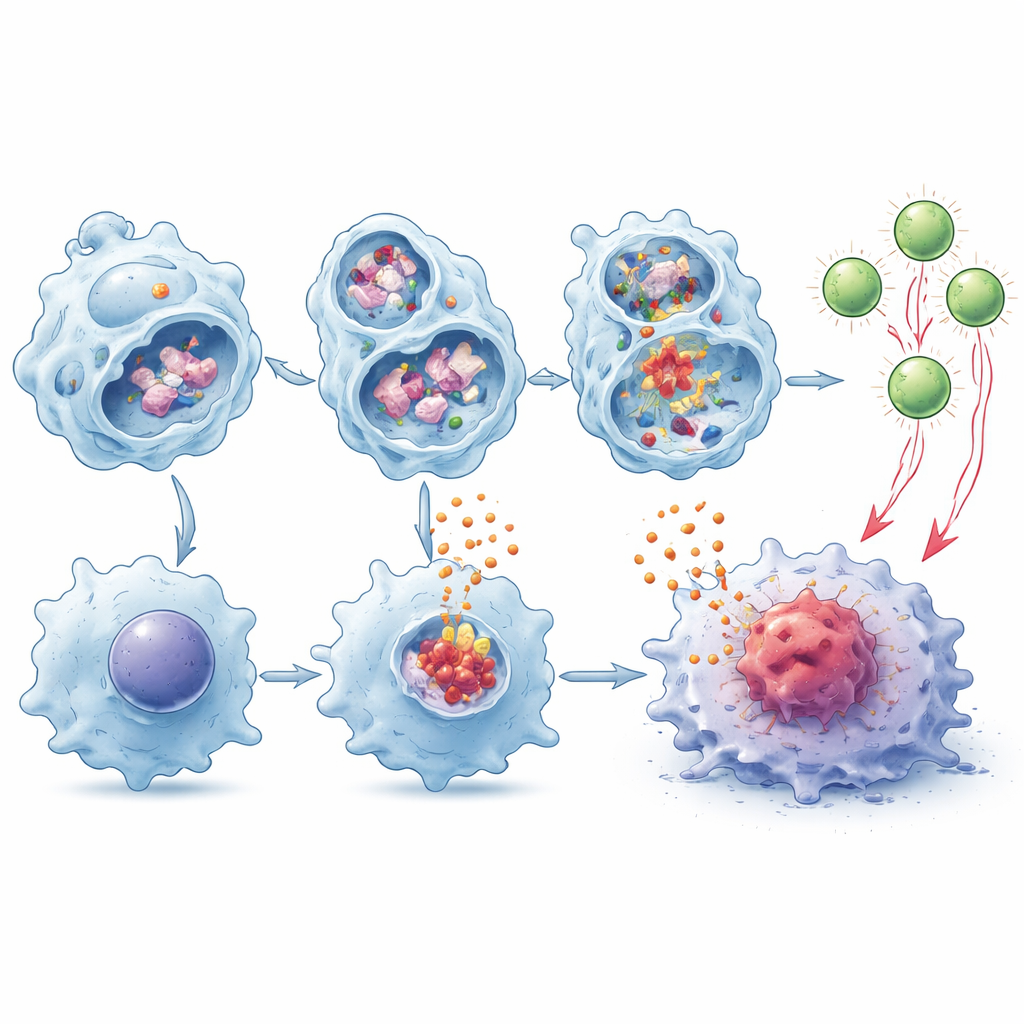
Помощь Т‑клеткам в распознавании и атаке опухолей
Макрофаги делают не только «сигналы тревоги» — они также расщепляют опухолевые белки и выставляют фрагменты на своей поверхности, чтобы привлечь Т‑клетки, процесс, известный как кросс‑презентация. Авторы обнаружили, что макрофаги с дефицитом TMEM175 медленнее разрушали опухолевый материал в лизосомах, оставляя больше целых фрагментов для презентации. В совместных культурах эти клетки гораздо эффективнее стимулировали расширение и активацию опухлеспецифичных CD8‑Т‑клеток, а эффект ещё сильнее усиливался в присутствии IL‑1β и IL‑18. Когда такие подготовленные Т‑клетки переносили в опухлестроящие мыши, лишённые собственных CD8‑клеток, они более эффективно замедляли рост опухолей по сравнению с Т‑клетками, обученными нормальными макрофагами.
Усиление эффективности терапии ингибиторами контрольных точек
Поскольку опухоли у животных с дефицитом TMEM175 были богаты активными Т‑клетками, исследователи проверили, как такая ситуация отреагирует на анти‑PD‑1, широко применяемый ингибитор контрольной точки. У стандартных мышей анти‑PD‑1 едва влиял на рост меланомы, что отражает резистентность, часто наблюдаемую в клинике. Напротив, у мышей с отсутствующим TMEM175 в макрофагах при введении того же препарата опухоли были значительно меньше и содержали больше погибших опухолевых клеток. В их опухолях обнаруживалось больше активированных макрофагов, Т‑ и NK‑клеток, что указывает на то, что перенастройка микросреды опухоли через TMEM175 делает существующую иммунотерапию более эффективной.
Новый рычаг воздействия на опухолевую микросреду
В целом исследование выявляет TMEM175 как молекулярный переключатель, контролирующий реакцию макрофагов на погибающие опухолевые клетки. При отсутствии этого лизосомального ионного канала опухолевый мусор легче дестабилизирует лизосомы, повышается уровень кальция, активируется инфламмасома и высвобождаются IL‑1β и IL‑18. Одновременно замедленное разрушение опухолевых белков улучшает их презентацию CD8‑Т‑клеткам. Вместе эти изменения превращают макрофагов из соучастников опухоли в мощных союзников, которые мобилизуют Т‑ и NK‑клетки против рака и повышают чувствительность опухолей к терапии анти‑PD‑1. Хотя ещё предстоит разработать препараты, селективно блокирующие TMEM175 и нацеленные на макрофаги, ассоциированные с опухолью, работа указывает на перспективное направление для комбинированной иммунотерапии рака.
Цитирование: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Ключевые слова: опухолевая микросреда, макрофаги, инфламмасома, иммунотерапия рака, кросс-презентация антигена