Clear Sky Science · sv
Brist på lysosomal TMEM175 i myeloida makrofager ger anti-tumörimmunitet via inflammasom- och korspresentationväg
Förvandla kroppens städpatrull till cancerbekämpare
Cancerbehandlingar förlitar sig i allt större utsträckning på att väcka immunsystemet, ändå lyckas många tumörer undkomma våra försvarsmekanismer. Denna studie undersöker en oväntad broms inne i immuncellerna—en jonkanal kallad TMEM175 som sitter på små återvinningskompartiment, lysosomer. Genom att ta bort TMEM175 specifikt från makrofager, kroppens cellulära städpatrull, visar författarna i möss att tumörer krymper, sprider sig mindre och svarar bättre på befintlig immunterapi. Arbetet tyder på ett nytt sätt att omskola tumörmikromiljön så att immunsystemet mer effektivt kan känna igen och förgöra cancerceller.
Varför vissa immunceller kan hjälpa tumörer att växa
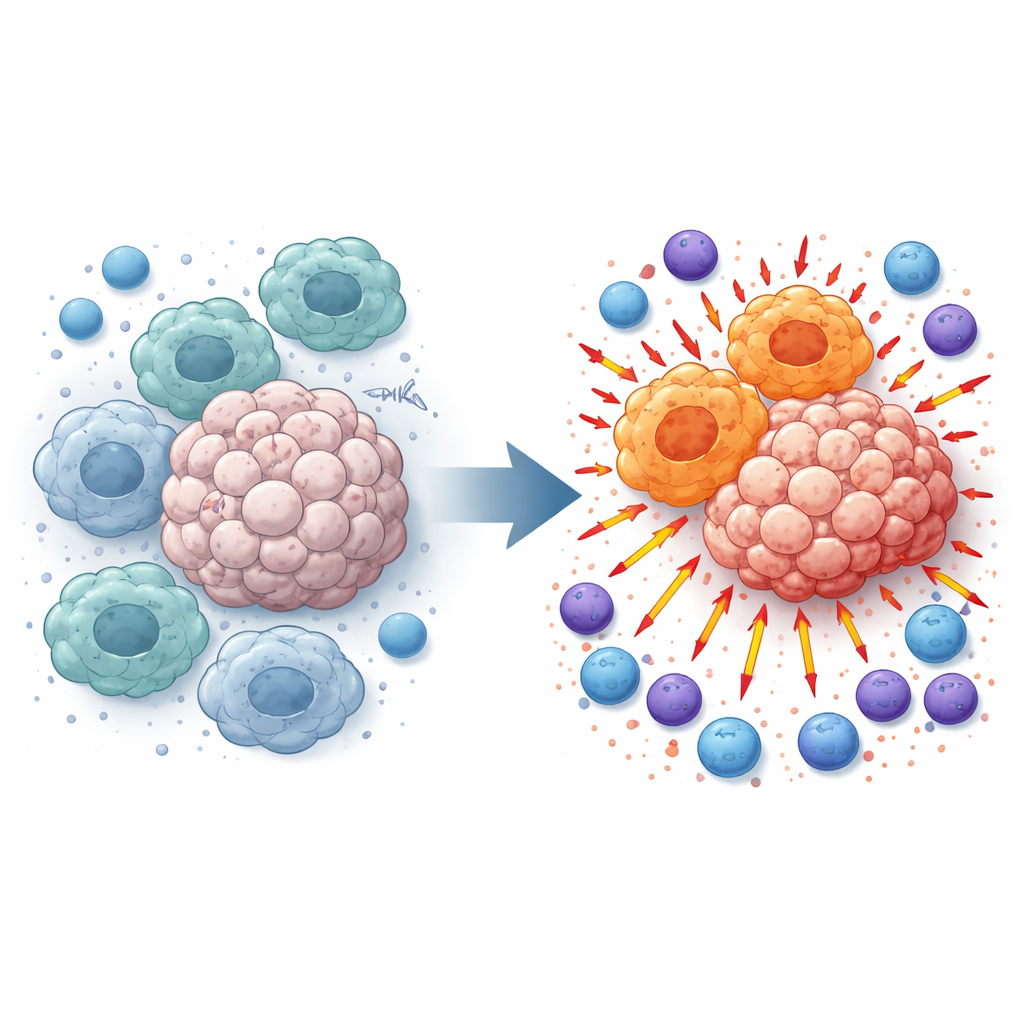
Makrofager patrullerar vävnader och slukar skräp, men inne i tumörer omprogrammeras de ofta till ett vårdande, tumörvänligt tillstånd. Dessa ”M2‑lika” makrofager dämpar inflammation och hindrar T‑celler och NK‑celler som annars skulle angripa cancer. Vid granskning av melanomprover från patienter och tumörbärande möss fann forskarna att TMEM175-nivåerna var högre i tumörer än i intilliggande normal vävnad och att nivåerna var starkt kopplade till detta suppressiva makrofagtillstånd. Den observationen ledde dem till frågan: vad händer om TMEM175 stängs av endast i myeloida celler såsom makrofager?
Att ta bort en lysosomal grindvakt förändrar balansen
Forskargruppen konstruerade möss där TMEM175 är utslaget specifikt i myeloida celler och planterade sedan melanom- eller lungcancerceller under huden eller i blodomloppet för att framkalla lungmetastaser. I dessa modeller växte tumörer i TMEM175‑deficienta möss långsammare och bildade färre metastatiska knutor. Detaljerad cellanalys visade att makrofager inne i dessa tumörer skiftade mot en ”M1‑lik” profil associerad med stark immunaktivering, medan den suppressiva M2‑lika populationen minskade. Samtidigt ansamlades betydligt fler CD4‑ och CD8‑T‑celler samt NK‑celler i tumörvävnaden och visade molekylära tecken på att vara aktiverade och redo att döda.
Hur celldelar tänder en inflammatorisk signal
För att avslöja de inre mekanismerna studerade forskarna benmärgsderiverade makrofager i odling. När dessa celler svalde fragment av döda tumörceller destabiliserades deras lysosomer, vilket ledde till läckage av enzymer som katepsin B och förändrade kalciumnivåer i omgivande vätska. I TMEM175‑deficienta makrofager var denna störning starkare, vilket ledde till kraftfull aktivering av ett molekylärt larmsystem kallat NLRP3‑inflammasomet. När detta blev aktivt utlöste komplexet frisättning av potenta budbärarmolekyler, inklusive cytokinerna IL‑1β och IL‑18. Blockering av enzymet kaspas‑1, eller neutralisering av IL‑1β eller IL‑18 med antikroppar, utsläckte i stor utsträckning den anti‑tumöreffekt som följde på TMEM175‑förlust hos möss, vilket visar att denna inflammatoriska kaskad är central för effekten.
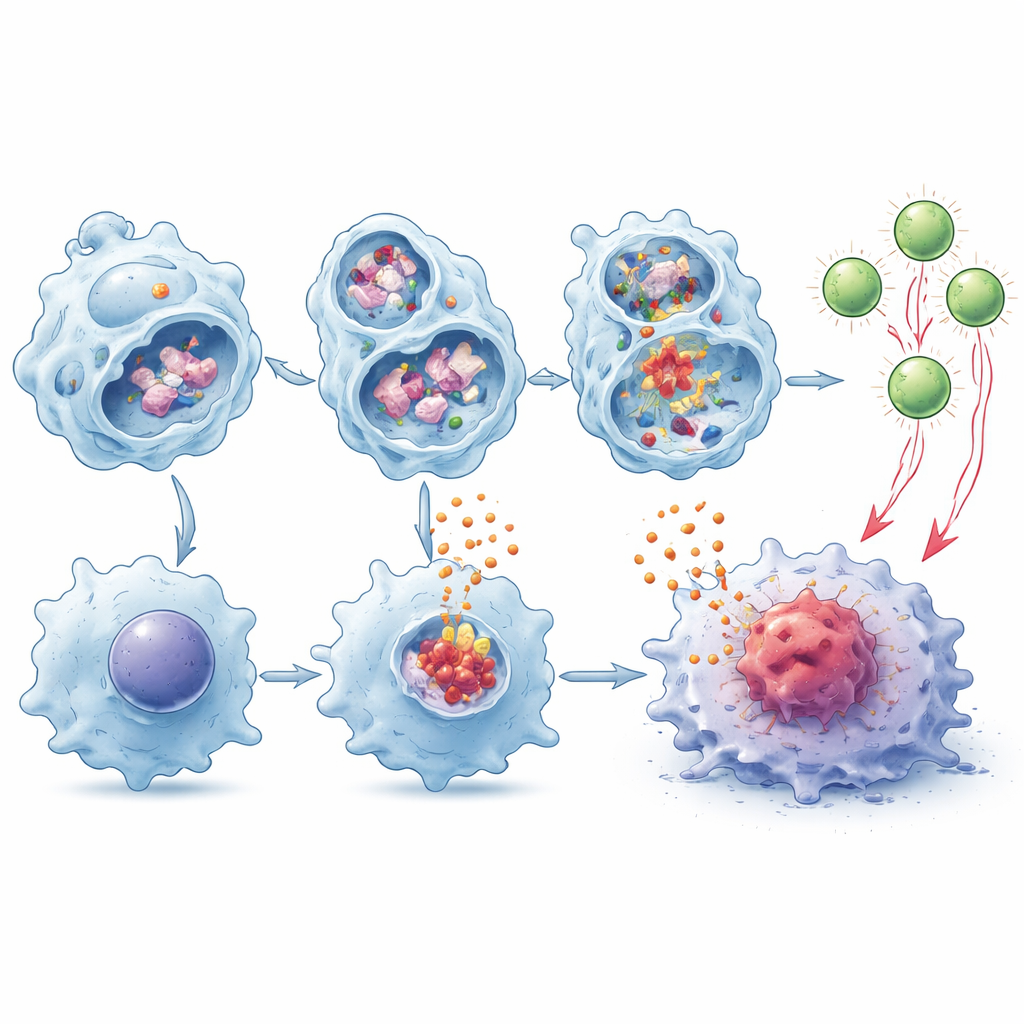
Hjälpa T‑celler att se och attackera tumörer
Makrofager gör mer än att utsöndra larm—de kan också sönderdela tumörproteiner och visa fragment på ytan för att väcka T‑celler, en process känd som korspresentation. Författarna fann att TMEM175‑deficienta makrofager bröt ner tumörmaterial långsammare inne i lysosomerna, vilket lämnade fler intakta fragment tillgängliga för presentation. I samodlingsförsök var dessa celler mycket bättre på att driva expansion och aktivering av tumörspecifika CD8‑T‑celler, och denna effekt förstärktes ytterligare i närvaro av IL‑1β och IL‑18. När sådana uppväckta T‑celler överfördes till tumörbärande möss som saknar egna CD8‑celler hämmande de tumörtillväxten mer effektivt än T‑celler utbildade av normala makrofager.
Stärka effekten av checkpoint‑terapi
Eftersom TMEM175‑deficienta tumörer var rika på aktiva T‑celler testade forskarna om detta tillstånd skulle svara annorlunda på anti‑PD‑1, en ofta använd checkpoint‑hämmare. Hos standardmöss påverkade anti‑PD‑1 knappt melanomtillväxten, vilket speglar den resistens som ofta ses i kliniken. I kontrast visade möss som saknade TMEM175 i makrofager markant mindre tumörer och mer tumörcelldöd när de fick samma läkemedel. Deras tumörer innehöll fler aktiverade makrofager, T‑celler och NK‑celler, vilket indikerar att omformningen av tumörmiljön genom TMEM175 gör etablerad immunterapi mer verkningsfull.
En ny kontrollpunkt för tumörmikromiljön
Sammanfattningsvis avslöjar studien TMEM175 som en molekylär strömbrytare som styr hur makrofager reagerar på döende tumörceller. När denna lysosomala jonkanal saknas destabiliseras tumörskräp lättare lysosomerna, kalciumnivåerna stiger och inflammasomet tänds och släpper loss IL‑1β och IL‑18. Samtidigt förbättrar den fördröjda nedbrytningen av tumörproteiner deras presentation för CD8‑T‑celler. Tillsammans omvandlar dessa förändringar makrofager från tumörmedhjälpare till starka allierade som samlar T‑celler och NK‑celler mot cancer och gör tumörer känsligare för anti‑PD‑1‑behandling. Medan läkemedel som selektivt blockerar TMEM175 och når tumörassocierade makrofager fortfarande behöver utvecklas, pekar arbetet på en lovande ny väg för kombinationsbaserad cancerimmunterapi.
Citering: Zhang, Z., li, X., Lu, T. et al. Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway. Nat Commun 17, 2770 (2026). https://doi.org/10.1038/s41467-026-69546-2
Nyckelord: tumörmikromiljö, makrofager, inflammasom, cancerimmunterapi, antigenkorspresentation