Clear Sky Science · zh
小鼠高亲和阳离子氨基酸转运蛋白1(CAT1)的氨基酸结合与病毒结合
细胞如何控制关键构件并应对病毒入侵
我们的细胞依赖某些氨基酸的稳定供应——这些微小分子既构建蛋白质又驱动关键反应。与此同时,一些病毒已经进化出劫持将这些营养物质输送入细胞的通道的能力。本研究以原子级细节揭示了小鼠中的这样一个通道CAT1,既将带正电的氨基酸穿过细胞膜,又充当导致白血病的病毒的入侵码头。理解这一双重角色有助于解释细胞如何感知营养、某些癌症如何得以生长,以及为什么特定病毒感染某些物种而不感染其他物种。
位于细胞表面的蛋白门卫
CAT1 位于细胞外膜,专门负责摄取三种带正电的氨基酸:精氨酸、赖氨酸和鸟氨酸。这些分子对于构建蛋白质、通过尿素循环排除有毒氨、激活生长通路以及生成如一氧化氮等信号分子都至关重要。当 CAT1 功能异常时,小鼠会在出生后不久死亡,而在人类中,相关的转运蛋白与卵巢癌和结肠癌有关。有趣的是,同一蛋白也是一种称为 Friend 小鼠白血病病毒的主要受体,该逆转录病毒利用 CAT1 识别并感染啮齿类细胞。
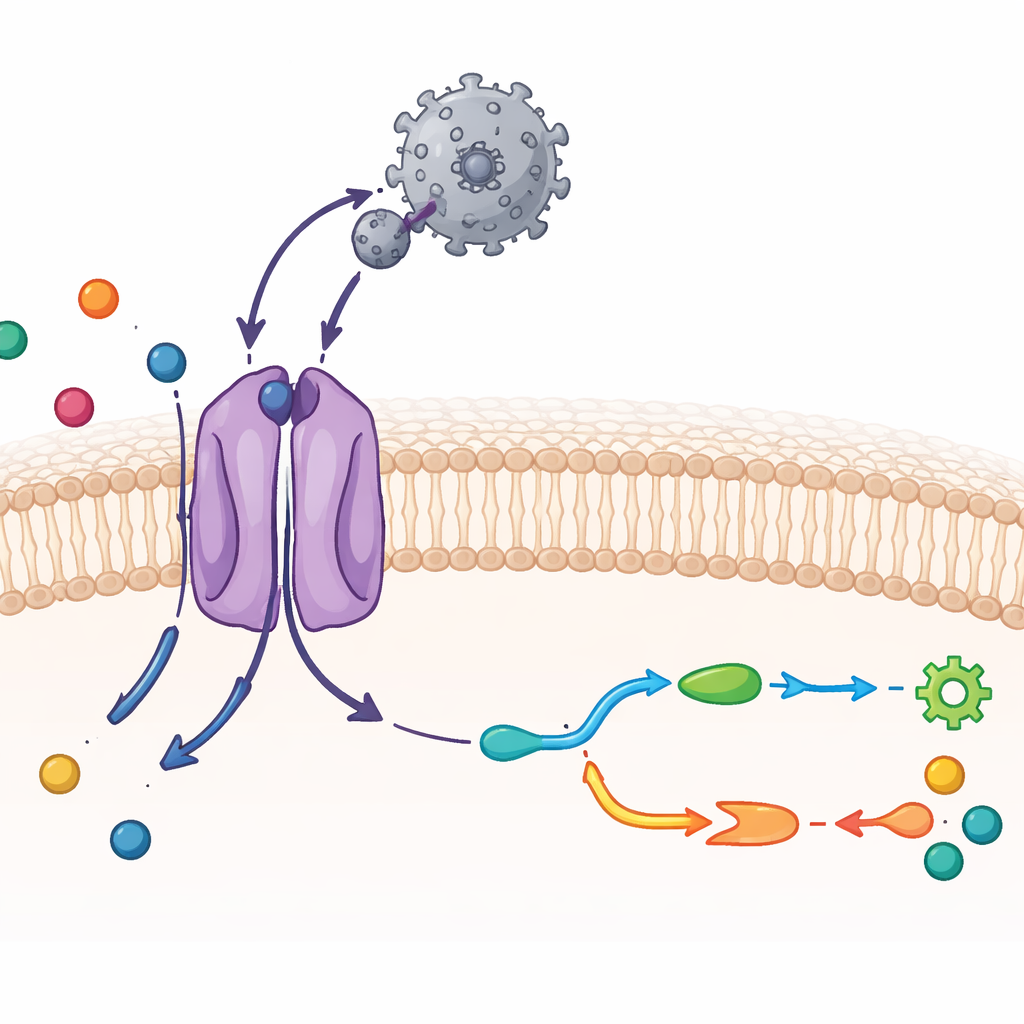
以原子级别观察 CAT1 与病毒的相互作用
研究者采用冷冻电子显微镜(一种能够在近原子分辨率下成像冷冻分子的技术)并结合生化实验。他们纯化了小鼠 CAT1 并将其与病毒的外部结合区域混合——一个紧凑的蛋白片段,可与转运蛋白结合。所得结构显示出一比一的复合体:单个病毒结合域附着在膜中的单个 CAT1 分子上。转运蛋白的大部分14个跨膜段都可见,其中包括该家族特有的两个额外跨膜段。病毒片段贴附在 CAT1 外侧暴露的一个环上,形成密集的氢键网络,解释了其异常紧密的结合。然而病毒蛋白本身几乎不改变形状,这有助于以很小的能量代价保持这种强相互作用。
CAT1 如何挑选并移动其货物
在 CAT1 内部,研究团队确认了精氨酸、赖氨酸和鸟氨酸结合的精确口袋。每种氨基酸的主链被一圈蛋白原子通过多个氢键固定,而侧链则被衬在一个由精确排列的侧基和一个关键的负电残基构成的腔体中。当该酸性残基或附近接触点通过突变被改变时,CAT1 在加入氨基酸后失去稳定性,显示出这些位点对识别的重要性。比较结合了精氨酸、赖氨酸和鸟氨酸的结构表明,CAT1 几乎以相同方式抓取这三者,仅为适应侧链长度的差异略作调整。这些细节解释了为何 CAT1 强烈偏好带正电的氨基酸并基本排斥中性氨基酸。
移动的门仍能抓住病毒
通过对比有无结合底物的 CAT1 成像,作者捕捉到了其工作循环的两个关键步骤。在一种状态下,货物位点对膜两侧都被封闭——一种“封闭”状态,氨基酸被锁在内部;在另一种状态下,该位点朝向细胞内开放,允许释放货物。这些变化涉及若干跨膜段的摆动运动和位于内侧表面一个柔性“闩锁”肽段,后者似乎控制朝向细胞的开放。值得注意的是,外侧与病毒结合的区域移动很小并在这些变动中保持牢固附着。这支持了早期证据:病毒对接与氨基酸转运在很大程度上是独立的——CAT1 即便在作为病毒受体时也能继续为细胞供给营养。
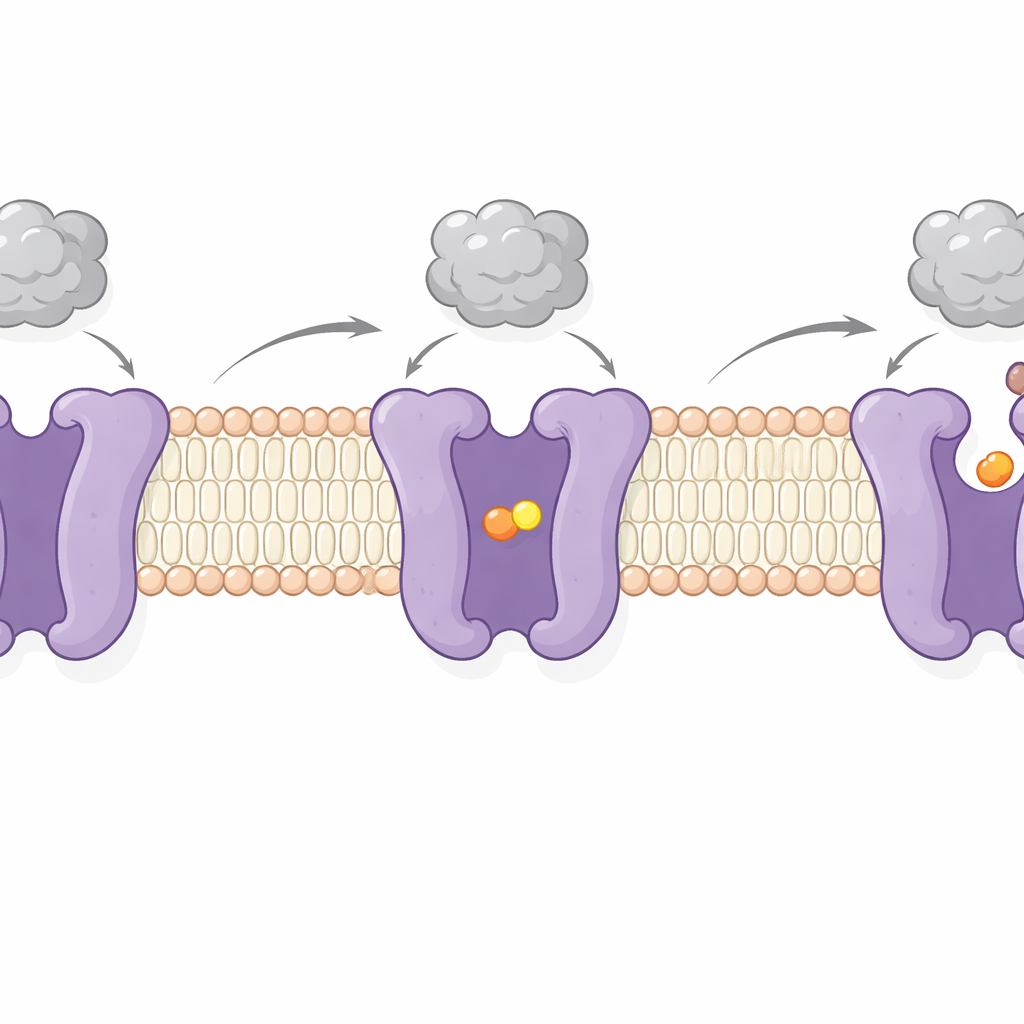
这一双重角色为何重要
通过精确描绘 CAT1 如何识别营养物和病毒,这项工作阐明了为何 Friend 白血病病毒能感染啮齿类但不能感染人类:病毒与 CAT1 的一个短外环结合,而该环在不同物种间差异显著。将小鼠该段置换到人类 CAT1 即足以在细胞实验中恢复病毒结合。结构还提示了 CAT1 如何帮助细胞感知精氨酸水平并将该信息传递给生长控制通路,并指出了可用于调节转运或阻断病毒入侵的具体位点。本质上,这项研究展示了单一膜蛋白如何既作为营养阀门又作为病毒抓手,不同的分子表面承担着维持生命与促进疾病的双重角色。
引用: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
关键词: 氨基酸转运, 膜蛋白结构, 病毒受体, 精氨酸代谢, 宿主嗜性