Clear Sky Science · fr
Fixation d’acides aminés et liaison virale par le transporteur cationique à haute affinité 1 (CAT1) de Mus musculus
Comment les cellules contrôlent des éléments constitutifs vitaux et font face à des envahisseurs viraux
Nos cellules dépendent d’un apport constant de certains acides aminés — de petites molécules qui construisent les protéines et alimentent des réactions clés. En parallèle, certains virus ont évolué pour détourner les mêmes portes d’entrée qui amènent ces nutriments dans les cellules. Cette étude révèle, au niveau atomique, comment l’une de ces portes chez la souris, nommée CAT1, transporte des acides aminés chargés positivement à travers la membrane cellulaire et sert en même temps de point d’attache pour un virus provoquant une leucémie. Comprendre ce double rôle aide à expliquer comment les cellules détectent les nutriments, comment certains cancers prospèrent et pourquoi des virus spécifiques infectent certaines espèces mais pas d’autres.
Le gardien protéique à la surface cellulaire
CAT1 se situe dans la membrane externe de la cellule et se spécialise dans l’importation de trois acides aminés chargés positivement : arginine, lysine et ornithine. Ces molécules sont essentielles pour former les protéines, éliminer l’ammoniac toxique via le cycle de l’urée, activer des voies de croissance et générer des molécules de signalisation comme le monoxyde d’azote. Lorsque CAT1 ne fonctionne pas correctement, les souris meurent peu après la naissance, et chez l’homme le transporteur apparenté est lié à des cancers de l’ovaire et du côlon. Fait intrigant, la même protéine sert aussi de récepteur principal pour un rétrovirus murin connu sous le nom de Friend murine leukemia virus, qui utilise CAT1 pour reconnaître et infecter les cellules de rongeurs.
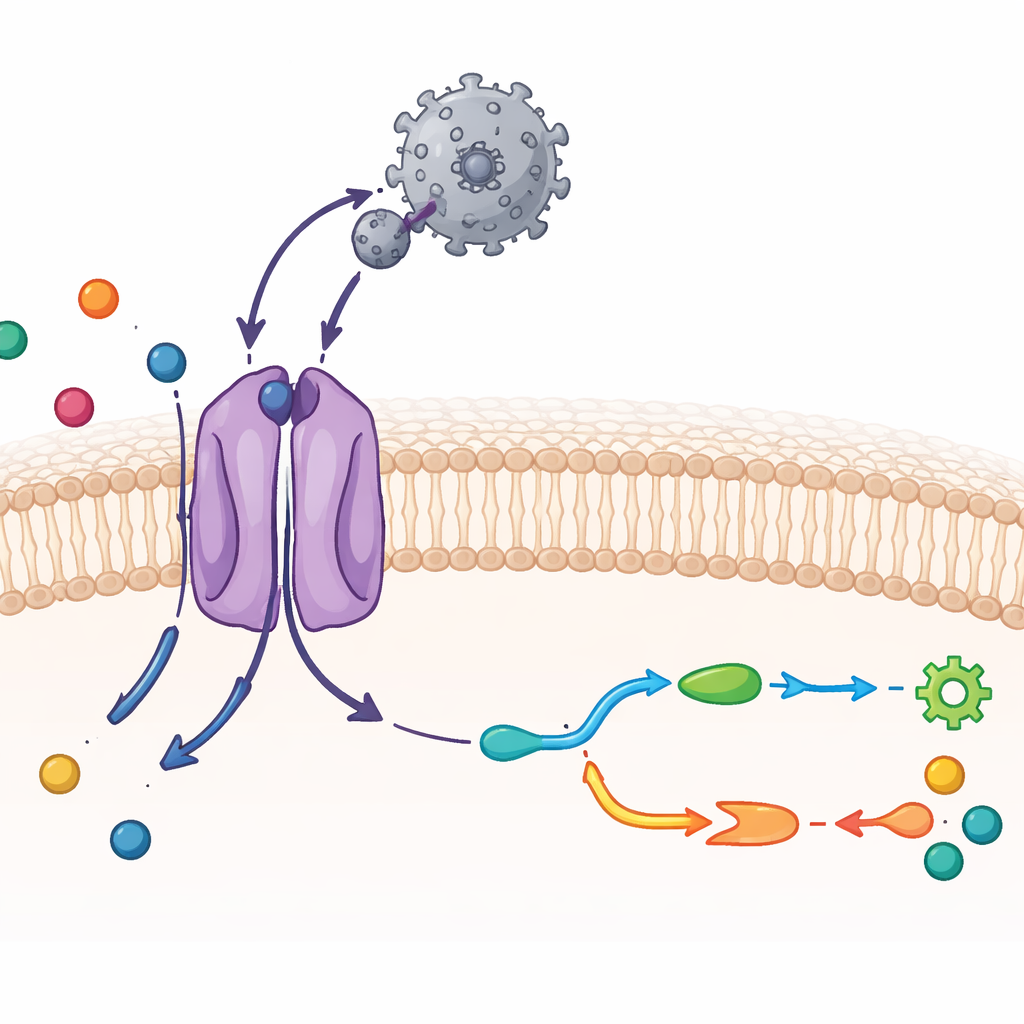
Voir CAT1 et un virus au détail atomique
Les chercheurs ont utilisé la cryo–microscopie électronique, une technique qui image des molécules gelées à une résolution quasi atomique, associée à des tests biochimiques. Ils ont purifié le CAT1 de souris et l’ont mis en présence de la région externe de liaison du virus, un fragment protéique compact qui s’accroche au transporteur. La structure obtenue montre un complexe un pour un : un seul domaine de liaison viral attaché à une seule molécule de CAT1 dans la membrane. La plupart des 14 segments traversant la membrane du transporteur ont pu être visualisés, y compris deux segments supplémentaires uniques à cette famille. Le fragment viral enlace une boucle exposée sur la face externe de CAT1 et forme un réseau dense de liaisons hydrogène, ce qui explique son maintien extraordinairement serré. Pourtant, la protéine virale elle-même change à peine de conformation, ce qui contribue à préserver cette interaction forte avec peu de coût énergétique.
Comment CAT1 choisit et déplace sa cargaison
À l’intérieur de CAT1, l’équipe a identifié la poche précise où se lient l’arginine, la lysine et l’ornithine. Le squelette de chaque acide aminé est maintenu en place par un cercle d’atomes protéiques formant de multiples liaisons hydrogène, tandis que les chaînes latérales s’insèrent dans une cavité bordée de groupes latéraux positionnés avec précision et d’un résidu négativement chargé critique. Lorsque ce résidu acide ou des points de contact voisins ont été modifiés par mutation, CAT1 a perdu sa capacité à se stabiliser lors de l’ajout d’acides aminés, révélant leur importance pour la reconnaissance. La comparaison des structures avec l’arginine, la lysine et l’ornithine liées a montré que CAT1 serre les trois presque de la même manière, ne s’ajustant que légèrement pour accommoder les différences de longueur des chaînes latérales. Ces détails expliquent pourquoi CAT1 préfère fortement les acides aminés chargés positivement et exclut en grande partie les neutres.
Une porte mobile qui garde pourtant le virus
En imageant CAT1 avec et sans acide aminé lié, les auteurs ont capturé deux étapes clés de son cycle de fonctionnement. Dans l’une, le site de cargaison est isolé des deux côtés de la membrane — un état « occlus » dans lequel l’acide aminé est enfermé à l’intérieur. Dans l’autre, le site s’ouvre vers l’intérieur de la cellule, permettant la libération de la cargaison. Ces changements impliquent des mouvements d’oscillation de plusieurs segments transmembranaires et d’un peptide « verrou » flexible sur la face interne qui semble contrôler l’ouverture vers le cytosol. Notamment, la région de liaison virale sur la face externe ne bouge que légèrement et reste solidement attachée pendant ces déplacements. Cela confirme des preuves antérieures selon lesquelles le docking viral et le transport d’acides aminés sont en grande partie indépendants — CAT1 peut continuer à nourrir la cellule tout en servant de récepteur viral.
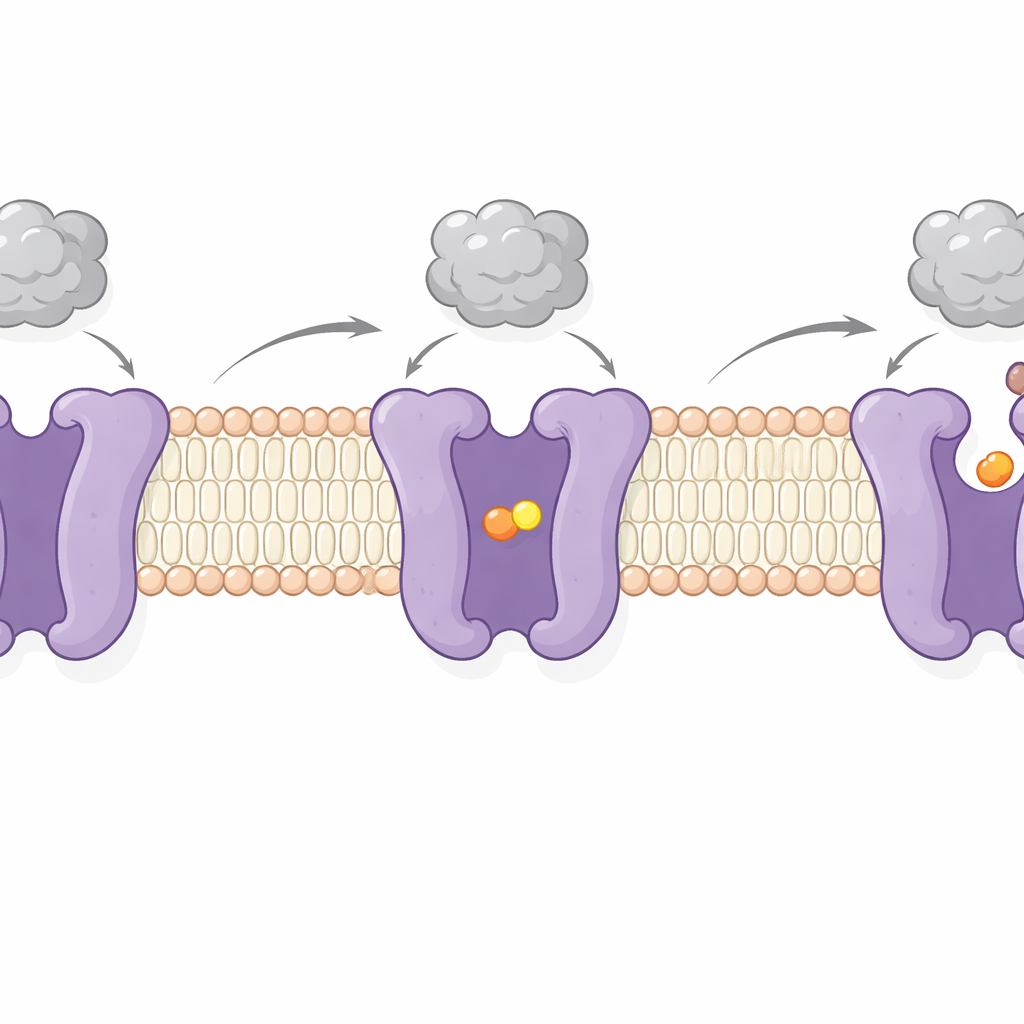
Pourquoi ce double rôle est important
En cartographiant précisément comment CAT1 reconnaît à la fois les nutriments et un virus, ce travail clarifie pourquoi le Friend leukemia virus infecte les rongeurs mais pas les humains : le virus s’engage sur une courte boucle externe de CAT1 qui diffère sensiblement selon les espèces. Le remplacement de ce segment de la souris par celui de l’humain suffit à restaurer la liaison virale dans des tests cellulaires. Les structures suggèrent aussi comment CAT1 aide les cellules à détecter les niveaux d’arginine et à transmettre cette information aux voies de contrôle de la croissance, et elles indiquent des sites précis où des médicaments ou des modificateurs chimiques pourraient moduler le transport ou bloquer l’entrée virale. En substance, l’étude montre comment une seule protéine membranaire peut agir à la fois comme une vanne nutritive et comme une poignée virale, différentes faces d’une même molécule servant des rôles essentiels à la vie et favorisant la maladie.
Citation: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Mots-clés: transport d’acides aminés, structure des protéines membranaires, récepteurs viraux, métabolisme de l’arginine, tropisme de l’hôte