Clear Sky Science · tr
Yüksek afiniteli Kationik Amino Asit Taşıyıcı 1 (CAT1) — Mus musculus’tan amino asit ve viral bağlanma
Hücreler Hayati Yapı Taşlarını Nasıl Denetler ve Viral Saldırılarla Nasıl Yüzyüze Gelir
Hücrelerimiz, proteinleri inşa eden ve temel reaksiyonları destekleyen küçük moleküller olan belirli amino asitlerin düzenli akışına bağımlıdır. Aynı zamanda bazı virüsler, bu besinleri hücre içine alan kapıları ele geçirmek üzere evrimleşmiştir. Bu çalışma, farelerdeki CAT1 adı verilen ve hem pozitif yüklü amino asitleri hücre zarından taşıyan hem de lösemiye yol açabilen bir virüs için giriş iskelesi görevi gören bir kapının atomik ayrıntıda nasıl çalıştığını gösteriyor. Bu çift işlevin anlaşılması, hücrelerin besinleri nasıl algıladığını, bazı kanserlerin nasıl geliştiğini ve neden belirli virüslerin bazı türleri enfekte edip diğerlerini etkilemediğini açıklamaya yardımcı olur.
Hücre Yüzeyindeki Protein Kapısı
CAT1, hücrenin dış zarında yer alır ve üç pozitif yüklü amino asit — arginin, lizin ve ornitin — ithal etmekte özelleşmiştir. Bu moleküller proteinlerin biçimlenmesi, üre döngüsüyle toksik amonyağın uzaklaştırılması, büyüme yollarının etkinleştirilmesi ve nitrik oksit gibi haberci moleküllerin üretilmesi için hayati öneme sahiptir. CAT1 düzgün çalışmadığında fareler doğumdan kısa süre sonra ölür ve insanlarda ilişkilendirilen benzer taşıyıcı, over ve kolon kanserleriyle bağlantılıdır. İlginç biçimde aynı protein, Friend murine leukemia virus olarak bilinen bir fare retrovirüsü için ana reseptör görevi de görür; bu virüs CAT1’i kullanarak kemirgen hücreleri tanır ve enfekte eder.
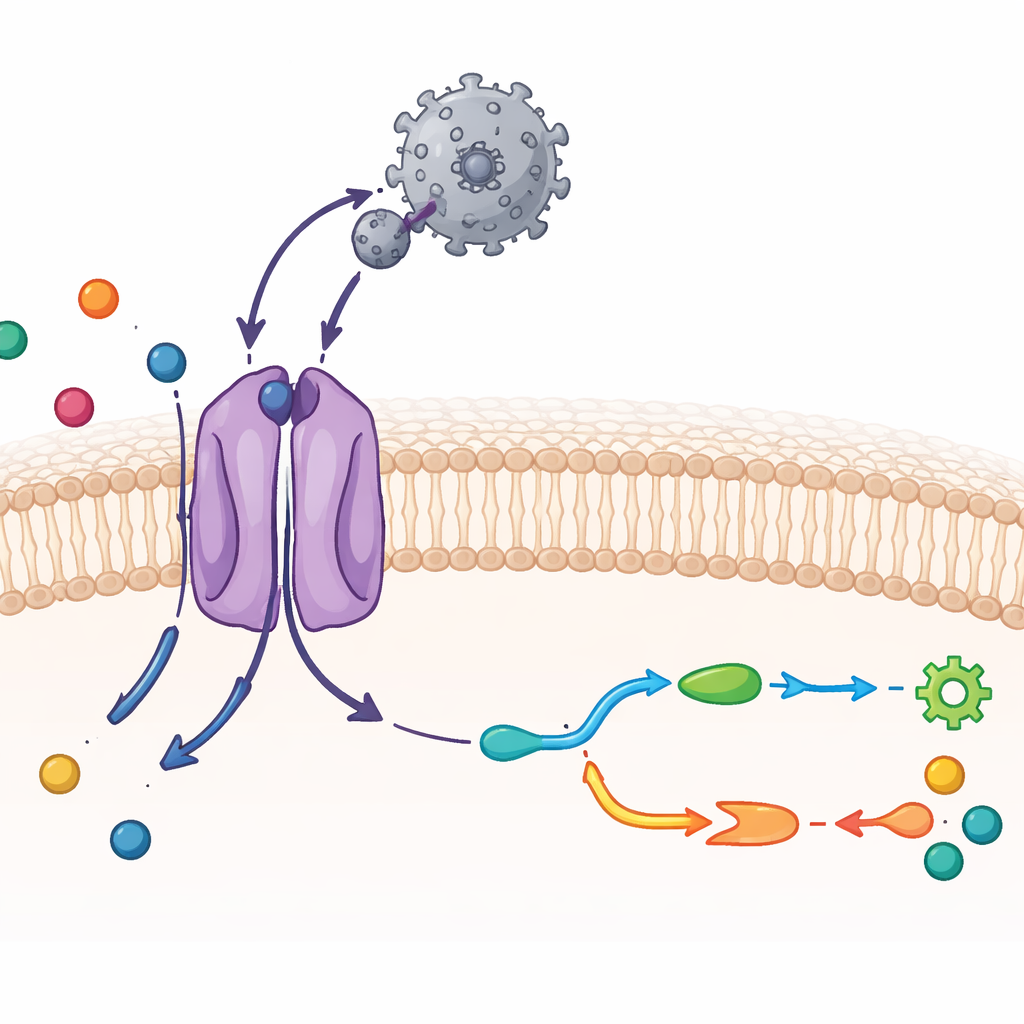
CAT1 ve Bir Virüsü Atomik Ayrıntıda Görmek
Araştırmacılar, donmuş molekülleri yakın-atomik çözünürlükte görüntüleyen kriyo-elektron mikroskopesini biyokimyasal testlerle birleştirdi. Fare CAT1’i saflaştırdılar ve taşıyıcıya tutunan kompakt bir protein parçası olan viral dış bağlanma bölgesi ile karıştırdılar. Ortaya çıkan yapı bir-çapa bir karma gösteriyor: molemin membranda tek bir CAT1 molekülüne bağlı tek bir viral bağlanma alanı. Taşıyıcının 14 zar geçişli segmentinin çoğu, aileye özgü iki ek segment de dahil olmak üzere, görselleştirilebildi. Viral fragment, CAT1’in dış tarafında açıkta kalan bir halkayı sardı ve yoğun bir hidrojen bağı ağı oluşturdu; bu, olağanüstü sıkı tutuşu açıklıyor. Buna karşın viral proteinin kendisi neredeyse şekil değiştirmiyor, bu da az enerji maliyetiyle güçlü etkileşimin korunmasına yardımcı oluyor.
CAT1 Yükünü Nasıl Seçer ve Taşır
CAT1’in içinde ekip, arginin, lizin ve ornitinin bağlandığı kesin cebi tanımladı. Her bir amino asidin omurgası, çoklu hidrojen bağları oluşturan bir protein atom halkası tarafından yerinde tutulurken, yan zincirler dikkatle konumlandırılmış yan gruplarla ve tek bir kritik negatif yüklü kalıntıyla döşeli bir boşluğa yerleşir. Bu asidik kalıntı veya yakın temas noktaları mutasyonla değiştirildiğinde CAT1, amino asit eklendiğinde stabil kalma yeteneğini yitirdi; bu da tanımada bu kalıntıların önemini ortaya koydu. Arginin, lizin ve ornitin bağlanmış yapılarının karşılaştırılması, CAT1’in bu üçünü neredeyse aynı şekilde kavradığını, sadece yan zincir uzunluklarındaki farkları karşılamak için hafifçe ayarlandığını gösterdi. Bu ayrıntılar CAT1’in neden pozitif yüklü amino asitleri güçlü biçimde tercih ettiğini ve nötr olanları büyük ölçüde dışladığını açıklar.
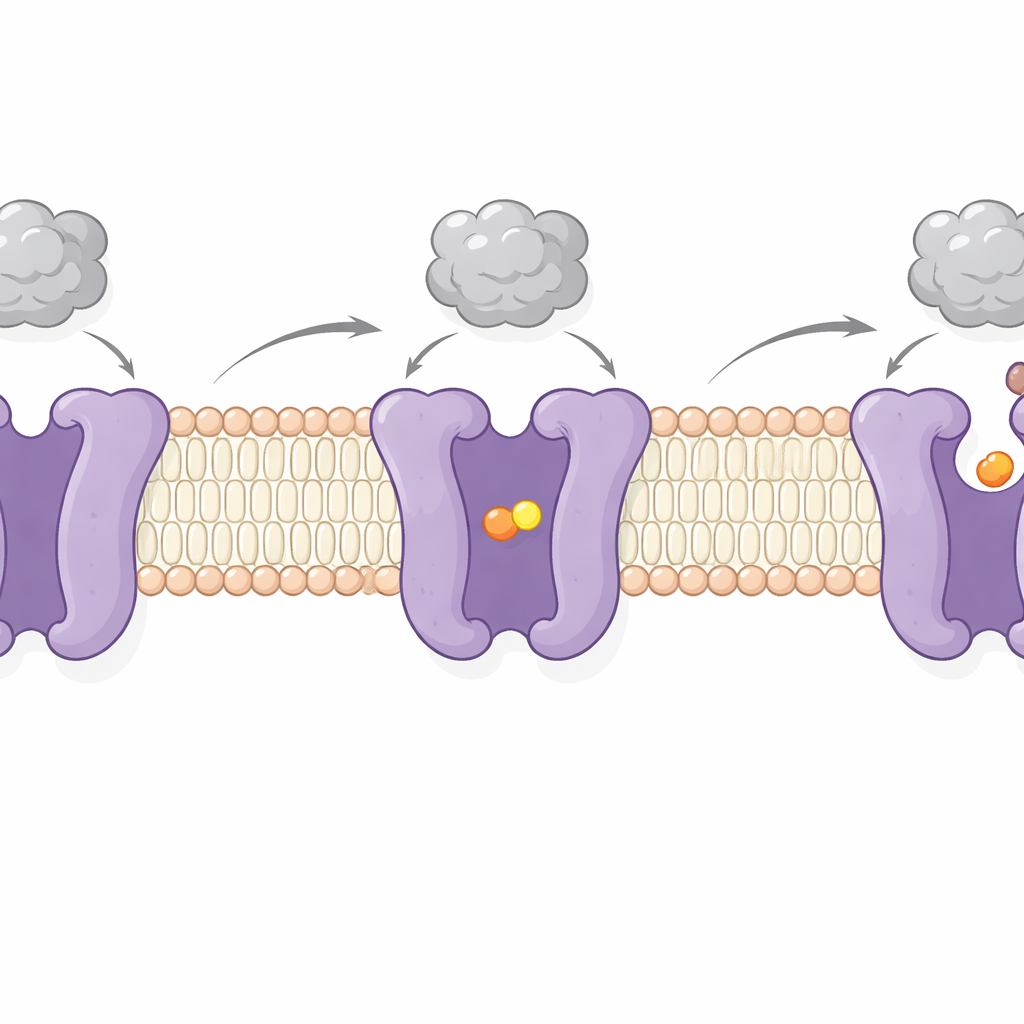
Hareket Eden Bir Kapı Ama Virüsü Hâlâ Tutuyor
Amino asit bağlı ve bağlı olmayan CAT1’i görüntüleyerek yazarlar çalışma döngüsünün iki ana adımını yakaladı. Birinde, yükleme bölgesi zarın her iki tarafından da izole edilir—amino asitin içinde kilitlendiği “oklüzif” durum. Diğerinde ise bölge hücre iç tarafına açılarak yükün serbest bırakılmasına izin verir. Bu değişiklikler, birkaç zar-geçişli segmentin sallanan hareketlerini ve iç yüzeydeki açılmayı kontrol ediyor gibi görünen esnek bir “kilit” peptidini içerir. Önemli olarak, dış taraftaki virüs-bağlanma bölgesi yalnızca hafifçe hareket eder ve bu değişimler sırasında sıkıca bağlı kalır. Bu, viral kenetlenme ile amino asit taşımanın büyük ölçüde bağımsız olduğu yönündeki önceki kanıtları destekler—CAT1, viral reseptör görevi görürken bile hücreyi beslemeye devam edebilir.
Bu Çift Rol Neden Önemli
CAT1’in hem besinleri hem de bir virüsü nasıl tanıdığını kesin olarak haritalayarak bu çalışma, Friend lösemi virüsünün kemirgenleri neden enfekte edip insanları enfekte etmediğini açıklığa kavuşturuyor: virüs, türler arasında belirgin biçimde farklılık gösteren kısa bir dış CAT1 halkasına bağlanıyor. Fareden insan CAT1’ine bu segmentin aktarılması, hücre testlerinde viral bağlanmayı geri getirmek için yeterli oluyor. Yapılar ayrıca CAT1’in arginin seviyelerini nasıl algılamaya ve bu bilgiyi büyüme-kontrol yollarına iletmeye yardımcı olabileceğine dair ipuçları veriyor ve taşıma işlevini ayarlayabilecek veya viral girişi engelleyebilecek ilaçların ya da kimyasal düzenleyicilerin hedefleyebileceği belirli bölgeleri işaretliyor. Özünde çalışma, tek bir zar proteininin hem bir besin vanasi hem de bir viral tutacak olarak nasıl işlev görebileceğini; aynı molekülün farklı yüzlerinin yaşamı sürdürücü ve hastalığı teşvik edici rolleri nasıl üstlendiğini gösteriyor.
Atıf: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Anahtar kelimeler: amino asit taşınımı, zar proteini yapısı, viral reseptörler, arginin metabolizması, konak tropizmi