Clear Sky Science · pl
Wiązanie aminokwasów i wirusa przez wysokoafinitywny kationowy transporter aminokwasów 1 (CAT1) z Mus musculus
Jak komórki kontrolują niezbędne cegiełki i stają wobec wirusowych najeźdźców
Nasze komórki polegają na stałym dopływie niektórych aminokwasów — małych cząsteczek, które budują białka i napędzają kluczowe reakcje. Jednocześnie niektóre wirusy wyewoluowały, by przejmować bramki, przez które te składniki odżywcze trafiają do komórek. Badanie to ukazuje, w skali atomowej, jak jedna z takich bramek u myszy, nazwana CAT1, zarówno transportuje dodatnio naładowane aminokwasy przez błonę komórkową, jak i służy jako punkt wejścia dla wirusa wywołującego białaczkę. Zrozumienie tej podwójnej roli pomaga wyjaśnić, jak komórki wykrywają składniki odżywcze, jak niektóre nowotwory prosperują oraz dlaczego konkretne wirusy zakażają jedne gatunki, a nie inne.
Bramkarz białkowy na powierzchni komórki
CAT1 osadza się w zewnętrznej błonie komórkowej i specjalizuje się w pobieraniu trzech dodatnio naładowanych aminokwasów: argininy, lizyny i ornityny. Cząsteczki te są niezbędne do kształtowania białek, usuwania toksycznego amoniaku w cyklu mocznikowym, włączania szlaków wzrostu oraz wytwarzania przekaźników, takich jak tlenek azotu. Gdy CAT1 nie funkcjonuje prawidłowo, myszy umierają krótko po urodzeniu, a u ludzi związany transporter jest powiązany z nowotworami jajnika i jelita grubego. Co ciekawe, to samo białko pełni także rolę głównego receptora dla mysiego retrowirusa znanego jako Friend murine leukemia virus, który wykorzystuje CAT1 do rozpoznawania i infekowania komórek gryzoni.
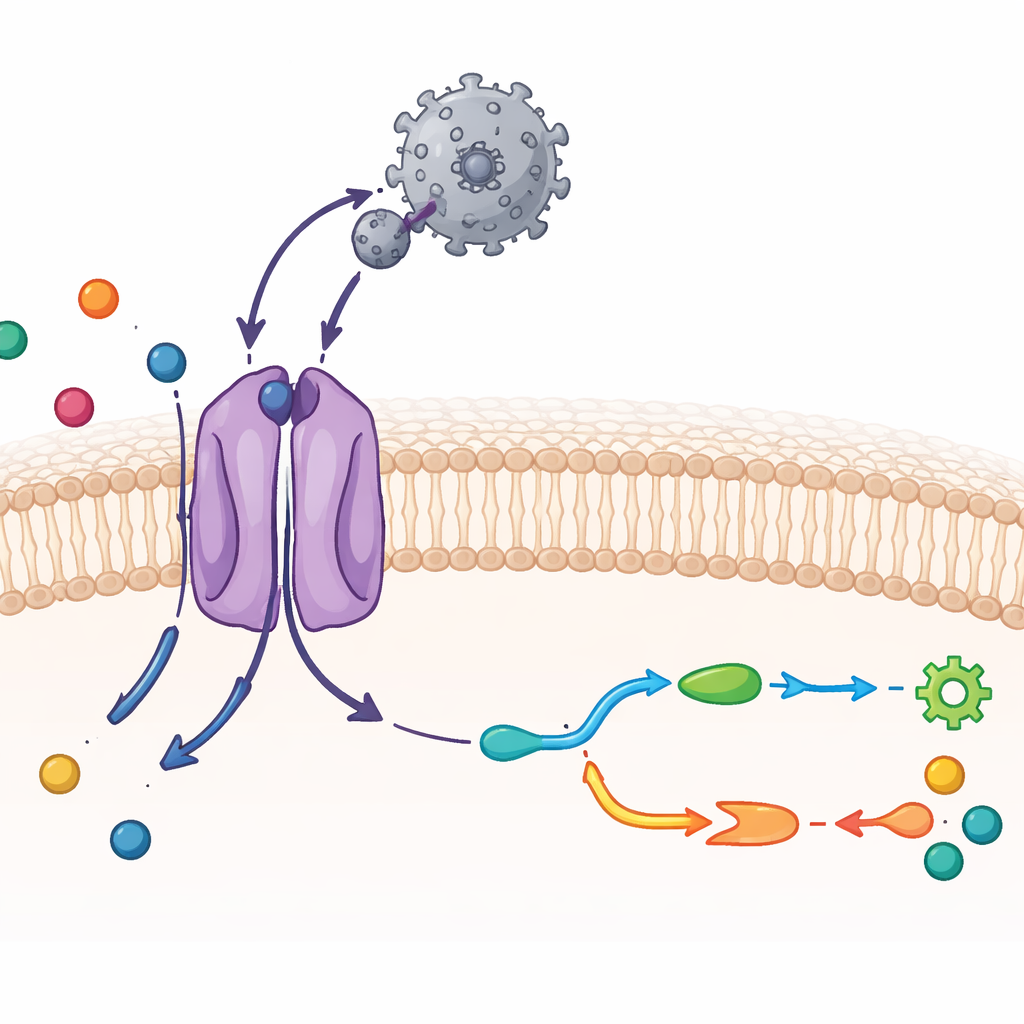
Obserwacja CAT1 i wirusa w szczegółach atomowych
Naukowcy zastosowali krioelektronową mikroskopię — technikę obrazowania zamrożonych cząsteczek w niemal atomowej rozdzielczości — wraz z testami biochemicznymi. Oczyszczono mysiego CAT1 i zmieszano go z zewnętrznym regionem wiążącym wirusa, zwartym fragmentem białka, który zaczepia się o transporter. Otrzymana struktura pokazuje kompleks jeden do jednego: pojedynczą domenę wiążącą wirusa przyczepioną do pojedynczej cząsteczki CAT1 w błonie. Większość z 14 segmentów przechodzących przez błonę transportera udało się zobrazować, w tym dwa dodatkowe segmenty charakterystyczne dla tej rodziny. Fragment wirusowy obejmuje odsłoniętą pętlę po stronie zewnętrznej CAT1 i tworzy gęstą sieć wiązań wodorowych, co tłumaczy jego niezwykle silne przytwierdzenie. Sam białkowy fragment wirusa prawie nie zmienia kształtu, co pomaga utrzymać tę silną interakcję przy niskim koszcie energetycznym.
Jak CAT1 wybiera i przemieszcza swój ładunek
Wnętrze CAT1 zawiera precyzyjną kieszeń, w której wiążą się arginina, lizyna i ornityna. Szkielet każdego aminokwasu jest utrzymywany przez pierścień atomów białkowych tworzących liczne wiązania wodorowe, podczas gdy łańcuchy boczne są osadzone w wnęce wyłożonej starannie rozmieszczonymi grupami bocznymi i jednym krytycznym resztą o ładunku ujemnym. Gdy tę kwaśną resztę lub pobliskie punkty kontaktu zmieniano przez mutację, CAT1 tracił zdolność stabilizacji po dodaniu aminokwasów, ujawniając ich znaczenie dla rozpoznawania. Porównanie struktur z związanymi argininą, lizyną i ornityną wykazało, że CAT1 uchwytuje wszystkie trzy niemal w ten sam sposób, dopasowując jedynie nieznacznie konfigurację do różnic w długości łańcucha bocznego. Te szczegóły wyjaśniają, dlaczego CAT1 wyraźnie preferuje dodatnio naładowane aminokwasy i w dużej mierze wyklucza aminokwasy obojętne.
Ruchoma brama, która wciąż trzyma wirusa
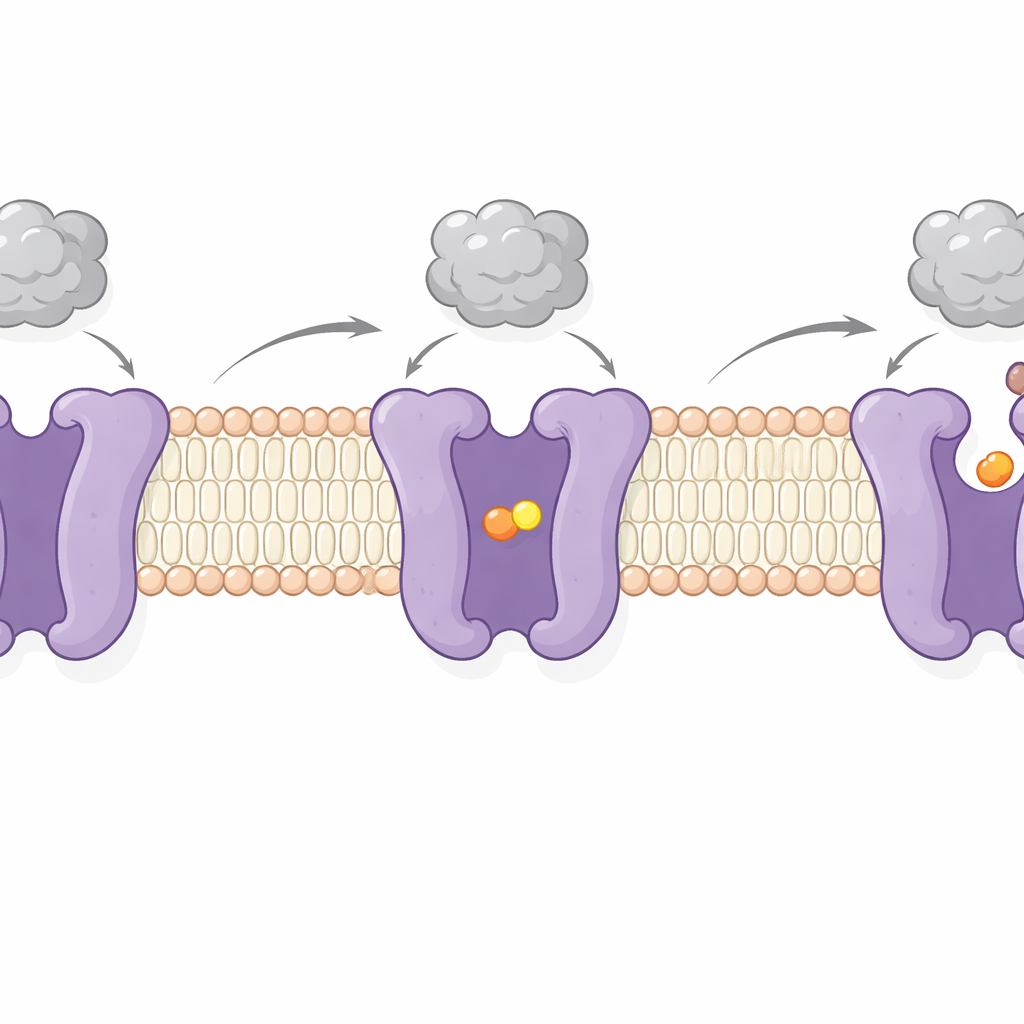
Obrazując CAT1 z aminokwasem i bez niego, autorzy uchwycili dwa kluczowe etapy jego cyklu pracy. W jednym miejscu wiązania jest zamknięte od obu stron błony — stan „okludowany”, w którym aminokwas jest uwięziony wewnątrz. W drugim miejsce otwiera się w stronę wnętrza komórki, co pozwala na uwolnienie ładunku. Zmiany te obejmują ruchy wahadłowe kilku segmentów przechodzących przez błonę oraz elastycznego peptydu „zatrzasku” po wewnętrznej stronie, który wydaje się kontrolować otwieranie w kierunku cytoplazmy. Co istotne, obszar wiązania wirusa po stronie zewnętrznej porusza się tylko nieznacznie i pozostaje mocno przymocowany podczas tych przemian. Wspiera to wcześniejsze dowody, że dokowanie wirusa i transport aminokwasów są w dużej mierze od siebie niezależne — CAT1 może dalej zasilać komórkę, jednocześnie pełniąc rolę receptora wirusa.
Dlaczego ta podwójna rola ma znaczenie
Mapując dokładnie, jak CAT1 rozpoznaje zarówno składniki odżywcze, jak i wirusa, praca ta wyjaśnia, dlaczego wirus Friend zakaża gryzonie, a nie ludzi: wirus angażuje krótką zewnętrzną pętlę CAT1, która różni się znacząco między gatunkami. Wstawienie tego segmentu z mysiego białka do ludzkiego CAT1 wystarcza, by przywrócić wiązanie wirusa w testach komórkowych. Struktury sugerują też, jak CAT1 pomaga komórkom wyczuwać poziomy argininy i przekazywać tę informację do szlaków kontrolujących wzrost, oraz wskazują konkretne miejsca, w których leki lub modyfikatory chemiczne mogłyby modulować transport lub blokować wejście wirusa. W istocie badanie pokazuje, jak pojedyncze białko błonowe może działać zarówno jako zawór odżywczy, jak i uchwyt wirusowy, z różnymi powierzchniami tej samej cząsteczki służącymi rolom podtrzymującym życie i sprzyjającym chorobie.
Cytowanie: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Słowa kluczowe: transport aminokwasów, budowa białek błonowych, receptory wirusowe, metabolizm argininy, tropizm gospodarza