Clear Sky Science · de
Aminosäure- und Virusbindung durch den hochaffinen kationischen Aminosäuretransporter 1 (CAT1) aus Mus musculus
Wie Zellen lebenswichtige Bausteine regulieren und Viren begegnen
Unsere Zellen sind auf einen stetigen Fluss bestimmter Aminosäuren angewiesen — kleine Moleküle, die Proteine aufbauen und zentrale Reaktionen antreiben. Gleichzeitig haben einige Viren Wege entwickelt, genau jene Tore zu kapern, die diese Nährstoffe in die Zellen bringen. Diese Studie zeigt auf atomarer Ebene, wie ein solches Tor bei Mäusen, genannt CAT1, sowohl positiv geladene Aminosäuren durch die Zellmembran transportiert als auch als Andockstelle für ein leukaemieverursachendes Virus dient. Das Verständnis dieser Doppelfunktion erklärt, wie Zellen Nährstoffe wahrnehmen, wie manche Tumoren gedeihen und warum bestimmte Viren einige Arten, aber nicht andere, infizieren.
Der Protein-Wächter an der Zelloberfläche
CAT1 sitzt in der äußeren Zellmembran und ist spezialisiert auf den Import von drei positiv geladenen Aminosäuren: Arginin, Lysin und Ornithin. Diese Moleküle sind entscheidend für die Proteingestaltung, die Beseitigung toxischer Ammoniak über den Harnstoffzyklus, die Aktivierung von Wachstumswegen und die Erzeugung von Signalstoffen wie Stickstoffmonoxid. Funktioniert CAT1 nicht richtig, sterben Mäuse kurz nach der Geburt, und beim Menschen ist der verwandte Transporter mit Ovar- und Darmkrebs in Verbindung gebracht worden. Auffällig ist, dass dasselbe Protein auch als Hauptrezeptor für ein Maus-Retrovirus, das als Friend murine leukemia virus bekannt ist, dient und dieses Virus CAT1 zur Erkennung und Infektion von Nagetierzellen nutzt.
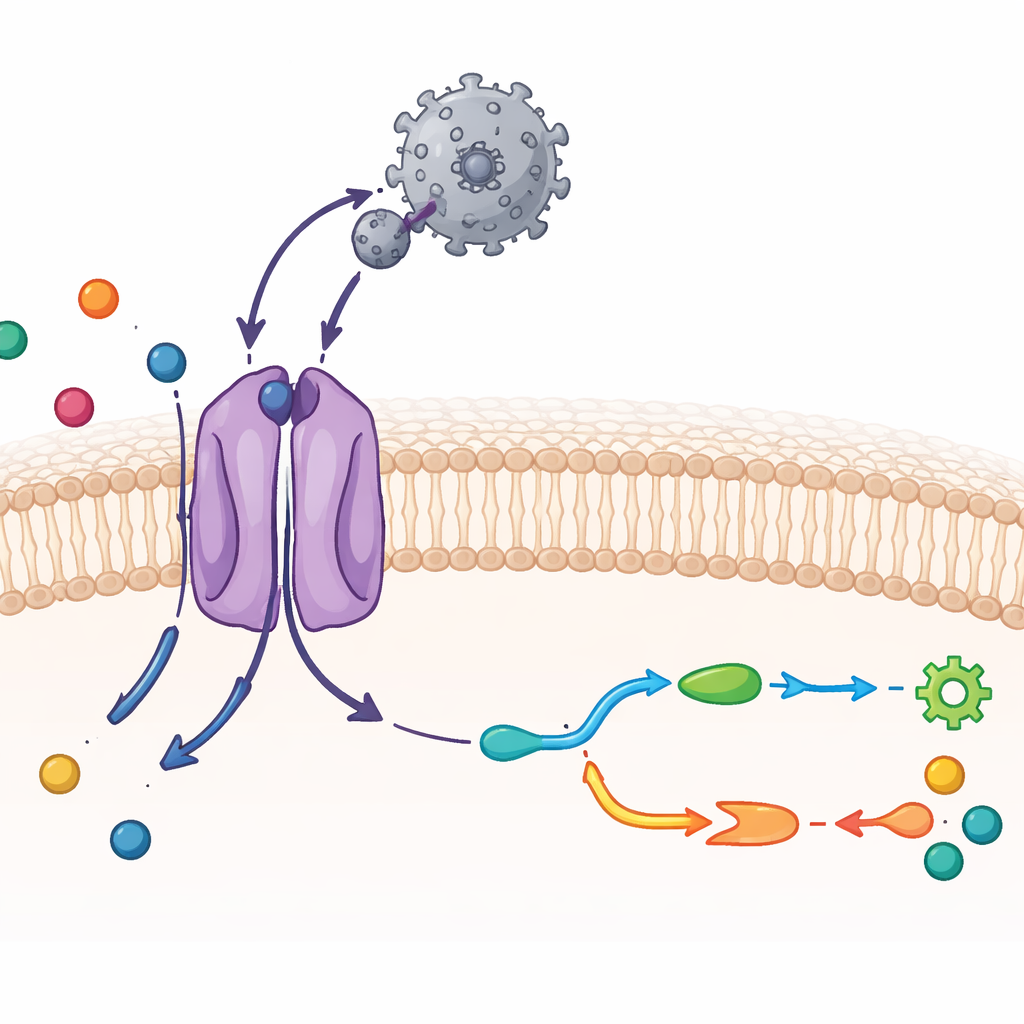
CAT1 und ein Virus in atomarer Auflösung sehen
Die Forschenden verwendeten Kryo-Elektronenmikroskopie, eine Technik, die eingefrorene Moleküle in annähernder atomarer Auflösung abbildet, zusammen mit biochemischen Tests. Sie reinigten Maus-CAT1 und mischten ihn mit der äußeren Bindungsregion des Virus, einem kompakten Proteinfragment, das an den Transporter bindet. Die resultierende Struktur zeigt einen Eins-zu-eins-Komplex: eine einzelne virale Bindungsdomäne, die an ein einzelnes CAT1-Molekül in der Membran gebunden ist. Die meisten der 14 membranüberspannenden Segmente des Transporters konnten dargestellt werden, einschließlich zweier zusätzlicher Segmente, die für diese Familie einzigartig sind. Das virale Fragment umschließt eine exponierte Schleife auf der Außenseite von CAT1 und bildet ein dichtes Netz von Wasserstoffbrücken, was seine außerordentlich starke Bindung erklärt. Zugleich verändert sich das virale Protein selbst kaum in seiner Form, was hilft, die starke Wechselwirkung bei geringem energetischem Aufwand aufrechtzuerhalten.
Wie CAT1 seine Fracht auswählt und bewegt
Im Inneren von CAT1 identifizierte das Team die genaue Tasche, in der Arginin, Lysin und Ornithin binden. Das Rückgrat jeder Aminosäure wird von einem Ring aus Proteinatomen in Position gehalten, die mehrere Wasserstoffbrücken ausbilden, während die Seitenketten in einer Höhlung liegen, die von sorgfältig positionierten Gruppen und einer einzelnen, kritischen negativ geladenen Aminosäurerest-Restgruppe ausgekleidet ist. Wenn dieser saure Rest oder benachbarte Kontaktpunkte durch Mutationen verändert wurden, verlor CAT1 seine Fähigkeit, sich bei Zugabe von Aminosäuren zu stabilisieren, was deren Bedeutung für die Erkennung offenbart. Der Vergleich der Strukturen mit gebundenem Arginin, Lysin und Ornithin zeigte, dass CAT1 alle drei nahezu gleich greift und sich nur geringfügig anpasst, um Unterschiede in der Seitenkettenlänge aufzunehmen. Diese Details erklären, warum CAT1 positiv geladene Aminosäuren stark bevorzugt und neutrale größtenteils ausschließt.
Ein bewegliches Tor, das das Virus dennoch hält
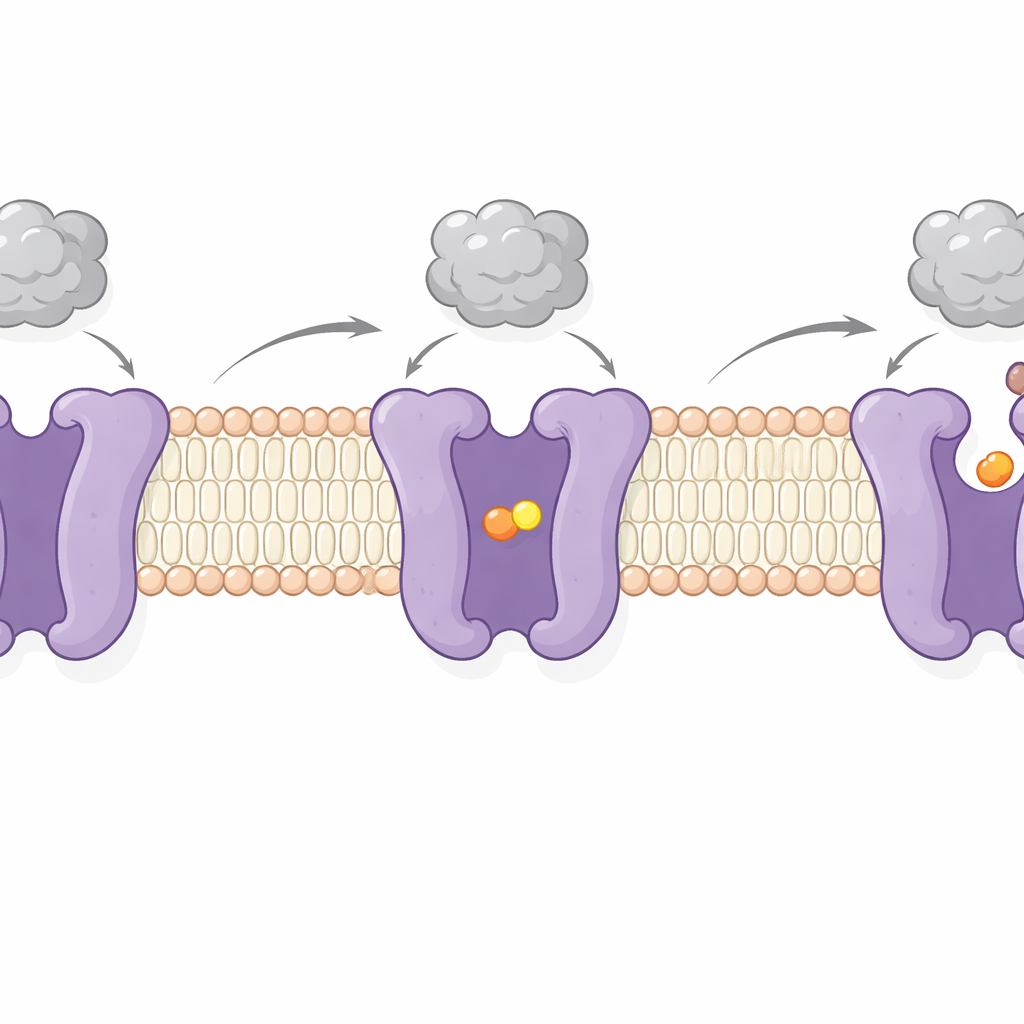
Durch die Darstellung von CAT1 mit und ohne gebundene Aminosäure erfassten die Autoren zwei Schlüsselzustände seines Arbeitszyklus. In einem ist die Frachtstelle von beiden Seiten der Membran abgeschirmt — ein „okkudierter“ Zustand, in dem die Aminosäure eingeschlossen ist. Im anderen öffnet sich die Stelle zur Zellinnenseite und ermöglicht die Freisetzung der Fracht. Diese Veränderungen beinhalten Schwenkbewegungen mehrerer membranüberspannender Segmente und ein flexibles „Riegel“-Peptid an der Innenseite, das offenbar das Öffnen zur Zellseite kontrolliert. Bemerkenswert ist, dass die virusbindende Region an der Außenseite sich nur leicht bewegt und während dieser Verschiebungen fest gebunden bleibt. Das stützt frühere Hinweise, dass virales Andocken und Aminosäuretransport weitgehend unabhängig sind — CAT1 kann die Zelle weiter mit Nährstoffen versorgen, während es gleichzeitig als viraler Rezeptor dient.
Warum diese Doppelfunktion wichtig ist
Indem genau kartiert wird, wie CAT1 sowohl Nährstoffe als auch ein Virus erkennt, klärt diese Arbeit, warum das Friend-Leukämievirus Nagetiere, aber keine Menschen infiziert: Das Virus greift eine kurze Außenschleife von CAT1 an, die zwischen den Arten deutlich unterschiedlich ist. Das Austauschen dieses Segments von der Maus in den menschlichen CAT1 reicht in Zellversuchen aus, um die virale Bindung wiederherzustellen. Die Strukturen geben zudem Hinweise darauf, wie CAT1 Zellen hilft, Argininspiegel zu erkennen und diese Information an wachstumskontrollierende Wege weiterzuleiten, und sie zeigen bestimmte Stellen, an denen Medikamente oder chemische Modifikatoren den Transport feinregeln oder den Viruseintritt blockieren könnten. Im Kern zeigt die Studie, wie ein einzelnes Membranprotein sowohl als Nährstoffventil als auch als viraler Griff fungieren kann, wobei verschiedene Seiten desselben Moleküls lebenswichtige und krankheitsfördernde Rollen übernehmen.
Zitation: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Schlüsselwörter: Aminosäuretransport, Membranproteinstruktur, virale Rezeptoren, Argininstoffwechsel, Wirtstropismus