Clear Sky Science · es
Unión de aminoácidos y de virus por el transportador catiónico de alta afinidad 1 (CAT1) de Mus musculus
Cómo las células controlan bloques vitales y afrontan invasores virales
Nuestras células dependen de un flujo constante de ciertos aminoácidos, moléculas pequeñas que construyen proteínas y alimentan reacciones clave. Al mismo tiempo, algunos virus han evolucionado para secuestrar las mismas puertas que introducen estos nutrientes en las células. Este estudio revela, con detalle atómico, cómo una de esas puertas en el ratón, denominada CAT1, transporta aminoácidos cargados positivamente a través de la membrana celular y a la vez actúa como muelle de entrada para un virus que provoca leucemia. Comprender este doble papel ayuda a explicar cómo las células detectan nutrientes, por qué algunos cánceres prosperan y por qué ciertos virus infectan a unas especies pero no a otras.
El vigilante proteico en la superficie celular
CAT1 se sitúa en la membrana exterior de la célula y se especializa en importar tres aminoácidos cargados positivamente: arginina, lisina y ornitina. Estas moléculas son esenciales para moldear proteínas, eliminar el amoníaco tóxico mediante el ciclo de la urea, activar vías de crecimiento y generar mensajeros como el óxido nítrico. Cuando CAT1 no funciona correctamente, los ratones mueren poco después del nacimiento, y en humanos el transportador relacionado está vinculado a cánceres de ovario y colon. De manera intrigante, la misma proteína también sirve como principal receptor para un retrovirus de ratón conocido como Friend murine leukemia virus, que utiliza CAT1 para reconocer e infectar células de roedores.
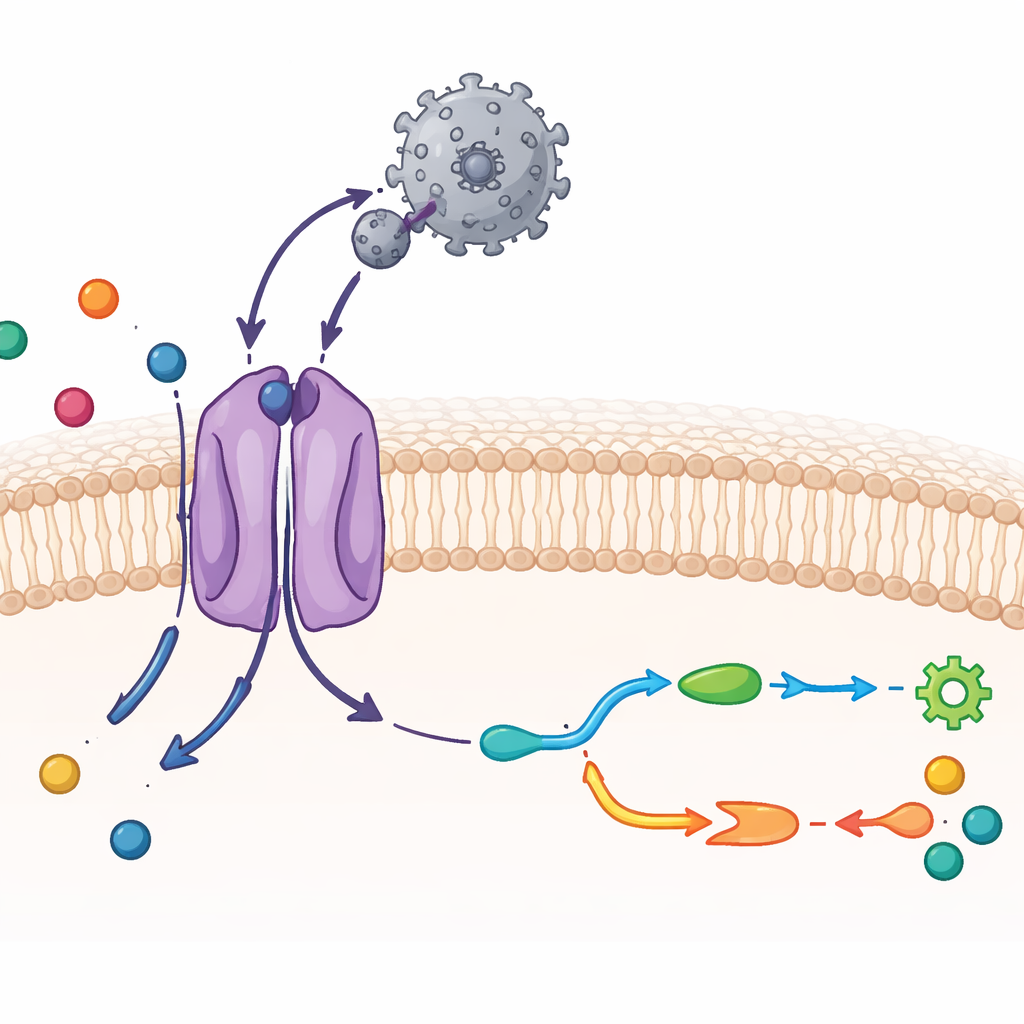
Ver CAT1 y un virus con detalle atómico
Los investigadores emplearon crio–microscopía electrónica, una técnica que imagina moléculas congeladas a resolución casi atómica, junto con ensayos bioquímicos. Purificaron CAT1 de ratón y lo mezclaron con la región externa de unión del virus, un fragmento proteico compacto que se adhiere al transportador. La estructura resultante muestra un complejo uno a uno: un único dominio de unión viral unido a una sola molécula de CAT1 en la membrana. Se pudieron visualizar la mayor parte de los 14 segmentos transmembrana del transportador, incluidas dos hélices adicionales que son únicas en esta familia. El fragmento viral abraza un bucle expuesto en el lado externo de CAT1 y forma una densa red de enlaces de hidrógeno, lo que explica su agarre extraordinariamente fuerte. Aun así, la proteína viral apenas cambia de forma, lo que contribuye a mantener esta interacción fuerte con poco coste energético.
Cómo CAT1 selecciona y mueve su carga
Dentro de CAT1, el equipo identificó el bolsillo preciso donde se unen arginina, lisina y ornitina. El esqueleto de cada aminoácido queda retenido por un anillo de átomos proteicos que forma múltiples enlaces de hidrógeno, mientras que las cadenas laterales se alojan en una cavidad revestida con grupos laterales cuidadosamente posicionados y un único residuo cargado negativamente crítico. Cuando este residuo ácido o puntos de contacto cercanos se alteraron por mutación, CAT1 perdió su capacidad de estabilizarse al añadir aminoácidos, revelando su importancia para el reconocimiento. Comparar estructuras con arginina, lisina y ornitina unidas mostró que CAT1 sujeta las tres casi de la misma manera, ajustándose solo ligeramente para acomodar diferencias en la longitud de la cadena lateral. Estos detalles explican por qué CAT1 prefiere con fuerza aminoácidos con carga positiva y excluye en gran medida a los neutros.
Una puerta en movimiento que aún mantiene al virus
Al imaginar CAT1 con y sin aminoácido unido, los autores capturaron dos pasos clave de su ciclo de trabajo. En uno, el sitio de carga queda sellado desde ambos lados de la membrana—un estado “ocluido” en el que el aminoácido está encerrado en el interior. En el otro, el sitio se abre hacia el interior celular, permitiendo la liberación de la carga. Estos cambios implican movimientos de oscilación de varios segmentos transmembrana y un péptido “cerrojo” flexible en la superficie interna que parece controlar la apertura hacia la célula. Notablemente, la región de unión viral en el exterior se mueve solo ligeramente y permanece firmemente adherida durante estos desplazamientos. Esto respalda evidencia previa de que el acoplamiento viral y el transporte de aminoácidos son en gran medida independientes: CAT1 puede seguir alimentando a la célula incluso mientras actúa como receptor viral.
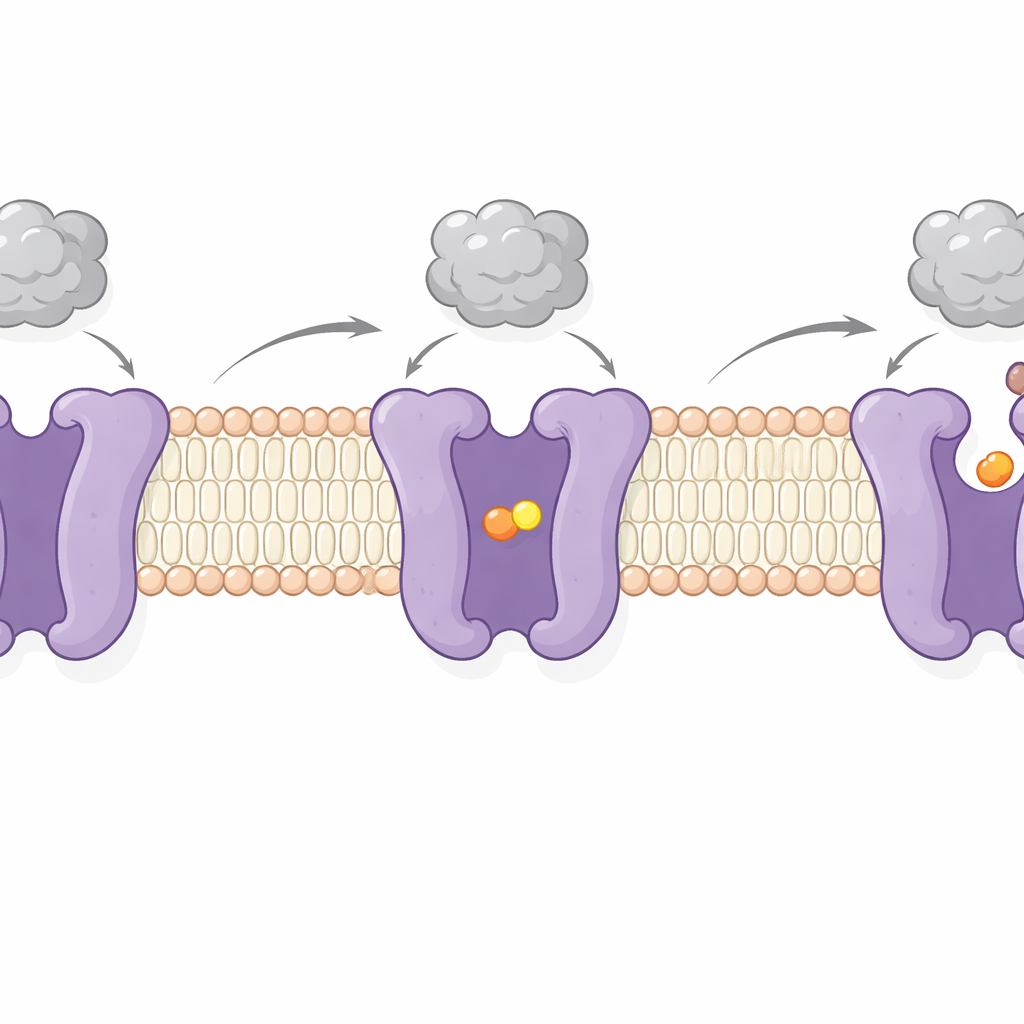
Por qué importa este doble papel
Al mapear exactamente cómo CAT1 reconoce tanto nutrientes como un virus, este trabajo aclara por qué el virus de la leucemia Friend infecta a roedores pero no a humanos: el virus se engancha a un corto bucle externo de CAT1 que difiere notablemente entre especies. Sustituir este segmento del ratón en el CAT1 humano es suficiente para restaurar la unión viral en ensayos celulares. Las estructuras también sugieren cómo CAT1 ayuda a las células a detectar los niveles de arginina y transmitir esa información a vías de control del crecimiento, y señalan sitios específicos donde fármacos o modificadores químicos podrían ajustar el transporte o bloquear la entrada viral. En esencia, el estudio muestra cómo una única proteína de membrana puede actuar tanto como válvula de nutrientes como asa para virus, con distintas caras de la misma molécula sirviendo roles que sostienen la vida y que promueven la enfermedad.
Cita: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Palabras clave: transporte de aminoácidos, estructura de proteínas de membrana, receptores virales, metabolismo de la arginina, tropismo del huésped