Clear Sky Science · ru
Связывание аминокислот и вируса высокоаффинным катионным транспортёром аминокислот 1 (CAT1) мыши (Mus musculus)
Как клетки контролируют жизненно важные строительные блоки и противостоят вирусным захватчикам
Наши клетки зависят от постоянного поступления определённых аминокислот — маленьких молекул, которые строят белки и подпитывают ключевые реакции. В то же время некоторые вирусы эволюционировали так, чтобы захватывать те же ворота, через которые эти питательные вещества попадают в клетки. В этом исследовании показано на атомном уровне, как один такой канал у мышей, называемый CAT1, одновременно переносит положительно заряженные аминокислоты через клеточную мембрану и служит точкой входа для вызывающего лейкемию вируса. Понимание этой двойной роли помогает объяснить, как клетки ощущают наличие питательных веществ, почему некоторые виды рака процветают и почему определённые вирусы инфицируют одни виды, но не другие.
Белковый привратник на поверхности клетки
CAT1 расположен в плазматической мембране клетки и специализируется на ввозе трёх положительно заряженных аминокислот: аргинина, лизина и орнитина. Эти молекулы необходимы для формирования белков, удаления токсичного аммиака через цикл мочевины, запуска путей роста и образования сигнальных молекул, таких как оксид азота. При нарушении работы CAT1 мыши гибнут вскоре после рождения, а у людей родственный переносчик связан с раком яичников и кишечника. Любопытно, что тот же белок также является основным рецептором для мышиного ретровируса Friend murine leukemia virus, который использует CAT1 для узнавания и инфицирования клеток грызунов.
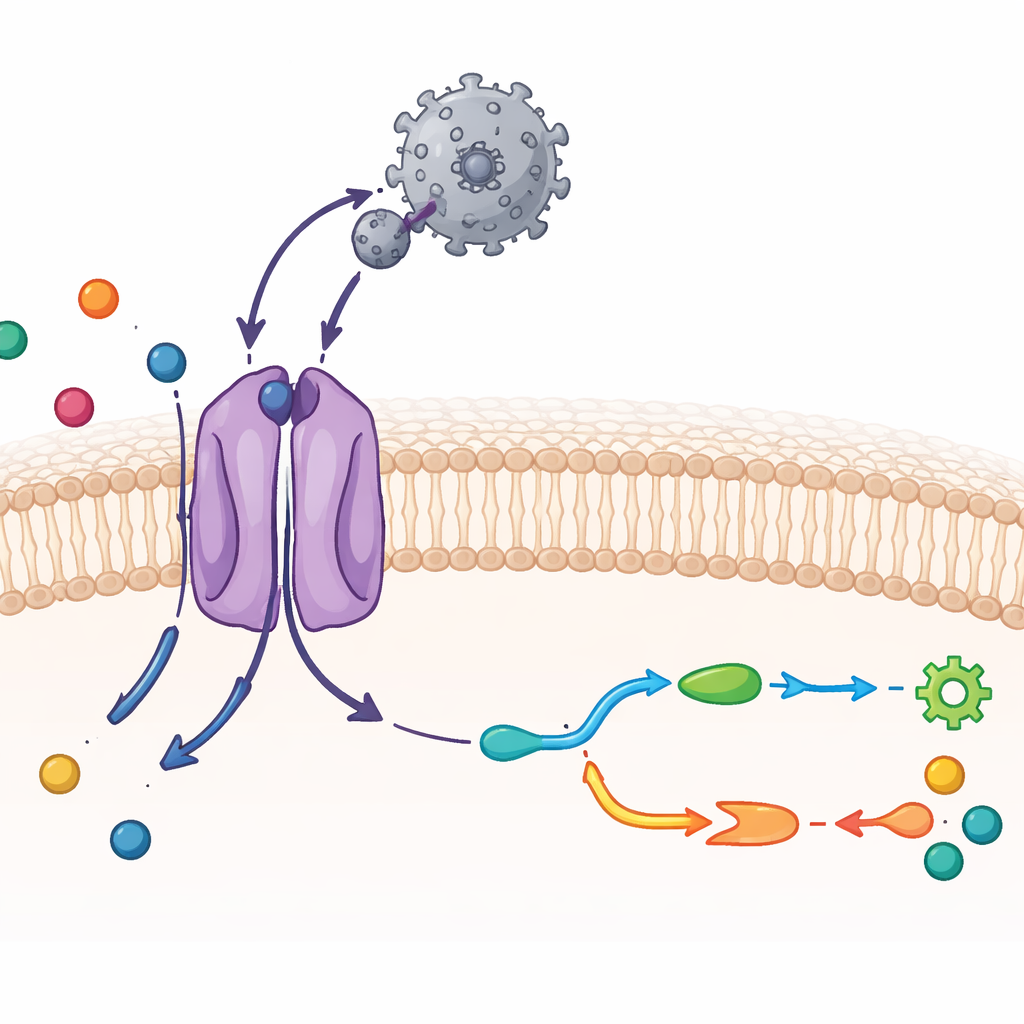
Наблюдение CAT1 и вируса на атомном уровне
Исследователи применили криоэлектронную микроскопию — метод получения изображений замороженных молекул с близкой к атомной разрешающей способностью — в сочетании с биохимическими тестами. Они очистили мышиный CAT1 и смешали его с внешней областью связывания вируса, компактным фрагментом белка, который прикрепляется к переносчику. Полученная структура показывает комплекс в соотношении один к одному: один вирусный домен связывания прикреплён к одной молекуле CAT1 в мембране. Большинство из 14 трансмембранных сегментов транспортёра удалось визуализировать, включая два дополнительных сегмента, уникальных для этого семейства. Вирусный фрагмент охватывает выступающую петлю на внешней стороне CAT1 и образует плотную сеть водородных связей, что объясняет его чрезвычайно прочное сцепление. При этом сам вирусный белок почти не изменяет форму, что помогает сохранять сильное взаимодействие с минимальными энергетическими затратами.
Как CAT1 выбирает и перемещает свой груз
Внутри CAT1 команда выявила точную карманную область, где связываются аргинин, лизин и орнитин. Главная цепь каждой аминокислоты фиксируется кольцом атомов белка, образующим несколько водородных связей, в то время как боковые цепи располагаются в полости, выстланной тщательно организованными группами боковых цепей и одной критической отрицательно заряженной остатком. Когда этот кислотный остаток или соседние контактные точки изменяли посредством мутаций, CAT1 терял способность стабилизировать связь при добавлении аминокислот, что выявило их важность для распознавания. Сравнение структур с связанными аргинином, лизином и орнитином показало, что CAT1 захватывает все три практически одинаково, лишь незначительно подстраиваясь под различия в длине боковых цепей. Эти детали объясняют, почему CAT1 сильно отдаёт предпочтение положительно заряженным аминокислотам и в значительной степени исключает нейтральные.
Двигающиеся створки, которые всё ещё удерживают вирус
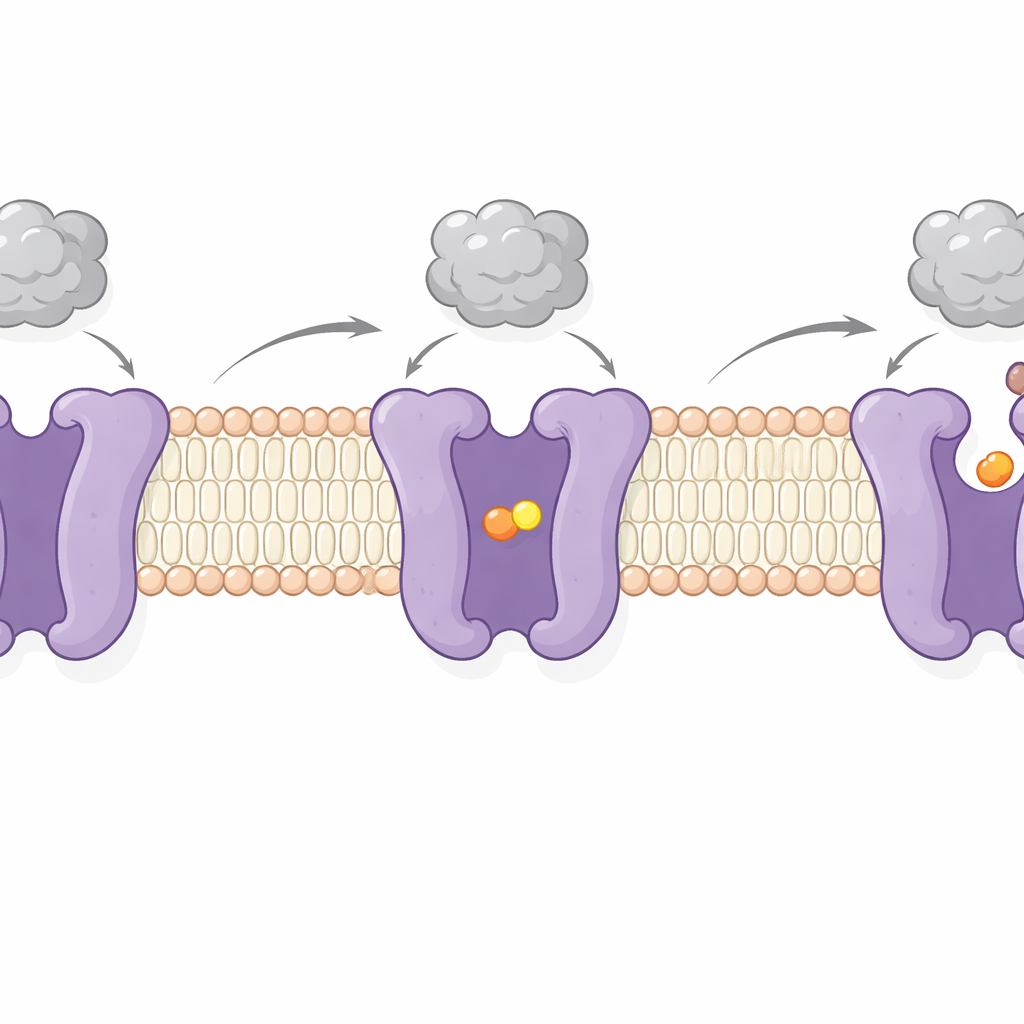
Снимки CAT1 с связанными и несвязанными аминокислотами позволили авторам зафиксировать два ключевых шага его рабочего цикла. В одном состоянии сайт для груза запечатан с обеих сторон мембраны — «окклюдированное» состояние, в котором аминокислота заключена внутри. В другом сайт открывается в сторону цитоплазмы, позволяя грузу высвободиться. Эти изменения включают маятникообразные движения нескольких трансмембранных сегментов и гибкой «застёжки» пептида на внутренней поверхности, которая по-видимому контролирует открытие в сторону клетки. Примечательно, что вируссвязывающая область на внешней стороне движется лишь незначительно и остаётся прочно прикреплённой во время этих перестроек. Это подтверждает предыдущие данные о том, что вирусная посадка и транспорт аминокислот по сути независимы — CAT1 может продолжать снабжать клетку питанием, одновременно служа вирусным рецептором.
Почему эта двойная роль важна
Точное картирование того, как CAT1 узнаёт и питательные молекулы, и вирус, проясняет, почему вирус Friend поражает грызунов, но не людей: вирус взаимодействует с короткой внешней петлёй CAT1, которая существенно различается между видами. Замена этого сегмента из мышиного варианта в человеческий CAT1 достаточно, чтобы восстановить вирусное связывание в клеточных тестах. Структуры также дают наводки на то, как CAT1 помогает клеткам чувствовать уровень аргинина и передавать эту информацию в пути контроля роста, и указывают конкретные участки, где лекарства или химические модификаторы могли бы настроить транспорт или блокировать проникновение вируса. По сути, исследование показывает, как один мембранный белок может служить одновременно клапаном для питательных веществ и ручкой для вируса, причём разные поверхности одной и той же молекулы выполняют поддерживающие жизнь и способствующие заболеванию роли.
Цитирование: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Ключевые слова: транспорт аминокислот, структура мембранных белков, вирусные рецепторы, метаболизм аргинина, тропизм хозяина