Clear Sky Science · sv
Aminosyra- och virusbindning av den högaffinitiva katjoniska aminosyra-transportören 1 (CAT1) från Mus musculus
Hur celler kontrollerar livsviktiga byggstenar och möter virusangrepp
Våra celler är beroende av ett jämnt flöde av vissa aminosyror — små molekyler som bygger proteiner och driver viktiga reaktioner. Samtidigt har vissa virus utvecklat sätt att kapra just de portar som för dessa näringsämnen in i cellerna. Denna studie visar på atomnivå hur en sådan port hos musen, kallad CAT1, både för över positivt laddade aminosyror genom cellmembranet och fungerar som infästningspunkt för ett leukemiskt virus. Att förstå denna dubbla roll hjälper oss att förklara hur celler känner av näringstillstånd, hur vissa cancerformer frodas och varför specifika virus infekterar vissa arter men inte andra.
Proteingränsvakten vid cellytan
CAT1 sitter i cellens yttre membran och är specialiserad på att ta upp tre positivt laddade aminosyror: arginin, lysin och ornithin. Dessa molekyler är viktiga för att forma proteiner, avlägsna giftig ammoniak via ureacykeln, slå på tillväxtsignaler och producera signalsubstanser som kväveoxid. När CAT1 inte fungerar ordentligt dör möss kort efter födseln, och hos människor har den närbesläktade transportören kopplats till äggstocks- och koloncancer. Intressant nog fungerar samma protein också som huvudreceptor för ett musretrovirus känt som Friend murine leukemia virus, som använder CAT1 för att känna igen och infektera gnagarceller.
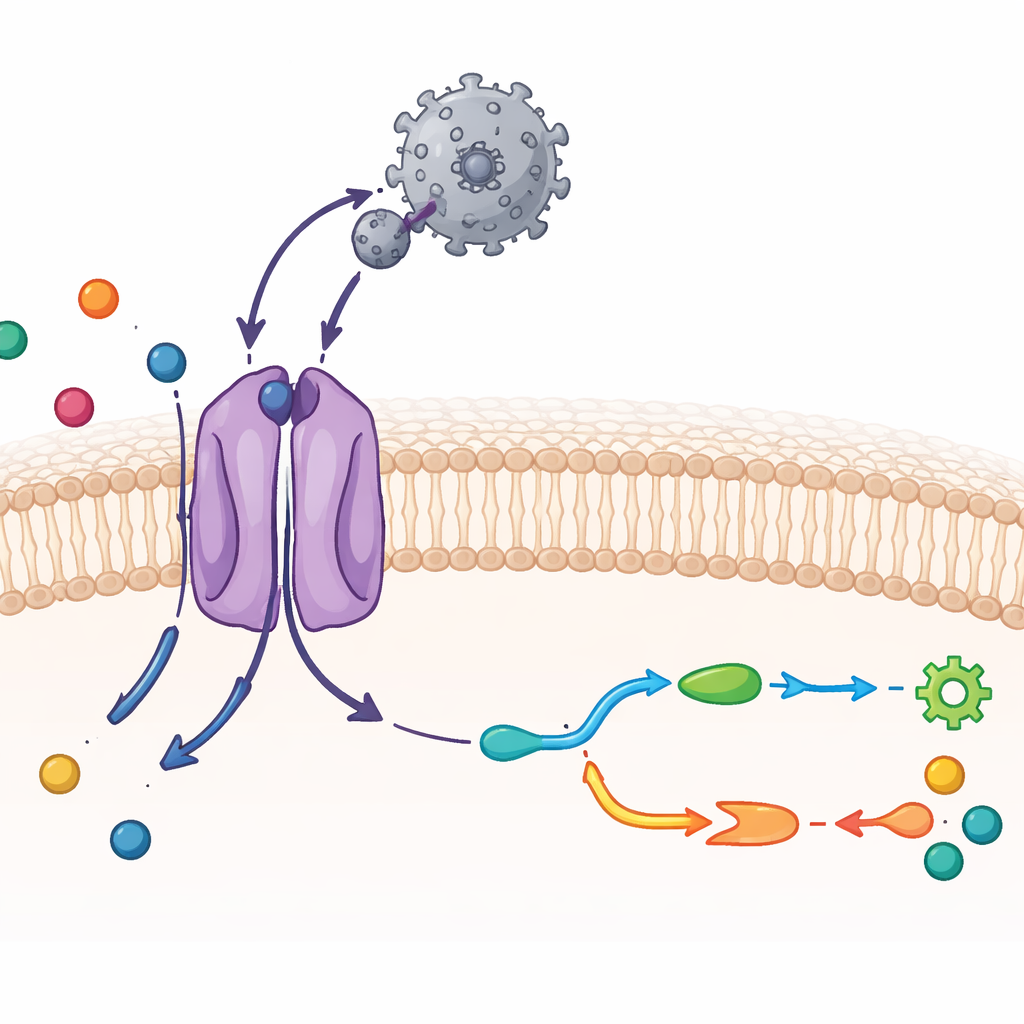
Att avbilda CAT1 och ett virus i atomär detalj
Forskarna använde kryoelektronmikroskopi, en teknik som avbildar frusna molekyler i nästan atomupplösning, tillsammans med biokemiska tester. De renade mus-CAT1 och blandade den med virusets yttre bindningsregion, ett kompakt proteinfragment som hakar fast vid transportören. Den färdiga strukturen visar ett ett-till-ett-komplex: ett enda viralt bindningsdomän fäst vid en enda CAT1-molekyl i membranet. De flesta av transportörens 14 membranöverspännande segment kunde visualiseras, inklusive två extra segment som är unika för denna familj. Virusfragmentet omsluter en exponerad slinga på CAT1:s utsida och bildar ett tätt nätverk av vätebindningar, vilket förklarar dess ovanligt starka grepp. Ändå förändras det virala proteinet knappt i formen, vilket hjälper till att upprätthålla denna starka interaktion med liten energikostnad.
Hur CAT1 väljer och förflyttar sin last
Inne i CAT1 identifierade teamet det exakta fickan där arginin, lysin och ornithin binder. Aminosyrornas ryggradsdel hålls på plats av en ring av proteinatomer som bildar flera vätebindningar, medan sidokedjorna vilar i en kavitetsomgivning klädd med noggrant placerade sidogrupper och en enda kritisk negativt laddad rest. När denna sura rest eller närliggande kontaktpunkter förändrades genom mutation förlorade CAT1 förmågan att stabilisera när aminosyror tillsattes, vilket visar deras betydelse för igenkänning. Jämförelser av strukturer med bundet arginin, lysin och ornithin visade att CAT1 griper alla tre nästan på samma sätt och justerar sig endast något för att rymma skillnader i sidokedjornas längd. Dessa detaljer förklarar varför CAT1 starkt föredrar positivt laddade aminosyror och i stor utsträckning utesluter neutrala.
En rörlig port som ändå håller fast viruset
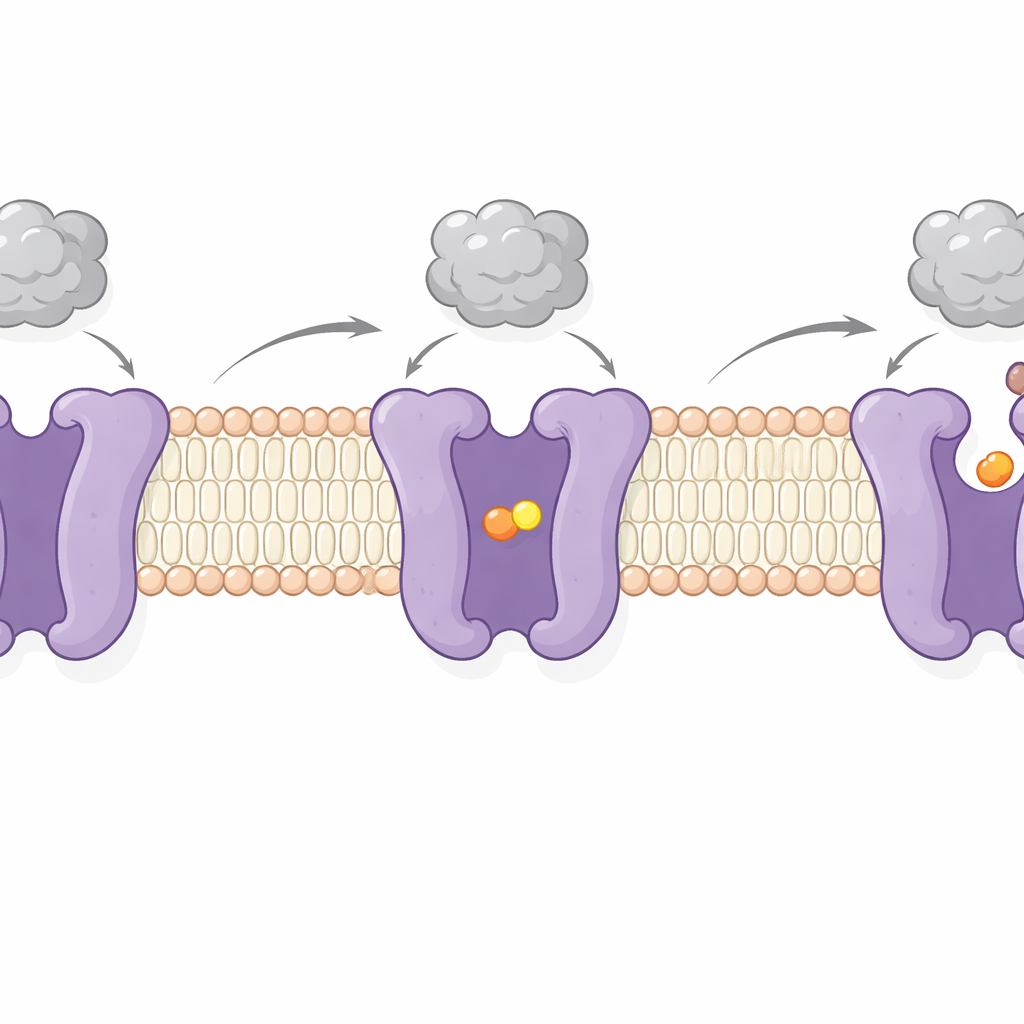
Genom att avbilda CAT1 med och utan bundet aminosyra fångade författarna två nyckelsteg i dess arbetscykel. I det ena är lastfickan förseglad från båda sidor av membranet — ett ”okkluderat” tillstånd där aminosyran är inlåst inuti. I det andra öppnar sig fickan mot cellens inre och tillåter frigivning av lasten. Dessa förändringar involverar gungande rörelser av flera membranöverspännande segment och en flexibel ”låsnings”-peptid på den inre ytan som verkar kontrollera öppning mot cellens insida. Anmärkningsvärt nog rör sig virusbindande regionen på utsidan bara något och förblir fast fäst under dessa skiftningar. Detta stöder tidigare bevis för att virusdockning och aminosyratransport till stor del är oberoende — CAT1 kan fortsätta förse cellen med näring även medan den fungerar som viral receptor.
Varför denna dubbla roll spelar roll
Genom att kartlägga exakt hur CAT1 känner igen både näringsämnen och ett virus klargör arbetet varför Friend-leukemiviruset infekterar gnagare men inte människor: viruset binder en kort yttre slinga på CAT1 som skiljer sig påtagligt mellan arter. Att byta denna segment från mus till mänsklig CAT1 räcker för att återställa viral bindning i celltester. Strukturerna ger också ledtrådar om hur CAT1 hjälper celler att känna av argininnivåer och vidarebefordra den informationen till tillväxtreglerande vägar, och de pekar ut särskilda platser där läkemedel eller kemiska modifierare skulle kunna justera transport eller blockera viral ingång. I grunden visar studien hur ett enda membranprotein kan fungera både som en näringsventil och ett viralt grepp, där olika sidor av samma molekyl tjänar livsuppehållande respektive sjukdomsfrämjande roller.
Citering: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Nyckelord: aminosyra-transport, membranproteinsstruktur, virusreceptorer, argininmetabolism, värdtropism