Clear Sky Science · nl
Aminozuur- en virusbinding door de hoogaffiene kationische aminozuurtransporter 1 (CAT1) van Mus musculus
Hoe cellen vitale bouwstenen regelen en virale indringers het hoofd bieden
Onze cellen zijn afhankelijk van een voortdurende aanvoer van bepaalde aminozuren—kleine moleculen die eiwitten opbouwen en cruciale reacties aandrijven. Tegelijkertijd hebben sommige virussen zich ontwikkeld om precies die poorten te kapen die deze voedingsstoffen de cel in laten. Deze studie onthult, tot op atomaire details, hoe één zo’n poort bij muizen, CAT1 genoemd, zowel positief geladen aminozuren over het celmembraan transporteert als dienstdoet als aanhechtingspunt voor een leukemie-veroorzakend virus. Inzicht in deze dubbele rol helpt verklaren hoe cellen nutrienten waarnemen, hoe sommige kankers gedijen, en waarom bepaalde virussen sommige soorten wel en andere niet infecteren.
De eiwitpoortwachter aan het celoppervlak
CAT1 zit in het buitenste membraan van de cel en is gespecialiseerd in het importeren van drie positief geladen aminozuren: arginine, lysine en ornithine. Deze moleculen zijn essentieel voor het vormen van eiwitten, het verwijderen van giftig ammoniak via de ureumcyclus, het inschakelen van groeipaden en het produceren van signaalmoleculen zoals stikstofoxide. Werkt CAT1 niet goed, dan sterven muizen kort na de geboorte, en bij mensen is de verwante transporter gekoppeld aan eierstok- en darmkankers. Intrigerend genoeg dient hetzelfde eiwit ook als de belangrijkste receptor voor een muizenretrovirus dat Friend murine leukemia virus heet, dat CAT1 gebruikt om knaagdiercellen te herkennen en te infecteren.
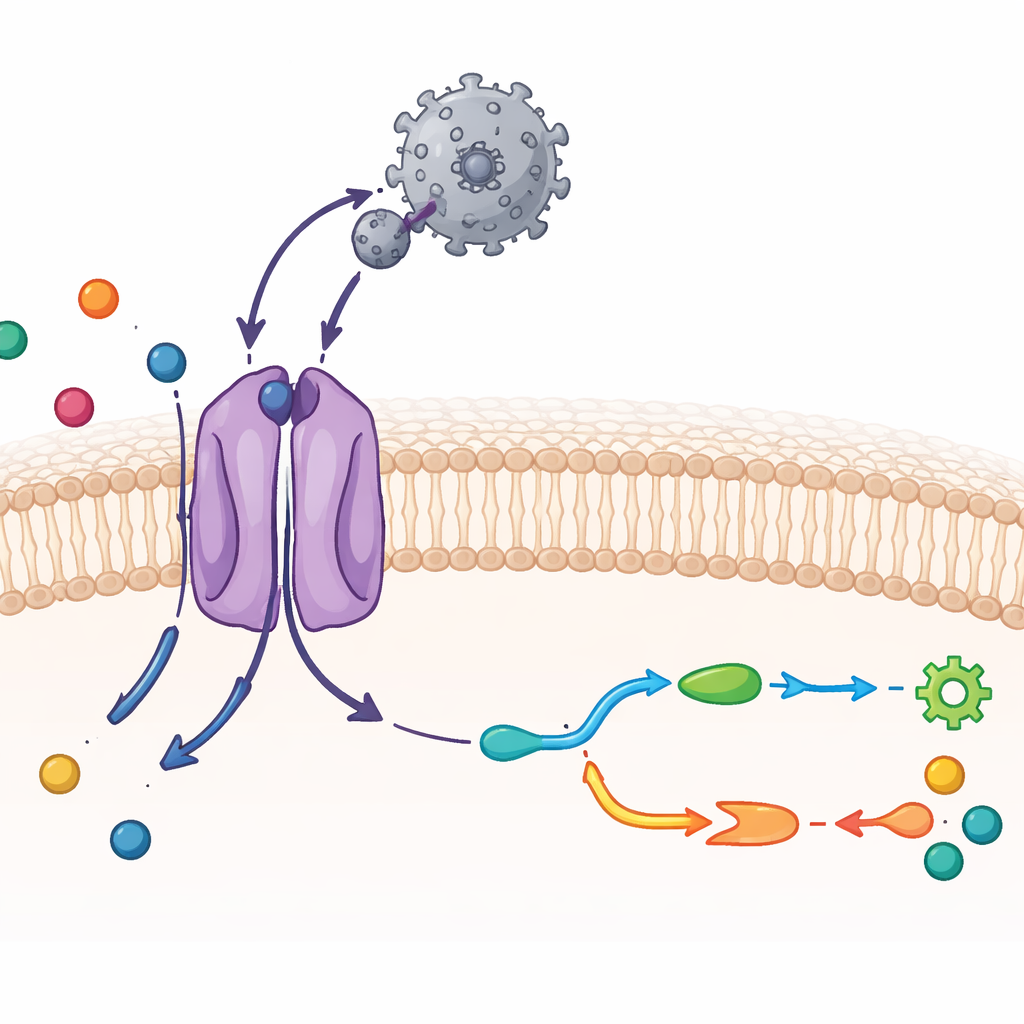
CAT1 en een virus in atomaire details zien
De onderzoekers gebruikten cryo-elektronenmicroscopie, een techniek die ingevroren moleculen bijna op atomaire resolutie afbeeldt, gecombineerd met biochemische tests. Ze zuiverden muis-CAT1 en mengden het met het virale buitenste bindingsgebied, een compact eiwitfragment dat zich aan de transporter vastklampt. De resulterende structuur toont een één-op-één complex: één viraal bindingsdomein verbonden met één CAT1-molecuul in het membraan. Het grootste deel van de veertien membraanoverspannende segmenten van de transporter kon worden gevisualiseerd, inclusief twee extra segmenten die uniek zijn voor deze familie. Het virale fragment omhelst een blootliggend lusje aan de buitenzijde van CAT1 en vormt een dicht netwerk van waterstofbruggen, wat de buitengewoon sterke greep verklaart. Toch verandert het virale eiwit zelf nauwelijks van vorm, wat helpt deze sterke interactie te behouden met geringe energetische kosten.
Hoe CAT1 zijn lading kiest en verplaatst
Binnen CAT1 identificeerde het team de precieze pocket waar arginine, lysine en ornithine binden. De ruggegraat van elk aminozuur wordt op zijn plaats gehouden door een ring van proteïneatomen die meerdere waterstofbruggen vormen, terwijl de zijketens in een holte geschoven liggen die is bekleed met zorgvuldig gepositioneerde groepen en één kritisch negatief geladen residu. Wanneer dit zure residu of nabijgelegen contactpunten door mutatie werden veranderd, verloor CAT1 zijn vermogen te stabiliseren bij toevoeging van aminozuren, wat hun belang voor herkenning aantoont. Vergelijking van structuren met gebonden arginine, lysine en ornithine liet zien dat CAT1 alle drie op vrijwel dezelfde manier vasthoudt, met slechts kleine aanpassingen om verschillen in zijketenglengte op te vangen. Deze details verklaren waarom CAT1 sterk de voorkeur geeft aan positief geladen aminozuren en neutrale aminozuren grotendeels uitsluit.
Een bewegende poort die het virus toch vasthoudt
Door CAT1 te imageren met en zonder gebonden aminozuur, vingen de auteurs twee belangrijke stappen van zijn werkcyclus. In de ene is de cargosite afgesloten van beide zijden van het membraan—een “geoccludeerde” toestand waarin het aminozuur opgesloten zit. In de andere opent de site naar het celinterieur, waardoor loslating van de lading mogelijk wordt. Deze veranderingen omvatten scharnierende bewegingen van meerdere membraanoverspannende segmenten en een flexibel “grendel”peptide aan de binnenzijde dat de opening naar de cel lijkt te regelen. Opmerkelijk is dat het virusbindingsgebied aan de buitenzijde slechts beperkt beweegt en stevig bevestigd blijft tijdens deze verschuivingen. Dit ondersteunt eerder bewijs dat virale docking en aminozuurtransport grotendeels onafhankelijk zijn—CAT1 kan de cel blijven voeden terwijl het tegelijkertijd als virale receptor fungeert.
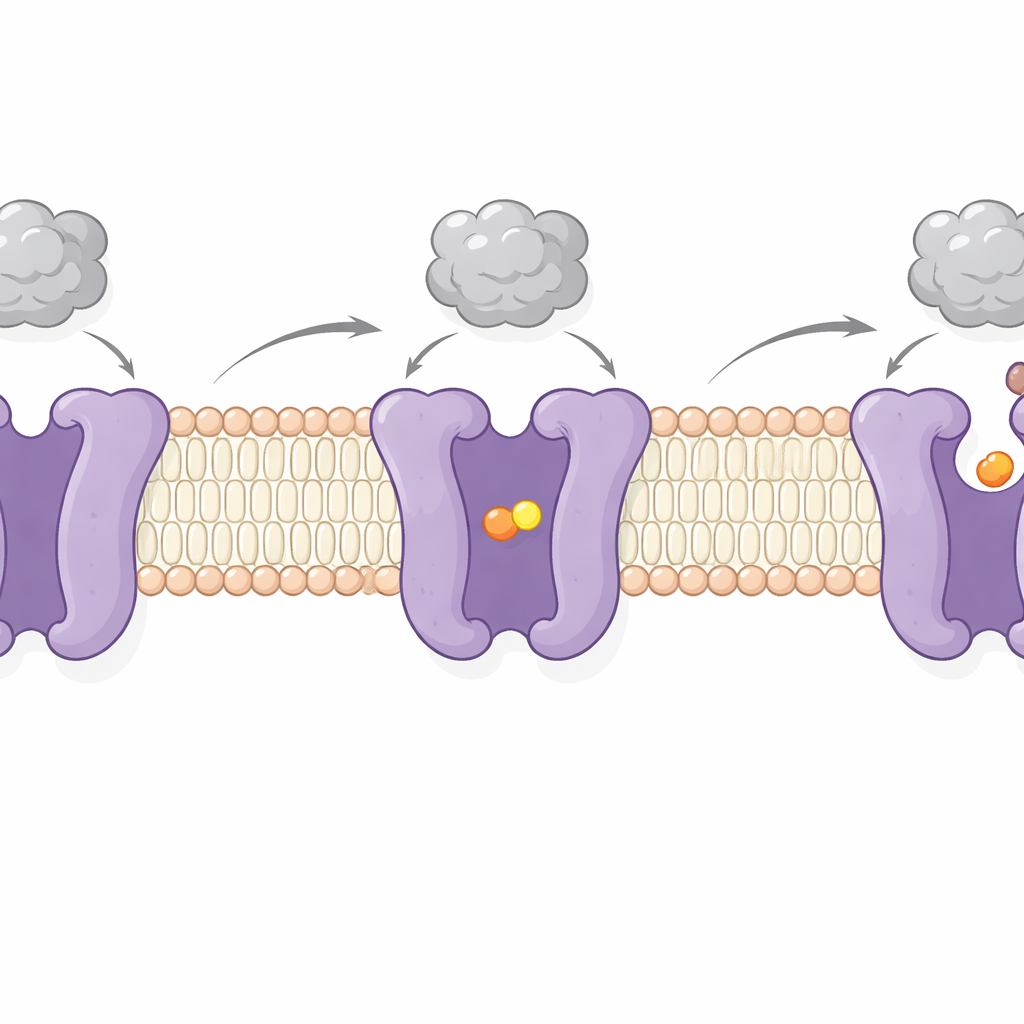
Waarom deze dubbele rol van belang is
Door precies in kaart te brengen hoe CAT1 zowel nutrienten als een virus herkent, verduidelijkt dit werk waarom het Friend-leukemievirus knaagdieren infecteert maar geen mensen: het virus grijpt een kort buitenlusje van CAT1 aan dat duidelijk verschilt tussen soorten. Het vervangen van dit segment van muis door dat van de mens is al voldoende om virale binding in celtests te herstellen. De structuren geven ook aanwijzingen hoe CAT1 cellen helpt arginine-niveaus te detecteren en die informatie door te geven aan groeiregulatiepaden, en ze wijzen op specifieke plaatsen waar geneesmiddelen of chemische modificatoren transport kunnen bijsturen of virale binnenkomst kunnen blokkeren. In wezen laat de studie zien hoe één membraaneiwit tegelijk kan fungeren als voedingsklep en als virale greep, met verschillende kanten van hetzelfde molecuul die levensondersteunende en ziektebevorderende rollen vervullen.
Bronvermelding: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Trefwoorden: aminozuurtransport, membraaneiwitstructuur, virale receptoren, argininemetabolisme, gastheer-tropisme