Clear Sky Science · pt
Ligação de aminoácidos e vírus pelo transportador catiónico de alta afinidade 1 (CAT1) de Mus musculus
Como as células controlam blocos vitais de construção e enfrentam invasores virais
Nossas células dependem de um fluxo constante de certos aminoácidos — pequenas moléculas que constroem proteínas e alimentam reações essenciais. Ao mesmo tempo, alguns vírus evoluíram para sequestrar justamente os portais que trazem esses nutrientes para dentro das células. Este estudo revela, em detalhe atômico, como um desses portais em camundongos, chamado CAT1, tanto transporta aminoácidos carregados positivamente através da membrana celular quanto atua como ponto de entrada para um vírus causador de leucemia. Compreender esse papel duplo ajuda a explicar como as células detectam nutrientes, como alguns cânceres prosperam e por que vírus específicos infectam algumas espécies e não outras.
O porteiro proteico na superfície celular
O CAT1 localiza-se na membrana externa da célula e é especializado em importar três aminoácidos carregados positivamente: arginina, lisina e ornitina. Essas moléculas são vitais para a conformação das proteínas, remoção de amônia tóxica pelo ciclo da ureia, ativação de vias de crescimento e geração de mensageiros como o óxido nítrico. Quando o CAT1 não funciona corretamente, camundongos morrem logo após o nascimento, e em humanos o transportador relacionado está associado a cânceres de ovário e de cólon. Curiosamente, a mesma proteína também serve como o receptor principal para um retrovírus murino conhecido como Friend murine leukemia virus, que usa o CAT1 para reconhecer e infectar células de roedores.
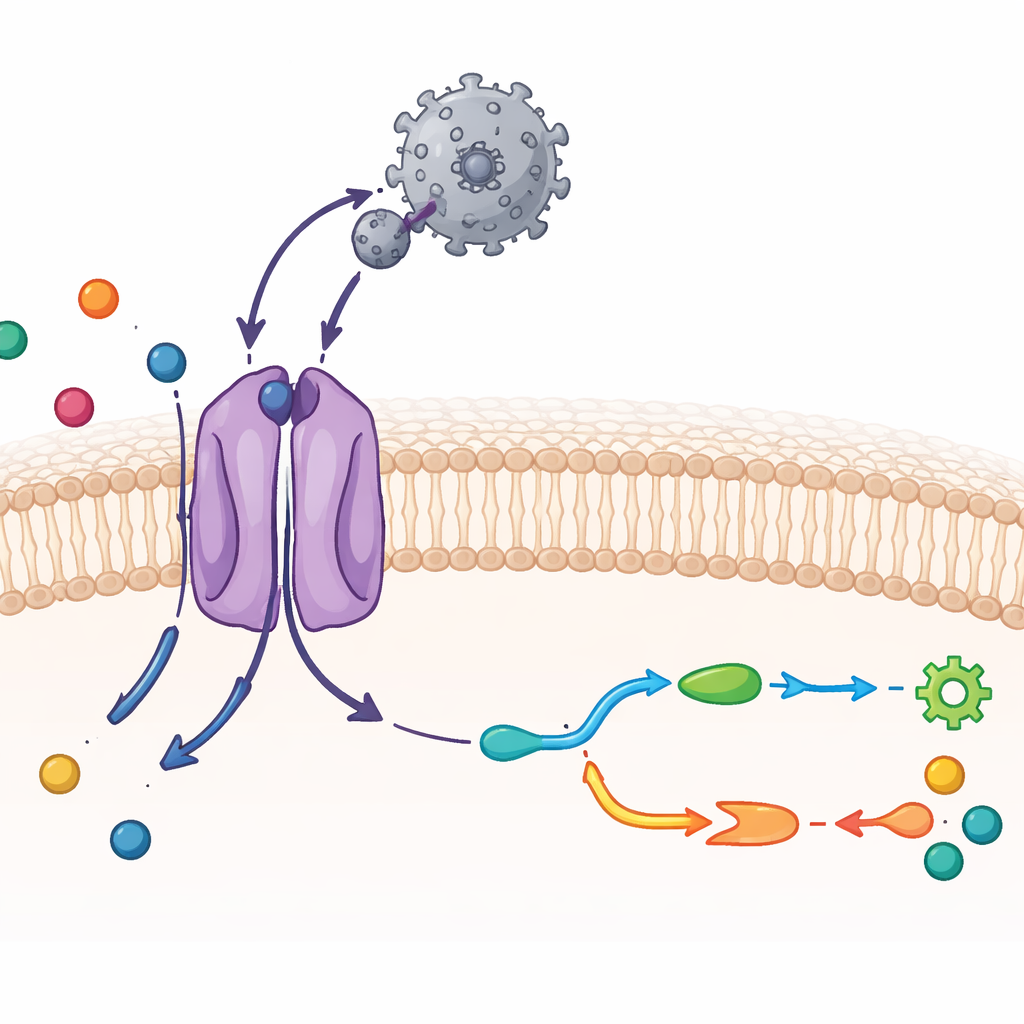
Visualizando o CAT1 e um vírus em detalhe atômico
Os pesquisadores usaram crio-microscopia eletrônica, uma técnica que imagina moléculas congeladas em resolução quase atômica, junto com testes bioquímicos. Eles purificaram o CAT1 de camundongo e o misturaram com a região externa de ligação do vírus, um fragmento proteico compacto que se prende ao transportador. A estrutura resultante mostra um complexo um-para-um: um único domínio viral ligado a uma molécula de CAT1 na membrana. A maioria dos 14 segmentos transmembrana do transportador pôde ser visualizada, incluindo dois segmentos extras que são exclusivos dessa família. O fragmento viral envolve um laço exposto no lado externo do CAT1 e forma uma densa teia de ligações de hidrogênio, o que explica sua aderência extraordinariamente forte. Ainda assim, a própria proteína viral praticamente não muda de forma, o que ajuda a manter essa interação forte com baixo custo energético.
Como o CAT1 escolhe e move sua carga
No interior do CAT1, a equipe identificou o bolso preciso onde arginina, lisina e ornitina se ligam. O esqueleto (backbone) de cada aminoácido é mantido no lugar por um anel de átomos da proteína que forma múltiplas ligações de hidrogênio, enquanto as cadeias laterais ficam encaixadas em uma cavidade revestida por grupos laterais posicionados com precisão e por um único resíduo negativo crítico. Quando esse resíduo ácido ou pontos de contato próximos foram alterados por mutação, o CAT1 perdeu a capacidade de se estabilizar ao adicionar aminoácidos, revelando sua importância para o reconhecimento. Comparar estruturas com arginina, lisina e ornitina ligados mostrou que o CAT1 prende os três de forma quase idêntica, ajustando-se apenas levemente para acomodar diferenças no comprimento da cadeia lateral. Esses detalhes explicam por que o CAT1 prefere fortemente aminoácidos carregados positivamente e, em grande parte, exclui os neutros.
Um portão móvel que ainda segura o vírus
Ao imagensr o CAT1 com e sem aminoácido ligado, os autores capturaram dois passos-chave de seu ciclo de funcionamento. Em um, o sítio de carga fica isolado de ambos os lados da membrana — um estado “ocluído” no qual o aminoácido está preso no interior. No outro, o sítio se abre em direção ao interior celular, permitindo a liberação da carga. Essas mudanças envolvem movimentos oscilantes de vários segmentos transmembrana e um peptídeo “trava” flexível na superfície interna que parece controlar a abertura para o interior da célula. Notavelmente, a região de ligação ao vírus no lado externo se move apenas ligeiramente e permanece firmemente presa durante essas alterações. Isso corrobora evidências anteriores de que o acoplamento do vírus e o transporte de aminoácidos são, em grande parte, independentes — o CAT1 pode continuar nutrindo a célula mesmo enquanto serve como receptor viral.
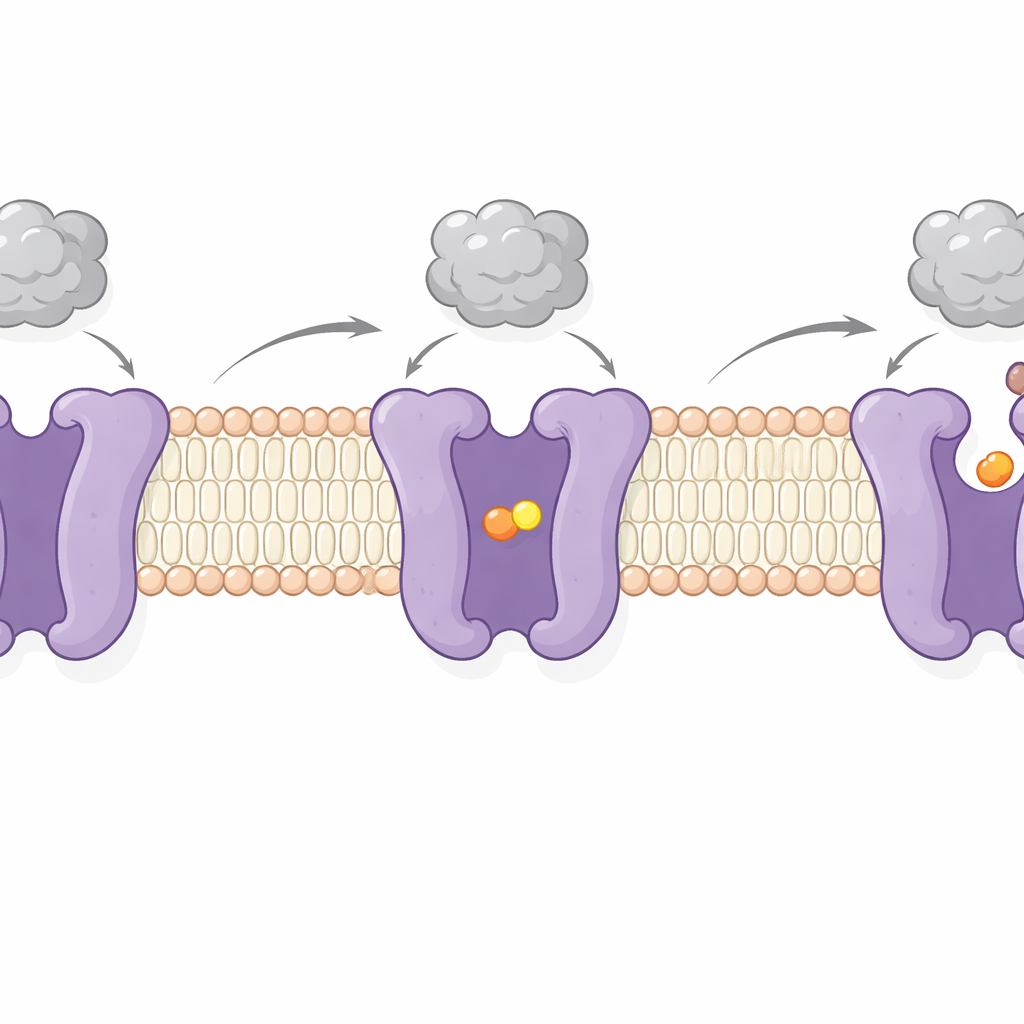
Por que esse papel duplo é importante
Ao mapear exatamente como o CAT1 reconhece tanto nutrientes quanto um vírus, este trabalho esclarece por que o Friend leukemia virus infecta roedores, mas não humanos: o vírus interage com um curto laço externo do CAT1 que difere marcadamente entre as espécies. Trocar esse segmento do camundongo para o CAT1 humano é suficiente para restaurar a ligação viral em testes celulares. As estruturas também sugerem como o CAT1 ajuda as células a detectar níveis de arginina e a transmitir essa informação para vias de controle do crescimento, e indicam sítios específicos onde fármacos ou modificadores químicos poderiam ajustar o transporte ou bloquear a entrada viral. Em essência, o estudo mostra como uma única proteína de membrana pode atuar tanto como uma válvula de nutrientes quanto como um ponto de agarramento viral, com faces diferentes da mesma molécula servindo papéis que sustentam a vida e promovem a doença.
Citação: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Palavras-chave: transporte de aminoácidos, estrutura de proteína de membrana, receptores virais, metabolismo da arginina, tropismo do hospedeiro